

А. Г. ВЫЩЕПАН, М. Е. МЕЛЬМАН
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ
СОЛЕНИЯ И КВАШЕНИЯ ОВОЩЕЙ

Москва ГОСТОРГИЗДАТ 1952
| {1} |
ПРЕДИСЛОВИЕ
Квашение и соление овощей в нашей стране получило широкое распространение как массовый вид переработки. Научные же исследования по технологии квашения значительно отстают от практики и ограничиваются главным образом изучением микробиологии молочнокислого брожения. Между тем рациональное построение всякой технологии возможно только на научной основе, так как только теоретическое осмысливание отдельных процессов и всего производства в целом дает возможность сознательно управлять им и заранее предвидеть его результаты.
Настоящая книга представляет собой попытку теоретического обобщения физико-химических исследований в области технологии квашения овощей.
Для теоретических обобщений авторы использовали опыт производственных предприятий, известные им литературные источники и свои экспериментальные исследования. Книга не претендует на исчерпывающее разрешение всех вопросов технологии квашения, но авторы надеются, что она поможет в совершенствовании производства и послужит началом более углубленных исследований в этой области.
| {2} |
ОБЩИЙ АНАЛИЗ ПРОЦЕССА КВАШЕНИЯ
ОВОЩЕЙ
Глава первая
В практике переработки овощей и технической литературе употребляют термины «соление» и «квашение» овощей. Солят огурцы, томаты, арбузы, а капусту и свеклу квасят.
Такое деление этих сходных по сущности консервирования видов переработки имеет свое историческое обоснование. В прошлом капусту и огурцы квасили без применения соли. Затем огурцы стали сохранять, заливая их раствором соли. Позднее применять соль стали и при квашении капусты. Еще до сих пор кое-где на Украине сохранился обычай квасить рубленую капусту без соли.
В настоящее время между квашением и солением как методами консервирования принципиальной разницы нет, так как в том и в другом случае консервантами являются молочная кислота и соль.
В процессе консервирования овощей при помощи молочнокислого брожения коллоиды клеточной ткани под действием соли и кислоты частично разрушаются или необратимо коагулируют, сильно набухая. Это приводит к утрате клеткой жизненных функций, вследствие чего в ней прекращаются все биохимические процессы гидролитического и окислительного характера, свойственные живой ткани. Под влиянием кислоты и соли прекращается или тормозится также жизнедеятельность большинства микроорганизмов (гнилостных бактерий и многих плесеней), действие которых в обычных условиях приводит к гибели овощей.
Возбудителями молочнокислого брожения являются различные виды молочнокислых бактерий, среди которых главное место занимают В. cucumeris fermentati и его газообразующие вариететы, В. brassicae fermentati, В. acidi lactici. По данным Я. Я. Никитинского и Б. С. Алеева, кроме этих бактерий, в квашеных овощах встречаются также В. beyerincki, В. cuntheri v. inactiva, В. ventricocus, В. listeri, В. brassicae acidae, В. leichmanni, В. hayducki, В. opacus и некоторые другие. Все эти виды молочнокислых бактерий различаются по силе кислотообразования и условиям развития. Одни из них выделяют газы, другие превращают сахар {3} в молочную кислоту без образования газов. Некоторые бактерии вырабатывают ароматические вещества (сложные эфиры). Встречающаяся иногда в огурцах длинная палочка В. abderhaldi вызывает ослизнение рассола, делает его тягучим.
Овощи солят и квасят, используя в основном самопроизвольное брожение, т. е. брожение, возбудителем которого является вся эпифитная микрофлора овощей. Следовательно, в процессе брожения принимают участие не только молочнокислые бактерии, но и ряд других микробов — дрожжи, маслянокислые и уксуснокислые бактерии, бактерии группы coli aerogenes и пр.
Насколько разнообразна и велика обсемененность овощей эпифитной микрофлорой, можно судить по данным исследований П. Г. Шугаевской, приведенным в табл. 1.
ТАБЛИЦА 1
Наименование показателей |
Содержание |
|||
в огурцах |
в капусте |
|||
свежих |
пролежавших |
свежей, хоро- |
лежалой, пло- |
|
Общее количество бактерий в 1 г..... |
50–900,5 тыс. |
3–20 млн. |
100–500 тыс. |
0,8–1,6 млн. |
Молочнокислые бактерии |
3–25 тыс. |
0,1–2,5 млн. |
5–100 тыс. |
8–500 тыс. |
Гнилостные бактерии по мпж...... |
1–8 тыс. |
20–200 тыс. |
1–27 тыс. |
14–400 тыс. |
Бактерии, выделяющие сероводород .... |
нет |
6–25 клеток |
до 20 бакт. |
25–200 бакт. |
Бактерии coli aerogenes . |
6–100 тыс. |
25–200 тыс. |
60–250 бакт. |
1–25 тыс. |
Маслянокислые бактерии |
нет |
2–25 клеток |
2–25 бакт. |
30–100 бакт. |
Уксуснокислые бактерии |
— |
— |
нет |
до 20 бакт. |
Дрожжевые грибки . . |
5–25 шт. |
10–50 шт. |
1–3 тыс. |
5–30 тыс. |
Обсемененность свежих огурцов молочнокислыми бактериями составляет всего 3–6%, а свежей капусты — от 5 до 20% общего количества микробов. Значительное место в эпифитной микрофлоре занимают гнилостные бактерии и бактерии группы coli aerogenes. Обсеменение овощей микрофлорой значительно возрастает при их хранении. Как видно из тех же данных табл. 1, общее количество бактерий на огурцах, пролежавших более суток, увеличилось в 20–60 раз и на лежалой капусте — в 3–4 раза.
Вследствие большого разнообразия эпифитной микрофлоры процесс самопроизвольного брожения принимает весьма сложный характер, так как при этом образуются продукты жизнедеятельности всех участвующих в брожении микробов. Если все же при солении и квашении овощей преобладает молочнокислое брожение, то это является результатом воздействия человека на его направленность, результатом избирательной способности самих бактерий и изменения рН среды вследствие образования молочной кислоты. {4}
Молочнокислые бактерии находят в овощах необходимые для их развития питательные вещества: белки и небелковые азотистые соединения, минеральные соли — калиевые, кальциевые, магниевые, фосфорные и пр. Легко сбраживаемые сахара овощей используются молочнокислыми бактериями в качестве источника энергии. Многие виды молочнокислых бактерий успешно развиваются в самых разнообразных температурных условиях, вплоть до 1–2° выше нуля. Это недоступно целому ряду других микробов, которые сопутствуют молочнокислым бактериям при брожении. Если это учесть, то становится понятным преимущественное развитие молочнокислых бактерий при солении и квашении овощей. Развитию молочнокислых бактерий способствует также торможение роста конкурирующей микрофлоры путем воздействия на нее различных химических и физических факторов.
Но самым существенным фактором, который задерживает развитие всех других микробиологических процессов, является образование молочной кислоты — продукта жизнедеятельности молочнокислых бактерий.
Кислотообразующая способность отдельных видов молочнокислых бактерий различна. Проф. А. П. Ситников называет такие пределы кислотообразования для некоторых видов: В. cucumeris fermentati, доминирующей в солении огурцов, — 0,88%, В. brassiсае fermentati — основного вида бактерий при квашении капусты — 1,46%, В. delbrucki — 1,7%. Однако вопрос о кислотообразовании еще недостаточно изучен. П. Г. Шугаевская, например, при внесении в рассол огурцов чистой культуры В. cucumeris fermentati обнаружила в рассоле через два месяца после засолки 0,99% молочной кислоты.
Практика самопроизвольного брожения показывает, что в благоприятных условиях в соленых огурцах накапливается до 1,2% молочной кислоты (Я. Я. Никитинский и Б. С. Алеев) и в квашеной капусте до 2%, а иногда и несколько больше (П. Г. Шугаевская и др.).
Оптимум развития большинства видов молочнокислых бактерий находится в пределах от 34 до 40° выше нуля. Но соление и квашение овощей никогда не проводят при оптимальных температурах развития молочнокислых бактерий потому, что при таких высоких температурах брожения интенсивно развиваются маслянокислые бактерии и различные потребители молочной кислоты, снижающие ее концентрацию (дрожжи типа torula, mycoderma, oidium lactis, penicillium, aspergillus и др). Вследствие развития этой нежелательной микрофлоры при повышенных температурах к концу брожения обычно накапливается молочной кислоты меньше, чем при низких температурах. Так, по нашим исследованиям, при ферментации огурцов в неохлаждаемых складах с температурой около 12–20° накапливалось кислоты максимум 0,95%, а в ледниках — 1,18%. При ферментации квашеной капусты при 21° — 1,46%, а при 2,5° — 1,59%. {5}
Хотя при солении овощей (огурцов, томатов, арбузов) и квашении капусты к концу ферментации при низких температурах молочной кислоты накапливается больше, чем при высоких, все же квашение капусты более эффективно проходит при температуре 18–24°, а соление огурцов, томатов и арбузов — при 1–5°. Это объясняется тем, что участвующие при самопроизвольном брожении молочнокислые бактерии принадлежат преимущественно к видам газообразующих. С повышением температуры брожения оно протекает интенсивнее и, следовательно, образуется больше газов. Бурное выделение газов при солении огурцов, томатов и арбузов приводит к разрыхлению их мякоти, внутренним ее разрывам и образованию пустот. Поэтому при солении овощей молочнокислую ферментацию необходимо вести замедленными темпами, избегая значительного газообразования, что достигается проведением ферментации при низких температурах. Исключение составляет лишь первоначальный период брожения при солении огурцов и томатов, или так называемая выдержка на ферментационной площадке. Эту выдержку необходимо проводить при 25–30° до накопления 0,25–0,35% молочной кислоты. Продолжается она от 24 до 48 час. и задачей ее является ускорение развития молочнокислых бактерий.
При квашении капусты бурное выделение газов не ухудшает ее качества. А так как квашение проводят в открытых чанах, то брожение должно быть ускорено, чтобы предупредить образование плесеней на поверхности капусты. Выделяющийся из капусты углекислый газ препятствует развитию поверхностной микрофлоры, подавляя ее жизнедеятельность. Однако по окончании ферментации усиленное выделение углекислого газа прекращается и создаются благоприятные условия для развития потребителей молочной кислоты. Чтобы предупредить развитие этой нежелательной микрофлоры, заквашенную капусту хранят при низких температурах (от –2 до 0°).
Проведение ферментации при солении плодовых овощей и квашении капусты в разных температурных условиях составляет основное различие этих одинаковых по существу видов консервирования.
Глава вторая
С самого начала квашения в овощах начинаются процессы, изменяющие их физические свойства и химический состав. Основные изменения сырья происходят под влиянием сбраживания сахаров молочнокислыми бактериями, являющимися факультативными анаэробами. Этот процесс (дыхание), как правило, происходит в них без участия кислорода. {6}
Для дыхания молочнокислые бактерии используют в овощах, прежде всего, шестиатомные сахара (глюкозу, фруктозу). Конечный итог процесса дыхания (брожения) обычно изображают в виде краткой схемы:
C6H12O6 |
————→ |
2C3H6O3 |
+ 18 кал. |
сахар |
молочная |
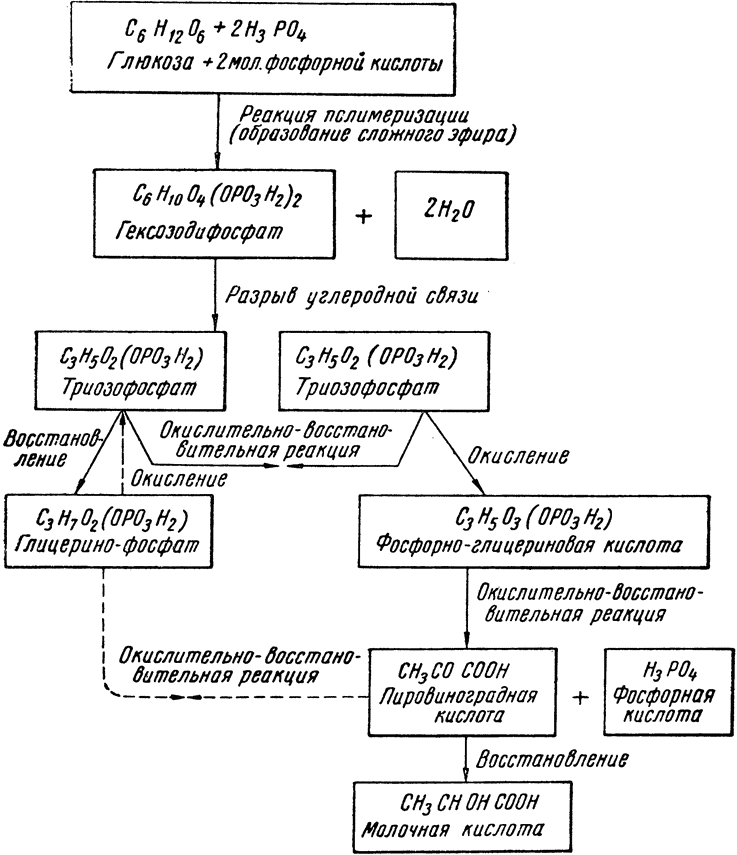
Однако процесс превращения сахаров в молочную кислоту, как показывают многие исследования, весьма сложен и проходит ряд фаз с образованием разнообразных промежуточных продуктов. Схема молочнокислого брожения по А. И. Опарину представлена ниже.
Схема молочнокислого брожения
| {7} |
Как следует из этой схемы, видную катализирующую роль в превращениях сахара играет фосфорная кислота, а молочная кислота является лишь конечным продуктом сложной цепи превращений: гексозодифосфат— триозофосфат — фосфорно-глицериновая кислота — пировиноградная кислота — молочная кислота.
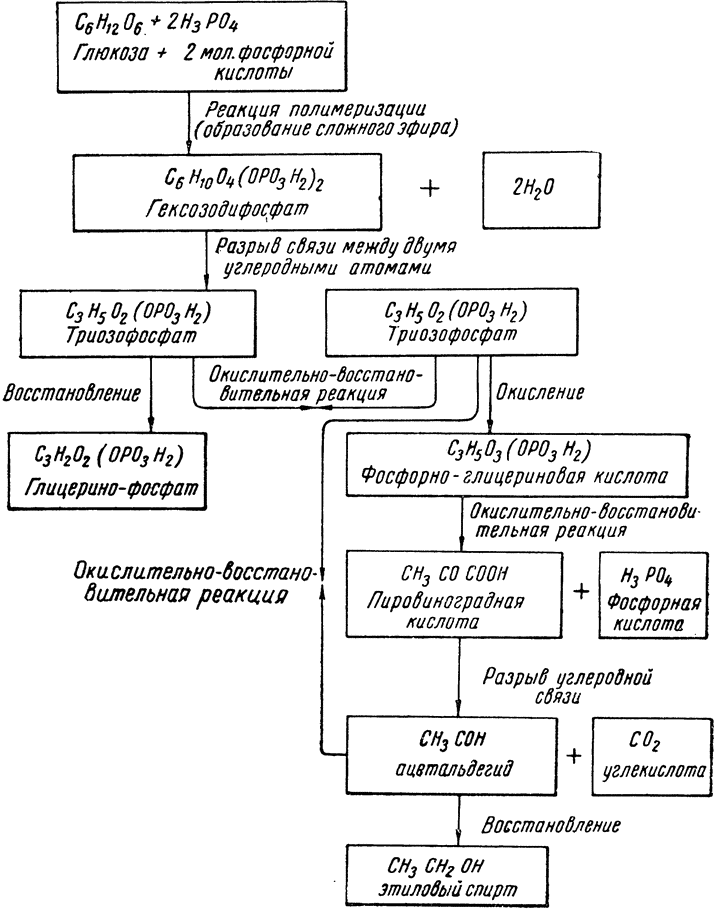
Заслуживает внимания то, что процесс превращения сахаров в спирт в большей своей части аналогичен процессу превращения их в молочную кислоту. По А. И. Опарину, спиртовое брожение проходит по схеме (см. ниже): глюкоза + фосфорная кислота — гексозодифосфат, превращающийся в триозофосфат, с выделением
Схема спиртового брожения
| {8} |
из последнего глицерино-фосфата и фосфорно-глицериновой кислоты, которая Затем превращается в пировиноградную кислоту с восстановлением фосфорной. Схемы молочнокислого и спиртового брожения тождественны до образования пировиноградной кислоты. Но дальше при молочнокислом брожении происходит восстановление пировиноградной кислоты в молочную, а при спиртовом — пировиноградная кислота распадается на ацетальдегид и углекислоту. Затем ацетальдегид восстанавливается в этиловый спирт.
Видимо, этой общностью большей части превращений следует объяснить постоянное наличие спирта при молочнокислом брожении овощей. Появление спирта вызывается не только наличием дрожжей в бродящей массе, но и образованием его некоторыми видами молочнокислых бактерий. А. П. Ситников отмечает способность к образованию спирта у В. brassicae fermentati (бактерии квашения капусты), которые в благоприятных условиях, (в сусле с мелом) могут довести его содержание до 2,4 объемного процента. В наших опытах мы наблюдали образование спирта в квашеной капусте даже при низких температурах квашения — 2–5°, при которых деятельность дрожжей почти прекращается. При этом спирт накапливался в пределах 0,2–0,3%. При более высоких температурах в капусте накапливается до 0,7% спирта.
В превращениях сахаров активную роль играют и бактерии coli aerogenes. Брожение сахаров, вызываемое этими бактериями, как отмечают Я. Я. Никитинский, А. П. Ситников и другие, сопровождается выделением углекислоты, водорода, а иногда и метана. Общий характер брожения, вызываемого В. coli, можно представить в виде следующей реакции:
2C6H12O6 + H2O ——→ |
C2H5OH |
+ CH3COOH + |
2CH3CHOHCOOH + |
2CO2 + 2H2 |
(спирт) |
(уксусная кислота) |
(молочная кислота) |
Иногда же при брожении, вызываемом этими бактериями, образуются янтарная, пропионовая и муравьиная кислоты. Таким образом, участие В. coli в брожении сахаров приводит к накоплению большого количества продуктов, наличие которых нежелательно в квашеных овощах. Этого нельзя сказать о спирте, наличие которого в небольших количествах (до 0,7%) в квашеной капусте приводит к образованию сложных эфиров, придающих ей характерный аромат и повышающих ее вкусовые достоинства.
В известных условиях в превращении сахаров принимают участие и маслянокислые бактерии, которые в качестве источников энергии используют, кроме сахаров, соли органических кислот, крахмал, пектиновые вещества, глицерин и др.
Разложение сахаров маслянокислыми бактериями идет по такой краткой схеме:
C6H12O6 ——→ C3H7COOH + 2CO2 + 2H2 + 15 кал.
| {9} |
В зависимости от состава питательной среды и условий брожения маслянокислые бактерии выделяют в качестве продуктов обмена масляную кислоту, углекислый газ, водород, а в некоторых случаях этиловый и бутиловый спирты, уксусную и муравьиную кислоты, ацетон и др.
В результате брожения сахаров и под влиянием внесенной соли происходят изменения химического состава овощей и их физических свойств. Взамен сбраживаемого сахара в овощах появляются молочная кислота, спирт и другие продукты. Уменьшается содержание азотистых веществ, часть которых затрачивается на развитие микрофлоры. Коллоиды овощей под влиянием кислот набухают, что вызывает изменение структуры плодовой мякоти и ее консистенции. Объем одних овощей (огурцы, капуста) уменьшается, других (свекла) — увеличивается. Удельный вес овощей, как правило, увеличивается, так как утраченный ими сахар, азотистые и минеральные вещества с излишком компенсируются введенной солью и образовавшимися продуктами брожения — кислотой, спиртом и пр. Кроме того, значительная часть воздуха в плодовой ткани замещается рассолом. Изменяется объем и абсолютный вес овощей, резко меняются их вкусовые и ароматические достоинства, как следствие изменения химического состава под влиянием брожения и введенных специй.
В результате всех этих изменений при квашении вырабатываются совершенно новые продукты как по химическому составу, так и по физическим свойствам и вкусовым особенностям, зачастую лишь по внешнему виду напоминающие свежие овощи.
Глава третья
Несмотря на большое разнообразие микрофлоры при самопроизвольном квашении овощей, правильным ведением процесса квашения удается обеспечить преобладание молочнокислого брожения и в большей или меньшей степени подавить все остальные побочные процессы. Достигается это воздействием на бродящую массу некоторых химических и физических факторов, к которым, прежде всего, необходимо отнести наличие соли, образующуюся при брожении молочную кислоту, эфирные масла и фитонциды специй, употребляемых при квашении, температуру квашения и газовую среду, в которой проходит брожение. К этим же факторам следует отнести и предварительную мойку овощей.
При мойке овощей значительная часть эпифитной микрофлоры смывается. Опытами установлено, что хорошо проведенной мойкой овощей удается смыть с них до 90% первоначального состава микроорганизмов. А это имеет существенное значение, особенно {10} в первый период брожения, до накопления в овощах достаточного количества молочной кислоты.
Соль при правильной ее дозировке оказывает положительное воздействие на процесс квашения овощей, помогая затормозить развитие нежелательной микрофлоры и обеспечить развитие молочнокислых бактерий. По данным Я. Я. Никитинского и Б. С. Алеева, 2% соли значительно ослабляют развитие бактерий типа coli и маслянокислых, а 3–6% задерживают развитие этих же бактерий. Отношение к соли молочнокислых бактерий несколько иное. А. Е. Насальская установила такое влияние соли на кислотообразование В. cucumeris fermentati, которое до известной степени характеризует и развитие этих бактерий (табл. 2).
|
ТАБЛИЦА 2
|
Из этих опытов следует, что 3%-ная концентрация соли оказывает весьма незначительное влияние на кислотообразование, уменьшая накопление кислоты на 10-й день всего на 12,8% по сравнению с суслом без соли. Но уже 5%-ный раствор соли снижает накопление кислоты на одну треть. Следовательно, устанавливая концентрацию соли в заквашиваемых овощах в 2–3%, можно задержать развитие бактерий группы coli и маслянокислых, не оказывая существенного влияния на развитие молочнокислых бактерий.
Такую дозировку соли (2–3%) применяют при квашении капусты и солении огурцов. Если в таре помещается 60% огурцов и 40% рассола, то, заливая огурцы 6–8%-ным раствором соли, достигают ее среднего содержания в готовом продукте от 2,4 до 3,2%.
Для того чтобы несколько задержать кислотообразование, можно повысить концентрацию соли.
Влияние образующейся при квашении овощей молочной кислоты очень эффективно при подавлении различных побочных процессов. Так, с подкислением среды, которое происходит в первые же часы квашения, прекращаются все гнилостные процессы, так как гнилостные бактерии требуют для своего развития рН среды, равной 7 и выше. Кроме того, накопление кислоты до 0,45% подавляет развитие дрожжей torula и некоторых других нежелательных микроорганизмов. Способность молочнокислых бактерий к кислотообразованию в значительной мере обеспечивает их {11} борьбу с разнообразной микрофлорой, не обладающей этим свойством. Однако следует иметь в виду, что наличие молочной кислоты в заквашиваемых продуктах не оказывает влияния на развитие спиртовых и пленчатых дрожжей, микодермы и различных плесеней, которые хорошо развиваются в кислой среде. На эту группу организмов оказывает влияние температура среды.
Влияние температуры очень существенно. По данным микробиологов, которые подтверждаются многолетней практикой соления и квашения овощей, развитие различных плесеней (тусо-derma, torula, oidium lactis, penicillium, aspergillus и пр.), а также маслянокислых бактерий подавляется низкими температурами. Известно также, что температурный минимум развития бактерий группы соli находится около 4°, дрожжей — 3–5° и уксуснокислых бактерий — 4–5°.
Но температура около 0–3° не подавляет жизнедеятельности молочнокислых бактерий, а лишь замедляет процесс кислотообразования. Несмотря на то, что ферментация в ледниках затягивается до 50–60 дней, многочисленными опытами и многолетней практикой соления огурцов установлено, что именно при этих условиях накапливается в огурцах наибольшее количество молочной кислоты. На нежинских заводах Укрторгплодоовощтреста при ледниковой ферментации огурцов содержание кислоты в них иногда достигает 1,2%, тогда как в неохлаждаемых складах такой концентрации достичь не удается.
Эффект кислотообразования при низких температурах ферментации состоит в подавлении, во-первых, всей нежелательной микрофлоры, использующей для брожения сахар, в том числе дрожжей, маслянокислых бактерий и бактерий группы coli, и, во-вторых, в подавлении жизнедеятельности различных плесеней — потребителей кислоты.
Поэтому нельзя согласиться с мнением Я. Я. Никитинского и Б. С. Алеева, которые считают, что для предохранения соленых огурцов от развития в них потребителей молочной кислоты огурцы следует перенести в помещение с сильно пониженной температурой, как только будет достигнут максимум кислотности при повышенных температурах брожения. Максимум кислотности может быть достигнут только при условии проведения главного периода брожения в низких температурах.
Побочное брожение безусловно подавляется и применением при посоле различных пряных растений, эфирные масла и фитонциды которых губительно действуют на многие микроорганизмы. Б. П. Токин на основании своих исследований и исследований других авторов пришел к заключению, что чеснок, хрен и красный перец обладают сильными бактерицидными свойствами. В то же время, как сообщает Токин, бактерии молочнокислого брожения оказались устойчивыми против фитонцидов чеснока. Судя же по практике соления овощей, применение при консервировании специй не только не оказывает губительного влияния на молочно-кислые {12} бактерии, но, повидимому, улучшает условия развития этих бактерий, устраняя с их пути конкурентов.
К числу факторов, регулирующих процесс квашения, необходимо отнести также и состав газовой среды. Молочнокислые бактерии, являясь факультативными анаэробами, не нуждаются в кислороде, а при развитии некоторых из них (бактерия Дельбрука) приток воздуха даже препятствует образованию кислоты. В то же время развитие спиртовых дрожжей в присутствии кислорода происходит энергичнее, чем без него. Пленчатые дрожжи, частые спутники всякого брожения, очень требовательны к кислороду, поэтому они развиваются преимущественно на поверхности бродящей массы. Уксуснокислые бактерии, микодерма и многие плесени являются чистыми аэробами и без доступа кислорода воздуха не развиваются. Этим в значительной мере объясняется факт предохранения от развития плесеней и уксусного скисания соленых овощей в закрытых бочках, полностью залитых рассолом. Если чаны открыты и не полностью залиты рассолом, то на поверхности квашеной капусты и других соленых овощей наблюдается дружное развитие плесеней.
Углекислый газ в количествах, образующихся при брожении не оказывает на молочнокислые бактерии отрицательного влияния.
Учитывая требовательность к кислороду многих видов сопутствующей молочнокислому брожению микрофлоры, соление и квашение овощей следует вести с максимальным ограничением притока кислорода, чтобы не допустить развития нежелательной микрофлоры.
При наиболее полном использовании всего комплекса рассмотренных нами физических и химических факторов можно и при самопроизвольном квашении обеспечить сравнительную чистоту молочнокислого брожения и получить готовые продукты высокого качества.
В некоторых случаях, желая придать молочнокислому брожению большую направленность и чистоту, овощи заквашивают чистыми культурами: В. cucumeris fermentati (для огурцов), В. brassicae fermentati (для капусты) и др.
Об эффективности применения чистых культур молочнокислых бактерий имеются разные мнения.
П. Г. Шугаевская, специально изучавшая этот вопрос, пришла к выводу, что общее направление микробиологических процессов при квашении огурцов и капусты чистыми культурами и обычным способом по сути одинаково. Отличие заключается лишь в скорости прохождения основных процессов — при квашении чистыми культурами быстрее накапливается молочная кислота. Такого же мнения придерживаются проф. И. А. Веселовский, М. М. Макарова и Н. П. Кирьялов.
Г. К. Титоренко, П. Г. Сорокин и некоторые другие авторы нашли, что применение чистых культур при квашении овощей не только ускоряет кислотообразование, но придает молочнокислому {13} брожению большую направленность и чистоту и способствует повышению качества квашеных овощей. Это же мнение отражено в производственных инструкциях Укрглавплодоконсерва и Центроплодоовоща. Проф. Г. Г. Скробанский установил, что при квашении капусты чистыми культурами лучше сохраняется витамин С.
Отсутствие единого мнения у исследователей этого вопроса объясняется разными условиями экспериментирования. Результаты исследований зависят от многих факторов: степени обсемененности эпифитной микрофлорой сырья, условий ферментации овощей с применением чистых культур и без них, хозяйственно-ботанических сортов сырья и прочих, которые у разных авторов были различными. Не останавливаясь на разборе отдельных исследований, мы все же должны отметить единодушное мнение о том, что применение чистых культур при квашении овощей ускоряет процесс кислотообразования. Это настолько существенно, что делает желательным применение чистых культур, как одного из регулятивных факторов. Особенно желательно применение чистой культуры негазообразующего вида В. cucumeris fermentati при солении плодовых овощей (например, арбузов). Это имеет наибольшее значение при проведении ферментации в неохлаждаемых помещениях. При самопроизвольном брожении развиваются газообразующие вариететы В. cucumeris fermentati и другие газообразующие виды молочнокислых бактерий. Под давлением образующихся газов, что зависит от интенсивности брожения, плодовая мякоть разрыхляется, образуются пустоты, а иногда (в арбузах) происходит почти полное разрушение мякоти. Таким образом, применение чистых культур негазообразующих бактерий будет способствовать сохранению структуры плодовой ткани консервируемых овощей и, следовательно, повышению их качества.
Результаты применения чистых культур при квашении капусты несколько иные. При квашении капусты применяют чистую культуру газообразующего вида В. brassica fermentati в смеси с чистой культурой дрожжей. Ввиду некоторых особенностей квашения капусты образование газов, скопляющихся на поверхности капусты в дошниках, при ее ферментации очень желательно.
Применение чистых культур при квашении капусты улучшает ее вкусовые качества. Если квашение производится поздней осенью при низких температурах, то применение чистых культур ускоряет процесс кислотообразования. Качество квашеной капусты в случае окончания ее ферментации при оптимальных температурах (21–24°) улучшается, если применяются чистые культуры и если готовый продукт хранится при низких температурах. Если же капуста хранится в неохлаждаемых помещениях, то эффект повышения качества, достигнутый при ферментации, утрачивается при хранении, и применение чистых культур, в конечном итоге, не дает положительных результатов.
| {14} |
Глава четвертая
Огурец (Cucumis sativus L.) представляет собой однолетнее травянистое стелющееся растение, принадлежащее к семейству тыквенных (Cucurbitaceae).
Плод огурца — ложная ягода, которая используется в свежем виде и для переработки в стадии зеленца, т. е. в незрелом состоянии.
Основными морфологическими признаками, определяющими технологические свойства огурцов, являются поверхность, форма, размер, окраска плода и размер семенного гнезда.
По характеру поверхности различают огурцы гладкие (галаховские), мелкобугорчатые (муромские, вязниковские) и крупнобугорчатые (нежинские, крымские, борщаговские, должик, чернобривец и др.).
Форма огурцов разнообразна. С. Г. Габаев выделяет шесть основных форм огурцов: шаровидную, эллипсоидальную, яйцевидную, обратнояйцевидную, веретеновидную и цилиндрическую. Могут быть еще и производные формы. Большинство сортов огурцов в поперечном разрезе имеют форму круга, трехгранника с закругленными концами или промежуточную между ними форму. Иногда вдоль плодов идут мелкие или глубокие борозды, что является типичным признаком ряда сортов.
Однако присущая определенному сорту огурцов форма может резко изменяться в зависимости от условий произрастания. Под влиянием неблагоприятных условий образуются различные искривления, уродующие форму плода (кубарики, крючки и пр.).
Огурцы используются в разных стадиях развития плода — от пятидневной завязи, длиной 2–2,5 см, до хорошо развитого плода, но зеленой окраски с мягкими, неогрубевшими семенами (зеленец).
Размеры огурцов у разных сортов различны. Наиболее распространенные сорта огурцов имеют длину плода до 15 см, но встречаются сорта, плоды которых достигают 70 см в длину.
| {15} |
ТАБЛИЦА 3
Наименование сорта огурцов |
Зеленец |
||||||||
форма |
поверхность |
окраска |
рисунок по длине плода |
индекс формы |
размер |
скороспелость |
мякоть плода |
размер семенного гнезда |
|
Муромские |
Коротко-яйцевидная и эллипсоидальная |
Мелкобугорчатая |
Светлозеленая |
До 3/4 |
1–1,6 |
Мелкий |
Скороспелый |
Тонкая, рыхлая |
Большое |
Вязниковские |
Удлиненно-яйцевидная и эллипсоидальная |
То же |
То же |
До 2/3 |
1,7–2,5 |
Средний |
То же |
То же |
„ |
Неросимые |
Удлиненно-яйцевидная |
Крупнобугорчатая |
Темнозеленая |
До 1/2 |
2,0-2,5 |
„ |
Среднеспелый |
Тонкая, средней плотности, полухрустящая |
„ |
Берлизовские |
Удлиненно-овальная |
То же |
То же |
До 1/2 |
2,5 |
„ |
То же |
Средней толщины, хрустящая |
Среднее |
Нежинские |
Цилиндрическая и удлиненно-яйцевидная |
Крупнобугорчатая и ребристая |
Темнозеленая и зеленая |
От 1/3 до 1/2 |
2,4-2,6 |
„ |
Среднепоздний |
Средней толщины, плотная, хрустящая |
„ |
Чернобривец |
Коротко-яйцевидная и овальная |
Крупнобугорчатая |
Темнозеленая |
До 1/2 |
1,3–1,6 |
Мелкий |
Скороспелый |
То же |
Небольшое |
Борщаговские |
Цилиндрическая, сбежистая к плодоножке |
Крупнобугорчатая и слаборебристая |
То же |
До 1/2 |
2,6-2,7 |
Крупный |
Среднепоздний |
„ |
Среднее |
Крымские |
Удлиненно-яйце-видная и цилиндрическая |
Крупнобугорчатая и ребристая |
„ „ |
От 1/4 до 1/2 |
3,3 |
„ |
То же |
Толстая, плотная, хрустящая |
„ |
Рябчик |
Цилиндрическая, слабо сбежистая |
Крупнобугорчатая и ребристая |
Зеленая и светлозеленая |
От 1/4 до 3/4 |
2,5-2,6 |
Средний |
„ „ |
Средней толщины, хрустящая |
„ „ |
Должик |
Удлиненно-овальная, вытянутая к плодоножке |
Крупнобугорчатая |
Зеленая |
До 1/2 |
2,5-3,0 |
Крупный |
„ „ |
То же |
„ „ |
Плоды огурцов бывают короткие (отношение длины к толщине1 — 1,5–2), полудлинные (индекс формы свыше 2 до 2,5) и длинные (свыше 2,5).
Окраска плодов в состоянии хозяйственной спелости зеленая, но разной интенсивности и различного рисунка. Если интенсивность окраски может варьировать внутри сорта в зависимости от условий произрастания, то рисунок является характерным сортовым признаком. У одних сортов огурцов по зеленому фону располагаются светлые полосы, у других этих полос нет; у одних сортов полосы размытые, у других — резко очерченные; у одних на вершине лысинка в виде белого пятна, у других ее нет и т. д.
Размер семенного гнезда является весьма существенным показателем, так как семенное гнездо — это наименее плотная часть плодовой мякоти, которая подвергается наибольшим структурным изменениям в процессе ферментации. Поэтому, чем меньший объем занимает в плодах семенная камера, тем это лучше. Кроме того, наблюдениями установлено, что чем больше размер семенной камеры, тем ткань ее рыхлее и семена крупнее. {16} Рыхлость ткани семенной камеры при солении приводит к образованию пустот и ослизнению ткани камеры. Н. Г. Рагулин1 объясняет образование пустот в огурцах с большой семенной камерой тем, что под действием плазмолиза в плодах происходит сжатие ткани в направлении от центра, где ткань обладает наиболее слабым межклеточным сцеплением, к более прочной внешней части плода — оболочке.
Не все сорта огурцов одинаково пригодны для соления. Лучшими для этого вида консервирования надо считать те сорта, которые в соленом виде сохраняют плотную структуру ткани, первоначальный объем, вес и окраску, а также обладают хорошими вкусовыми достоинствами.
Поэтому изучение влияния сортовых особенностей огурцов на качество готовых продуктов представляет значительный интерес.
В табл. 3 дается морфологическое описание десяти сортов огурцов, наиболее часто употребляющихся для засолки2. {17}
Средний химический состав огурцов (в процентах) в стадии съедобной зрелости, по данным отечественных исследователей, следующий:
Воды..... |
95–96 |
Кислоты (в пересче- |
0,07–0,13 |
|
Сахаров . . . . |
1,1–2,75 |
|||
Азотистых веществ |
0,75–1,55 |
Минеральных ве- |
0,35–0,57 |
|
Клетчатки |
0,39–0,68 |
|||
Пектиновых веществ |
0,15–0,30 |
Витамина С . . . |
5,0–12,58 мг% |
Колебания в содержании отдельных составных элементов и сухих веществ в целом находятся в зависимости от условий выращивания огурцов, стадии развития, сортовых особенностей и ряда других факторов.
Химический состав свежих огурцов в различной стадии зрелости по Ф. В. Церевитинову характеризуется такими данными (табл. 4):
|
ТАБЛИЦА 4
| |||||||||||||||||||||||||||||||||||
Химический состав нежинских огурцов различных размеров по принятой в промышленности сортировке по нашим исследованиям следующий (табл. 5):
ТАБЛИЦА 5
Размер огурцов |
Длина плодов (в см) |
Химический состав (в %) |
Витамин C (в мг%) |
||||||
вода |
сухие вещества |
общий сахар |
азотистые вещества |
пектиновые вещества |
зола |
клетчатка |
|||
Корнишоны |
5–7 |
93,91 |
6,09 |
1,6 |
1,76 |
0,28 |
0,76 |
0,54 |
12,9 |
Мелкие |
7–9 |
93,9 |
6,10 |
2,1 |
1,86 |
0,28 |
0,67 |
0,53 |
11,11 |
Средние |
9–12 |
94,78 |
5,22 |
2,4 |
1,13 |
0,24 |
0,53 |
0,69 |
10,84 |
Крупные зеленые . . . |
12–14 |
95,25 |
4,75 |
2,27 |
0,97 |
0,18 |
0,45 |
0,72 |
7,94 |
Крупные желтые . . . |
9–14 |
95,04 |
4,96 |
2,35 |
0,94 |
0,15 |
0,45 |
0,74 |
6,58 |
Как видно из таблицы, по мере созревания огурцов содержание сухих веществ в них уменьшается, что соответственно вызывает увеличение содержания влаги. Уменьшение количества сухих веществ сопровождается увеличением общего количества сахара. Количество азотистых, пектиновых и минеральных веществ по мере созревания огурцов уменьшается, но содержание клетчатки значительно повышается. {18}
Уменьшение содержания коллоидов (азотистых веществ и пектина) в огурцах по мере созревания значительно понижает их технологические свойства. Наличие коллоидов, являющихся важнейшей составной частью плодовой ткани, обусловливает сохранение ее структуры при солении.
С развитием огурцов содержание в них витамина С уменьшается с 12,9 мг% в корнишонах до 6,58 мг% — в крупных желтых.
Изучение химического состава различных хозяйственно-ботанических сортов огурцов, особенно для предприятий, перерабатывающих их в различные консервы, представляет значительный интерес.
Химический состав некоторых хозяйственно-ботанических сортов огурцов (Харьковской обл.) по нашим исследованиям приводится в табл. 6.
|
ТАБЛИЦА 6
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Анализируя эти данные, можно прийти к выводу, что по общему содержанию сухих веществ сорта огурцов мало чем отличаются один от другого. На общем фоне можно только отметить крайние колебания у сорта чернобривец (5,2) и берлизовских (4,68). Очевидно, при выращивании разных сортов огурцов в одинаковых климатических и почвенных условиях разница в общем количестве сухих веществ невелика. Но содержание некоторых из них, в частности общего сахара, азотистых веществ и витамина С, под влиянием индивидуальных особенностей сортов колеблется более значительно.
По содержанию сахара (2,75–2,74) выделяются сорта крымские, чернобривец и рябчик. Несколько меньше сахара содержат нежинские и берлизовские (2,46–2,45), еще меньше его обнаружено в сортах борщаговские и должик (2,28–2,26). В вязниковских и неросимых огурцах оказалось наименьшее количество сахара (2,0–2,04).
Содержание азотистых веществ у большинства сортов находится в пределах от 1,2 до 1,3% (за исключением сорта чернобривец — 1,55%, берлизовские — 1,08%). {19}
Для технологии соления очень существенно содержание в огурцах сахара как источника образования кислоты и азотистых веществ как коллоидов.
По содержанию сахара на последнем месте среди указанных сортов стоят неросимые и вязниковские, а по содержанию азотистых веществ — берлизовские огурцы.
По количеству витамина С можно различить две группы: с содержанием его свыше 10 и до 12,5 мг% и с содержанием 7–7,35 мг%. К первой группе относятся сорта нежинские, крымские, должик, рябчик, борщаговские, а ко второй — неросимые, вязниковские и берлизовские. Сорт чернобривец занимает промежуточное место — 9,1 мг%. Хотя витамина С в огурцах содержится незначительное количество, все же следует отметить, что и в этом отношении сорта неросимые, вязниковские и берлизовские стоят на последнем месте.
На химический состав огурцов несомненно существенное влияние оказывают почвенные и климатические условия их выращивания. Химический анализ огурцов сорта нежинские, выращенных в Полтавской, Сумской, Харьковской, Черниговской и Киевской областях, показал колебания в содержании азотистых веществ и сахара до 25%, пектина, клетчатки и золы до 50% и витамина С до 30%. Если такие колебания в химическом составе наблюдаются в огурцах, выращенных в близко расположенных областях, то, очевидно, следует ожидать более значительных отклонений в химическом составе огурцов, выращенных в различных климатических зонах.
Следовательно, эти факторы — климат и почва — необходимо признать решающими в их влиянии на химический состав, а отсюда и на технологические свойства огурцов.
Химический состав отдельных частей плода огурцов также неодинаков. Исследования химического состава отдельных частей плода огурцов сорта нежинские в стадии съедобной зрелости, приведенные в табл. 7, показывают, что в мякоти плодов огурцов
ТАБЛИЦА 7
Части плода |
Содержание (в %) |
Витамин C (в мг%) |
|||||||||
влаги |
глюкозы |
фруктозы |
сахарозы |
общего количества сахара |
кислоты (в пересчете на яблочную) |
азотистых веществ |
пектиновых веществ |
клетчатки |
золы |
||
Кожица ....... |
95,2 |
0,72 |
0,32 |
— |
1,04 |
0,17 |
0,79 |
— |
0,78 |
0,82 |
10,0 |
Мякоть ....... |
95,83 |
1,44 |
0,44 |
0,20 |
2,08 |
0,10 |
1,04 |
0,34 |
0,48 |
0,40 |
9,34 |
Семенная камера . . . |
95,70 |
1,80 |
0,22 |
0,24 |
2,26 |
0,17 |
1,12 |
0,39 |
0,61 |
0,51 |
9,28 |
сахара содержится в два раза больше, чем в кожице, и что наиболее богата им семенная камера. Азотистых веществ больше всего в семенной камере, что вполне естественно, так как в ней {20} находятся богатые азотом семена. Пектиновые вещества почти одинаково распределены в мякоти и семенной камере, а в кожице их не обнаружено. Кожица наиболее богата клетчаткой, золой и витамином С.
На качество соленых огурцов и их весовые изменения оказывают влияние не только химические, но и физические показатели: содержание воздуха в тканях огурцов, плотность кожицы, объем семенной камеры, удельный вес плода.
Физические свойства огурцов по мере их развития изменяются, как это видно из данных табл. 8, в которой приведен анализ нежинских огурцов на разных стадиях зрелости. Наибольший
|
ТАБЛИЦА 8
|
удельный вес у корнишонов — 0,972. По мере развития и созревания огурцов он уменьшается, доходя до 0,910 у крупных желтых огурцов. Это вызвано увеличением количества воздуха в тканях плодов, содержание которого возрастает от 4,8% у корнишонов до 10,6% у крупных желтых огурцов. По мере созревания огурцов увеличивается и относительный объем семенной камеры (в процентах к объему плода).
Для соления лучше употреблять огурцы в стадии зрелости корнишонов (50–70 мм). Корнишоны содержат примерно 4–5 объемных процентов воздуха. Наличие такого количества воздуха в тканях огурцов обеспечивает достаточную ее платность и вместе с тем возможность полного пропитывания плодовой мякоти рассолом. Меньшее содержание воздуха приводит к слишком замедленной ферментации и, очевидно, в связи с этим к ухудшению качества соленых огурцов. Но и большое содержание воздуха тоже отрицательно сказывается на качестве огурцов. Увеличение количества воздуха в тканях свыше 8%, характеризующее старение ткани или слишком рыхлое ее строение, уже приводит к образованию пустот в соленых огурцах. Плодовая ткань при старении, видимо, утрачивает способность удерживать рассол вследствие глубоких изменений коллоидной системы.
Нами исследованы физические свойства некоторых хозяйственно-ботанических сортов огурцов в ранней стадии развития (длина 50–70 мм).
Результаты исследований приведены в табл. 9.
| {21} |
|
ТАБЛИЦА 9
|
Из данных табл. 9 видно, что нежинские и крымские сорта огурцов имеют наименьшую семенную камеру, наименьшую плотность кожицы и наиболее благоприятное содержание воздуха. Остальные сорта огурцов по совокупности физических показателей стоят ниже их, особенно неросимые, вязниковские и берлизовские.
На качество готовой продукции оказывает влияние и поверхность плодов огурцов. Огурцы бугорчатые и бороздчатые в этом отношении считаются лучшими. Это объясняется тем, что при наличии бороздчатости и бугорчатости отношение поверхности плодов к их объему значительно больше, чем при гладкой поверхности. Следовательно, на единицу массы мякоти огурцов с бугорчатой поверхностью приходится большая площадь этой поверхности, что облегчает процесс двусторонней диффузии во время ферментации. Кроме того, поверхность таких огурцов даже при плотной укладке в бочки обеспечивает лучшее обтекание их рассолом, чем огурцов гладких. Это улучшает условия ферментации.
Неоспоримым является факт, что из свежих огурцов мелких размеров получаются соленые огурцы более высокого качества, чем из огурцов крупных. Мелкие огурцы характеризуются большей поверхностью, приходящейся на единицу их объема, по сравнению с крупными. Если отношение поверхности плодов (в см2) к их объему (в см3) назвать удельной поверхностью (S/V) (поверхность, отнесенная к единице массы вещества), то, как показывают наши расчеты для огурцов сорта нежинские, приведенные в табл. 10, у мелких корнишонов, длиной 5 см, удельная поверхность почти втрое больше, чем у крупных огурцов, длиной 14 см.
Очевидно, этот фактор является одним из решающих в формировании качества готовой соленой продукции, так как большая удельная поверхность малых по размеру огурцов обеспечивает более быструю диффузию и, следовательно, их лучшую ферментацию.
| {22} |
|
ТАБЛИЦА 10
| ||||||||||||||||||||||||||
По существующему стандарту соленые огурцы высшего сорта должны быть длиной не более 90 мм. Огурцы такой длины имеют удельную поверхность 1,34 см2. В соленых огурцах первого сорта допускаются плоды длиной до 120 мм и во втором сорте — до 140 мм. Удельная поверхность огурцов таких размеров, соответственно, будет равна 1,0 и 0,86 см2.
Колебания размеров удельной поверхности огурцов одной и той же длины, но разных хозяйственно-ботанических сортов, как это следует из данных табл. И, невелики и решающего значения при засолке не имеют. Однако уменьшение удельной поверхности в совокупности с другими факторами ухудшает засолочные качества огурцов.
Чтобы получить сравнимые данные об удельной поверхности по разным хозяйственно-ботаническим сортам огурцов, мы в табл. 11 привели их длину к одной длине, которая характерна для более мелких муромских огурцов, сохранив во всех случаях свойственный сорту индекс формы.
|
ТАБЛИЦА 11
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Наибольшую удельную поверхность имеют огурцы борщаговские, рябчик, крымские и нежинские и наименьшую — муромские, чернобривец и неросимые. {23}
Физические свойства огурцов одного и того же сорта изменяются при выращивании их в разных областях. Из этого следует сделать вывод, что и технологические качества огурцов зависят от почвенных и климатических условий.
Изменение качественных показателей огурцов, выращенных в различных климатических зонах, в значительной мере обусловило разные мнения многих авторов о пригодности к засолке одних и тех же сортов огурцов.
Для определения технологической пригодности огурцов к засолке, независимо от принадлежности их к тому или иному сорту, необходимо установить объективные показатели.
При таком решении вопроса в каждой почвенно-климатической зоне можно найти, как оно и наблюдается в действительности, ряд сортов, пригодных по своим объективным показателям для засолки в данной местности.
На основании приведенных выше данных можно сказать, что степень пригодности огурцов для соления определяют такие показатели: содержание сахара, коллоидных веществ (азотистых и пектина), воздуха в объемных процентах, объем семенной камеры, удельная поверхность плодов, характер этой поверхности, размер плодов и их удельный вес.
Глава пятая
Физические свойства свежих огурцов и их химический состав в процессе ферментации подвергаются глубоким изменениям. Изменяются объем и абсолютный вес огурцов, содержание воздуха в тканях плодов; сбраживаются сахара, вместо которых появляются молочная кислота и некоторое количество спирта и других побочных продуктов основного молочнокислого брожения;, уменьшается содержание азотистых, минеральных веществ и витамина С; появляется соль; изменяется консистенция ткани и т. д.
В результате всех физико-химических изменений, происходящих под влиянием сложного процесса ферментации, соленые огурцы приобретают свойственный им вкус, совершенно отличный от вкуса свежих.
Для более точного выяснения сущности некоторых явлений и факторов, их обусловливающих, мы рассмотрим отдельно изменения физических свойств огурцов.
Для технологии очень важно установить, в какой последовательности и с какой быстротой проходят процессы выделения из клеточной ткани огурцов сока в рассол и проникновения из рассола в плодовую ткань соли, а также, какие изменения эти {24} процессы вызывают в плодах огурцов. С целью изучения течения этих процессов одним из авторов данной книги были поставлены лабораторные опыты, краткое описание которых считаем необходимым привести.
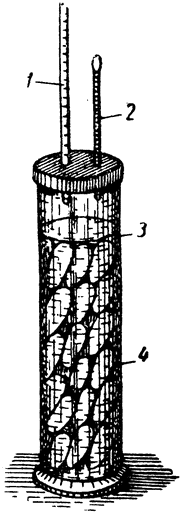
Огурцы укладывали в двухлитровые стеклянные цилиндры одинаковой формы и засаливали обычным путем. Каждый цилиндр герметически закрывали пробкой с двумя отверстиями. Через эти отверстия внутрь цилиндра были опущены бюретка на 50 см3 и термометр (рис. 1).
Огурцы в цилиндре заливали точно измеренным количеством рассола, крепостью в 8%, который полностью заполнял цилиндр и частично бюретку.
Во избежание испарения влаги из рассола отверстие в верхнем конце бюретки было герметически закрыто резиновой пробкой. Для удаления газов, образующихся в процессе брожения, верхний конец бюретки ежедневно открывали на несколько секунд.
 |
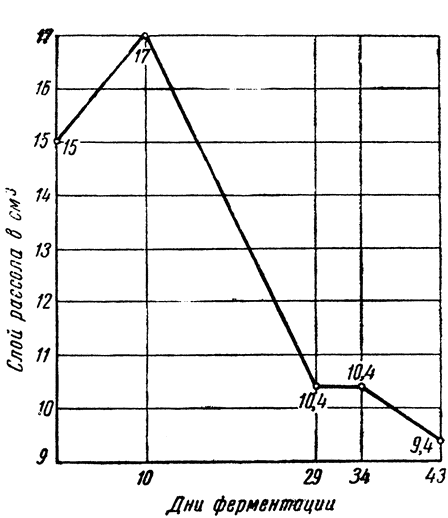 |
Рис. 1. Цилиндр для исследования размера потерь огурцами клеточного сока: 1 — бюретка; 2 — термометр, 3 — груз; 4 — цилиндр |
Рис. 2. Высота слоя в бюретке |
Опыт проводился при средней температуре в 18–20°.
По уровню рассола в бюретке учитывались изменения общего объема (огурцы + рассол). Эти изменения показаны на рис. 2.
Повышение уровня жидкости в бюретке продолжалось 10 дней, достигнув максимального уровня в 17,0 см3 (против первоначального уровня в 15 см3). {25}
К указанному сроку общий объем увеличился на 2 см3, что составляет к количеству влитого рассола 0,7%.
Начиная с 11-го дня слой жидкости стал уменьшаться и через 29 дней после засола огурцов достиг 10,4 см3, оставаясь на этом уровне в течение нескольких дней. В дальнейшем уровень рассола в бюретке снижался незначительно и спустя 43 дня с момента засола достиг минимального уровня в 9,4 см3. Ниже указанного уровня слой рассола в бюретке не опускался.
Полученные данные дали возможность судить только об изменении общего объема и установить периодичность этих изменений.
Чтобы определить причины изменения общего объема и физических свойств огурцов в периоды наибольшего увеличения объема жидкости в сосуде, в период стабилизации уровня жидкости и наибольшего его снижения, исследовались изменения веса, объема и удельного веса огурцов, содержание воздуха в их тканях, изменение количества рассола в других параллельных цилиндрах.
Установленное опытами увеличение общего объема всей массы в первые 10 дней могло произойти только в случае выделения сока из плодов в рассол, превышающего уменьшение их объема. Таким образом, основным процессом, который происходит в первые дни брожения, является осмос сока из огурцов в рассол.
Если в этот период и происходит диффузия соли из рассола в огурцы, то это явление вторичное и настолько замедленное, что не компенсирует основного процесса — осмоса сока. Это явление отмечено и рядом других авторов.
Приведенные лабораторные исследования дают возможность изучить физические изменения огурцов в процессе всего периода ферментации.
В табл. 12 данные изменений физических свойств огурцов в разные сроки ферментации перечислены для удобства рассмотрения на 1000 г огурцов.
Как показали исследования, интенсивное выделение сока из огурцов в первые 10 дней привело к уменьшению их объема на 61,4 см3 и увеличению воздуха в тканях плодов на 9,8 см3. Внешне эти явления проявились в увеличении объема рассола на 73 см3 и уменьшении веса огурцов на 72 г.
Во втором периоде брожения, продолжавшемся 19 дней, диффузия рассола в плодовую ткань стала настолько интенсивной, что затушевала происходящее еще выделение сока. В результате такой усиленной диффузии плоды впитали 47 см3 рассола, который, заполняя ткань, вытеснил 32,2 см3 воздуха и привел к увеличению объема плодов на 13,3 см3. Вес огурцов при этом увеличился на 61 г. Увеличение веса огурцов несколько превышает объем поглощенного рассола, так как вместе с рассолом в плодовую ткань проникает соль, которой к этому периоду в огурцах накапливается, как показывают химические анализы, около 95% ее окончательного содержания в соленых огурцах. Проникновение
| {26} |
|
ТАБЛИЦА 12
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
соли в огурцы приводит к уплотнению ткани и увеличению их удельного веса.
В третьем периоде, который в опытах продолжался 14 дней, брожение почти прекратилось, вследствие чего приостановилось накопление молочной кислоты и стабилизовалось ее содержание. Однако диффузия продолжалась, хотя и замедленными темпами. Количество рассола уменьшилось еще на 12 см3 за счет впитывания его плодами. Проникший в плоды рассол вытеснил еще 5,8 см3 воздуха из ткани и привел к дальнейшему увеличению объема огурцов на 5,1 см3. В результате этих изменений увеличился вес огурцов еще на 12 г, превысив на 1 г вес свежих огурцов.
Итоговые результаты за 43 дня ферментации и хранения огурцов таковы. Объем рассола увеличился на 14 см3 или на 1,4% к первоначальному. Следовательно, столько же сока потеряли огурцы, вследствие чего они так и не восстановили первоначального объема, который уменьшился на 43 см3, или на 4,2%. Уменьшение объема произошло за счет уплотнения ткани огурцов, в которой осталось 14,7 см3 воздуха вместо первоначальных 42,9 см3 в свежих плодах. Всего вытеснено из плодовой ткани 28,2 см3 воздуха, что составляет 2,7% их первоначального объема.
Несмотря на объемную потерю сока и связанное с этим уменьшение объема плодов, их вес не только не уменьшился, но даже {27} несколько увеличился против первоначального — на 0,1%. Это и понятно, так как вес проникшей в огурцы соли превысил потерю ими сухих веществ, ушедших с соком в рассол.
Для более полной характеристики совершающихся при ферментации огурцов физических явлений необходимо рассмотреть процесс диффузии соли из рассола в ткань огурцов.
В производственных условиях были засолены огурцы сорта
ТАБЛИЦА 13
|
Быстрота проникновения соли в огурцы и окончательное ее содержание показаны в табл. 13. Как видно из приведенных данных, уже через 2 дня количество накопившейся в огурцах соли составило 43,8% ее окончательного содержания. Диффузия соли в огурцы продолжалась до тех пор,
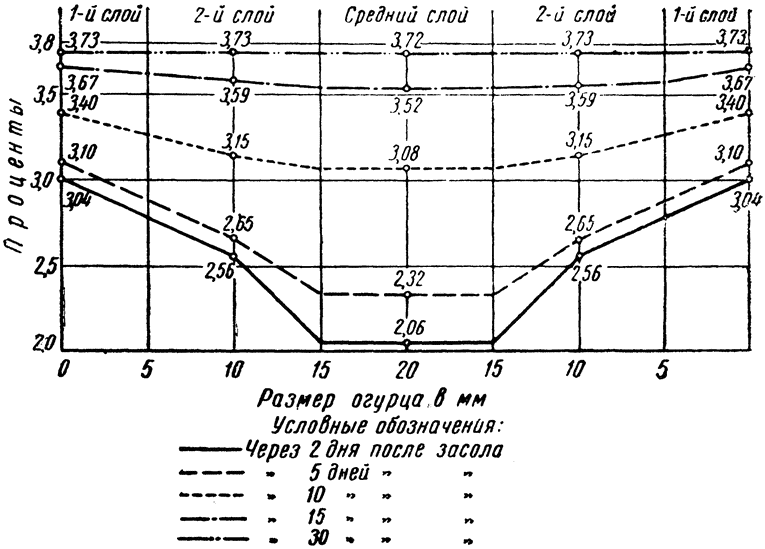 |
Рис. 3. Диаграмма диффузии соли в ткань огурца |
| {28} |
пока не установилось равновесие в содержании ее в огурцах и рассоле. Это равновесие в содержании соли в огурцах и рассоле при указанных условиях хранения было достигнуто на 25-й день. К этому сроку в огурцах накопилось 3,72% соли. На 30-й день содержание соли в огурцах еще немного увеличилось, достигнув 3,79%.
Накопленное количество соли вполне компенсирует незначительную потерю огурцами сока и в известных условиях может привести к абсолютному увеличению веса соленых огурцов по сравнению со свежими.
Соль проникает в толщу мякоти огурцов постепенно, как показано на рис. 3, и с различной скоростью в разных слоях плодов.
Только к концу ферментации, в данном случае на 30-й день, соль в огурцах распределяется равномерно по всей их толще. К этому времени вся плодовая мякоть приобретает одинаковые вкусовые достоинства, что вместе с остальными показателями определяет готовность огурцов к потреблению.
Издавна установилось мнение, что соление огурцов сопровождается уменьшением их веса.
Известные нам экспериментальные работы и литературные источники по этому вопросу (в основном инструктивного и учебного характера) не вскрывают причин, вызывающих потери в весе огурцов при ферментации и хранении, причем у различных авторов имеются совершенно противоречивые показатели. Одни авторы естественную убыль в весе соленых огурцов определяют в пределах 0–4%, другие в 6,3–9,4 и даже 25–30%.
Предполагают, что огурцы больше отдают влаги, чем поглощают рассола, а также теряют часть сухих веществ.
Теоретически можно прийти к предположению, что в огурцах при ферментации и хранении, при условии сохранения первоначального объема, не должно происходить убыли в весе. Наоборот, следует ожидать прибавления веса.
В мякоти огурцов в зависимости от их сорта содержится воздуха от 4 до 9% к объему плода. Физико-химические и гистологические исследования показывают, что проникающий в клетки огурца рассол замещает вытесненный им воздух.
Следовательно, вес огурцов может увеличиться вследствие уплотнения плодовой ткани и в результате увеличения содержания сухих веществ за счет соли.
Такое предположение подтверждается анализом удельного веса свежих и соленых огурцов.
Удельный вес свежих огурцов меньше воды и равняется в среднем 0,95–0,98. Это значит, что вес плода в граммах всегда меньше его объема в кубических сантиметрах. Вместе с тем известно, что минимальный удельный вес соленых огурцов больше единицы и равен 1,01–1,02. {29}
Таким образом, если огурцы не изменили своего первоначального объема, простой расчет приводит к выводу, что они должны прибавить в весе 4,1%. В самом деле, если свежий огурец объемом в 100 см3 при удельном весе 0,98 весит 98 г, то этот же огурец, но соленый, при удельном весе 1,02 (при неизменном объеме) весит уже 102 г; таким образом, он прибавил в весе 4 г, т. е. увеличил его на 4,1%.
Из этих теоретических предпосылок следует вывод, что весовые потери при ферментации огурцов в практике соления не являются неизбежными и если они имеются, то это вызвано уменьшением объема огурцов либо образованием пустот внутри плодов.
Для проверки результатов лабораторных исследований, приведенных в табл. 12, были поставлены производственные опыты. Были засолены огурцы сорта нежинские размером 91–120 мм в 18-литровых дубовых бочонках, которые хранились при средней температуре 10–12°.
Через 4, 10, 15, 20, 30 и 40 дней вскрывали по два бочонка для изучения изменений объема, веса огурцов, удельного веса и содержания воздуха в плодовой ткали.
В табл. 14 приведены данные этого изучения.
|
ТАБЛИЦА 14
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Данные таблицы подтверждают лабораторные исследования и теоретические соображения.
Ферментация была закончена на 30-й день. На 40-й — огурцы находились уже на хранении. Какие изменения произошли в огурцах к концу наблюдений?
Объем плодов огурцов уменьшился на 3,64%, а вес увеличился на 1,32% вследствие того, что удельный вес их возрос с 0,972 до 1,022, т. е. на 5,14%. Увеличение удельного веса огурцов вызвано проникновением соли в ткани плодов и уплотнением ее за счет замещения воздуха рассолом. Содержание воздуха в огурцах снизилось с 4,94 до 0,59%, т. е. воздуха в огурцах осталось всего 12,05% от первоначального содержания.
Так как в производственной практике чаще всего наблюдается уменьшение веса огурцов, а не увеличение, что, очевидно, связана {30} со значительно большим уменьшением их объема, чем это наблюдалось в приведенных опытах, необходимо рассмотреть факторы, которые влияют на величину изменения объема и, следовательно, веса.
Глава шестая
Объемные и весовые изменения огурцов вызываются явлениями диффузии и осмоса. Уменьшение объема и веса зависит от интенсивности осмоса и определяется количеством выделенного сока и, наоборот, диффузия рассола в ткани огурцов приводит к увеличению их веса и восстановлению объема. Конечные результаты изменений будут зависеть от некоторых факторов вторичного порядка, обусловливающих интенсивность и пределы диффузии и осмоса. К этим факторам относятся: содержание гидрофильных коллоидов в огурцах, сила давления, испытываемого огурцами в таре разной емкости, крепость рассола.
Естественно предположить, что наличие в тканях плодов огурцов азотистых, пектиновых веществ и других коллоидов будет оказывать влияние на процессы осмоса и диффузии. Вследствие своей гидрофильности и способности удерживать часть воды в связанном состоянии коллоиды должны задерживать и ограничивать отдачу плодовой тканью сока в рассол. Гидрофилыюсть коллоидов тем больше будет сказываться, чем больше в огурцах самих коллоидов, чем сильнее их водосвязывающая способность и сопротивляемость воздействию химических реагентов, особенно (что нас в данном случае интересует) воздействию соли и кислот.
Академик С. П. Костычев указывает, что протоплазма растительных объектов в большей своей части состоит из гидрофильных коллоидов и что этот тип коллоидов легко коагулирует при добавлении водоотнимающих веществ, в частности солей. Такую же мысль высказывает и академик А. В. Думанский, добавляя, что коагуляция коллоидов вызывает изменение количества связанной воды.
По мнению многих исследователей, коагуляция коллоидов протоплазмой растительной ткани приводит к потере ею механической прочности, способности удерживать воду и изменению эластичности.
М. Е. Мельман в своих исследованиях нашел такую зависимость между содержанием азотистых веществ в огурцах разной степени зрелости, их способностью удерживать воду и изменением объема при солении (см. табл. 15).
| {31} |
ТАБЛИЦА 15
Размеры огурцов (в мм) (сорт нежинские) |
Содержание азотистых веществ (в %) на сырой вес |
Количество связанной воды в свежих огурцах (в %) |
Потеря связанной воды в соленых огурцах (в % к содержанию ее в свежих) |
Уменьшение объема соленых огурцов (в % к первоначальному объему) |
||||
Зеленые |
от |
50 |
до |
70 |
1,76 |
31,6 |
72,4 |
2,6 |
„ |
„ |
71 |
„ |
90 |
1,86 |
32,6 |
75,2 |
3,1 |
„ |
„ |
91 |
„ |
120 |
1,13 |
21,1 |
78,8 |
5,8 |
„ |
„ |
121 |
„ |
140 |
0,97 |
20,2 |
79,7 |
6,2 |
Желтяки |
„ |
91 |
„ |
140 |
0,94 |
19,6 |
92,0 |
18,0 |
Прямая зависимость установлена между содержанием азотистых веществ и количеством связанной воды. Вполне определенной можно считать и зависимость между потерей связанной воды, которая вызывается денатурацией белков, и первоначальным объемом. Как видно из данных таблицы, меньше всего потеряли связанной воды и лучше сохранили свой объем корнишоны (50–70 мм). Желтяки (91–140 мм) потеряли связанную воду и уменьшили свой объем в наибольшей степени.
Эта связь между двумя рядами цифр указывает на причинную зависимость. Чем больше было потеряно связанной воды, тем, следовательно, полнее коагулировали белки и тем большую способность к изменению объема приобрели огурцы.
Однако утрата водоудерживающей способности ткани вследствие коагуляции белков не всегда и не обязательно вызывает соответствующее ей изменение объема. Коагуляция является лишь предпосылкой, могущей вызвать резкое изменение объема при наличии других факторов и, в частности, внешнего давления.
Из приведенных данных можно сделать практически ценный вывод: зеленые огурцы мелких размеров (до 100 мм), более богатые азотистыми веществами по сравнению с огурцами более крупными и зрелыми, меньше изменяют свой объем. Чем крупнее огурцы, тем они беднее азотистыми веществами и тем более они способны к изменению объема.
Следует отметить еще влияние коллоидов и в первую очередь азотистых веществ на сохранение структуры плодовой ткани соленых огурцов. Чем мельче огурцы и чем больше в них азотистых веществ, тем лучше сохраняется структура их ткани при солении. И наоборот, в бедных азотистыми веществами и более зрелых огурцах ткань при солении становится дряблой, расползающейся.
Независимо от содержания азотистых веществ, степени их коагуляции в процессе соления и потери ими водопоглощающей способности, на изменение объема и веса огурцов оказывает влияние {32} также и ряд других факторов и в первую очередь сила давления, испытываемого огурцами в таре разной емкости.
Огурцы одного и того же хозяйственно-ботанического сорта, одинакового размера и качества, при посоле в таре разной емкости неодинаково изменяют свой вес.
Для проверки этого явления на Корчаковском засолочном заводе в 1938 г. были поставлены производственные опыты. Были засолены огурцы сорта нежинские размеров 91–100 мм одинакового качества. Засолка произведена в бочках емкостью 16, 40, 60, 100, 125, 150 и 200 л, которые были залиты 8%-ным раствором соли. После выдержки на ферментационной площадке бочки с огурцами были помещены в ледник. По истечении 60 дней (после окончания ферментации) и каждый последующий месяц хранения проверялось изменение веса огурцов.
В табл. 16 приводим изменение веса огурцов в бочках разной емкости по окончании ферментации (60 дней) и через 7 месяцев со дня посола.
|
ТАБЛИЦА 16
| ||||||||||||||||||||||||||||||||||
Эта производственная проверка подтвердила, что вес огурцов в таре разной емкости в процессе соления меняется неодинаково. На величину уменьшения веса оказывает влияние сила давления в таре крупной емкости. При незначительном давлении, которое огурцы испытывают в мелкой таре (16 и 40 л) происходит даже увеличение веса.
Для более глубокого изучения этого явления в лаборатории были поставлены специальные опыты, в которых засоленные огурцы находились под разным давлением. При этом исследовались изменения объема, содержания воздуха, удельного веса плодов в связи с изменением ими абсолютного веса.
В восьми цилиндрах диаметром 4 см, но разной высоты, были засолены огурцы сорта нежинские размером 91–100 мм и залиты рассолом крепостью 8%. Удельный вес свежих огурцов был 0,994. Огурцы находились в цилиндрах в вертикальном положении: в цилиндре № 1 — один огурец, в цилиндре № 2 — два, в № 3 — три и т. д. В последнем, 8-м, цилиндре было 8 огурцов, расположенных один над другим. Засоленные огурцы хранились при средней температуре 12° до окончания ферментации. {33}
Исследование засоленных огурцов было произведено через 40 дней по окончании ферментации.
В табл. 17 приводятся данные о физических изменениях в огурцах под влиянием разного давления.
|
ТАБЛИЦА 17
| |||||||||||||||||||||||||||||||||||||||||||||||||
Следует отметить, что чем больше огурцы испытывали давление в цилиндрах, тем значительнее они уменьшили свой объем, причем уменьшение объема происходило параллельно уменьшению веса. Однако абсолютный вес огурцов в цилиндрах с одним, двумя, тремя и четырьмя огурцами (следовательно, с одним, двумя, тремя, четырьмя слоями огурцов) не уменьшился, а увеличился. Наибольший вес, как и наибольший объем, сохранили огурцы, находившиеся под наименьшим давлением.
Сила давления также сказалась на замещении воздуха рассолом в огуречной ткани. Лучше всего (на 95%) замещен воздух в огурцах цилиндра № 1, т. е. в том цилиндре, где никакого, в сущности, давления не было. По мере увеличения давления количество замещенного рассолом воздуха уменьшается, и в 8-м цилиндре в огурцах воздух замещен в среднем только на 44,8%. Это отразилось на удельном весе огурцов: чем менее полно замещен воздух рассолом, тем меньше удельный вес плодов.
Неполное замещение воздуха рассолом при большом давлении объясняется тем, что процесс осмоса сока из огурцов в первые дни брожения доминирует над процессом диффузии. При отдаче сока в рассол под влиянием внешнего давления происходит сжатие плодов и тем большее, чем больше давление. Так как давление является фактором постоянно действующим и неизменным, то сжавшийся плод не в состоянии восстановить своего объема. Вот этим ограничивается диффузия рассола в плоды и замещение воздуха в тканях.
В огурцах под давлением разной силы происходят не только весовые изменения, но и качественные. Огурцы, не потерявшие веса, обладают хорошо пропитанной рассолом плотной мякотью, сохраняют свою упругость и имеют лучшие вкусовые качества. Наоборот, чем больше огурцы потеряли веса, следовательно объема, {34} чем менее полно замещен воздух в тканях, тем мякоть плодов рыхлее, тем менее она пропитана рассолом и менее упруга. При большом давлении (в 200–300-литровых бочках) часть плодов теряет не только объем, но и форму — расплющивается.
В связи с рассмотренным выше вопросом о влиянии силы давления на физические свойства огурцов практически и теоретически полезным будет установить, влияют ли содержание азотистых веществ и связанная с их наличием в огурцах водоудерживающая способность плодов на сопротивление внешнему давлению и как сказывается это влияние.
Косвенный, но довольно верный ответ на этот вопрос мы находим в массовых производственных опытах.
По средним данным трехлетних наших исследований, результаты которых приводятся в табл. 18, установлены следующие весовые потери (в процентах) огурцов разных размеров в таре разной емкости.
|
ТАБЛИЦА 18
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Анализируя данные табл. 18, можно сделать вывод, что сила давления, испытываемая огурцами в таре, больше всего сказывается на огурцах с наименьшим содержанием азотистых веществ, т. е. на крупных огурцах, хранящихся в неохлаждаемых складах.
Интересно отметить, что огурцы, засоленные в дошниках, следовательно под большим давлением, и значительно потерявшие свой объем, после выгрузки из дошников способны частично восстанавливать свой объем и вес. Огурцы, засоленные в дошниках глубиной 2–2,5 м и потерявшие в весе 14%, после расфасовки их в бочки 125-литровой емкости восстанавливали свой вес в течение 40 дней. Через 10 дней восстанавливалось 3,8% потерянного веса, через 20 — 6,2%, через 30 — 6,7% и через 40 дней — 6,9%.
Чтобы выяснить, за счет чего происходит восстановление объема, часть выгруженных из дошника огурцов была расфасована в стеклянные банки и перенесена в лабораторию для изучения. Средняя температура хранения огурцов в лаборатории была 18°.
Как показало исследование, в условиях лаборатории вес огурцов стабилизировался на 19-й день. К этому времени вес увеличился на 9,53%, причем объем увеличился на 5,05% и содержание воздуха в тканях уменьшилось на 3,8 объемного процента.
Таким образом, восстановление веса огурцов произошло за счет частичного замещения воздуха в тканях и увеличения их объема.
| {35} |
Для изучения влияния крепости рассола на физические свойства огурцов огурцы сорта нежинские среднего размера (91–120 мм) были засолены в 3-килограммовых банках и залиты рассолами с содержанием соли в 5, 6, 7, 8, 12 и 15%. Ферментация огурцов проходила в подвале лаборатории при температуре 14–18°. Через 30 дней, по окончании ферментации, огурцы были исследованы на изменение веса, объема и удельного веса плодов.
Результаты происшедших изменений изображены на рис. 4.
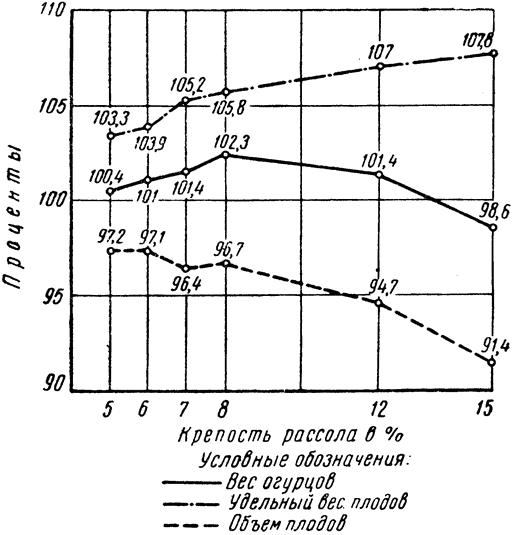 |
Рис. 4. Влияние крепости рассола на изменение физических свойств огурцов в процессе ферментации |
Изменения объема, удельного и абсолютного веса соленых огурцов показаны в процентах к объему, удельному и абсолютному весу свежих огурцов до закладки их в банки.
Влияние крепости рассола на изменение этих физических свойств огурцов видно из направления соответствующих кривых.
С повышением крепости рассола кривая удельного веса соленых огурцов непрерывно поднимается. В то же время кривая объема с небольшими зигзагами опускается вниз. Как показывает кривая веса, изменения его являются, в сущности, функцией изменений удельного веса и объема. До 8% концентрации рассола абсолютный вес огурцов возрастает, а в дальнейшем падает, снижаясь, однако, ниже веса свежих только в 15%-ном рассоле. {36}
Таким образом, наибольшее увеличение веса произошло в огурцах, залитых 8%-ным рассолом. Увеличение обсолютного веса с повышением концентрации рассола до 8% происходило потому, что удельный вес плодов возрастал в большей степени, чем уменьшался их объем. С повышением концентрации соли свыше 8% уменьшение объема огурцов оказалось настолько резким, что продолжающееся повышение удельного веса не в состоянии компенсировать потерю абсолютного веса, который постепенно снижается. С повышением концентрации соли свыше 8% происходит сильное обезвоживание плодов и, очевидно, наиболее полная коагуляция коллоидов, приводящая к тому, что плодовая ткань в значительной мере утрачивает способность удерживать влагу.
Интересен вопрос, почему повышение концентраций соли до 8% сказывается благоприятно на изменении абсолютного веса? Если рассматривать это явление с точки зрения влияния концентрации соли на коагуляцию коллоидов, то следовало бы ожидать, что наиболее эффективным окажется 5%-ный рассол, а не 8%-ный.
Дальнейшие исследования показали, что в соленых огурцах с 5%-ным рассолом воздух в плодовой ткани замещен рассолом на 47,5%, а в огурцах, залитых 8% -ным рассолом,— на 95,8%, т. е. значительно полнее. Это обстоятельство и привело к большему увеличению абсолютного веса огурцов в 8%-ном рассоле по сравнению с огурцами, залитыми 5%-ным рассолом.
Более глубоко это явление еще не изучено. Возможно, здесь сказалось влияние микробиологических процессов, течение которых с повышением концентрации соли проходит более замедленными темпами. Вследствие этого количество выделяющихся при брожении газов с увеличением концентрации соли уменьшается в единицу времени и, следовательно, ослабляется разрушающее их действие на плодовую ткань.
Некоторым подтверждением этого является качественное состояние соленых огурцов. Наиболее плотная ткань, хорошо пропитанная рассолом, наилучшая консистенция и вкус оказались у огурцов, залитых 8%-ным рассолом. Плоды огурцов в 5%-ном рассоле — с рыхловатой тканью, слабой консистенцией и пониженных вкусовых качеств. Здесь сказался результат накопления побочных продуктов молочнокислого брожения. Наименьшей эластичностью обладали огурцы, засоленные в крепких рассолах (12 и 15% концентрации); в них ткань суховатая, обезвоженная, поверхность морщинистая, плоды с несколько измененной формой, вследствие значительного уменьшения объема, вкус излишне соленый.
Рассмотрение материалов этих исследований приводит к выводу, что наиболее эффективными являются рассолы 6–8% концентрации, так как при этой концентрации незначительное сокращение объема огурцов перекрывается интенсивным проникновением рассола в плодовую ткань и почти полным вытеснением из нее воздуха. Это приводит не только к сохранению, но даже к некоторому {37} увеличению первоначального веса огурцов при отсутствии значительного внешнего давления.
Указанные концентрации соли дают возможность более чисто вести процесс молочнокислой ферментации и накапливать сравнительно быстро необходимое для консервирования количество молочной кислоты.
ВЫВОДЫ
Анализируя физические изменения, происходящие в огурцах при ферментации, и факторы, обусловливающие их, следует сделать такие общие выводы.
1. Вопреки установившемуся мнению, процесс ферментации сам по себе не сопровождается весовыми потерями огурцов. В результате ферментации может произойти и прибавление в весе.
2. Весовые изменения в огурцах определяются двумя противоположно направленными явлениями — уменьшением объема плодов вследствие отдачи сока в рассол и увеличением их удельного веса в результате вытеснения рассолом воздуха из плодовой ткани с одновременным повышением содержания сухих веществ за счет соли. В зависимости от преобладания того или другого явления происходит увеличение или уменьшение веса огурцов при солении.
3. Оба эти явления в свою очередь обусловлены качеством сырья (в частности, содержанием коллоидных веществ и воздуха) и условиями, в которых проходит ферментация. Следовательно, весовые изменения огурцов при солении зависят от регулирования указанных факторов.
4. Степень уменьшения объема огурцов зависит от содержания коллоидных веществ и воздуха в плодовой ткани, от силы давления, испытываемого огурцами в таре разной емкости и концентрации соли в рассоле. Чем больше азотистых веществ в огурцах и чем меньше давление (т. е. чем меньше тара), тем меньше изменяется объем огурцов. К тому же результату приводит содержание воздуха в огурцах в пределах 4–6 объемных процентов и применение рассолов крепостью 6–8%.
5. При засолке зеленых огурцов нормальных размеров (50–120 мм) в таре до 40-литровой емкости или мелких огурцов (до 50 мм) в таре емкостью до 125 л можно избежать весовых потерь, так как в этих условиях потеря веса за счет уменьшения объема, как правило, перекрывается увеличением абсолютного веса вследствие значительного повышения удельного веса плодов.
6. С увеличением емкости тары свыше 40 л и размеров огурцов свыше 50 мм при засолке огурцов происходит уменьшение их абсолютного веса. Это уменьшение веса тем значительнее, чем больше емкость тары и крупнее огурцы.
7. Проведение ферментации при низких температурах (в ледниках) способствует уменьшению потерь, так как процесс ферментации {38} (в частности, процесс осмоса) проходит замедленными темпами, вследствие чего менее значительно уменьшается объем огурцов.
8. Чем лучше сохраняется первоначальный объем и вес огурцов, тем выше их качество в соленом виде, и наоборот.
Глава седьмая
По химическому составу соленые огурцы довольно резко отличаются от свежих. Сахар свежих огурцов в соленых заменяется кислотой, уменьшается содержание азотистых, минеральных веществ и витаминов, появляется новое вещество — поваренная соль, накапливаются различные эфирные масла (от вводимых специй), образуются сложные эфиры.
Все это приводит к резкому изменению вкуса, запаха и консистенции огурцов, их абсолютного и удельного веса.
Для характеристики этих изменений приводим химический состав нежинских огурцов первого сорта, размером 91–120 мм, свежих и засоленных в 8%-ном рассоле (табл. 19).
|
ТАБЛИЦА 19
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Сравнение химического состава свежих и соленых огурцов не дает еще представления о превращениях отдельных веществ в самом процессе ферментации. Между тем учет химических изменений совершенно необходим для выяснения сущности процесса ферментации и правильного его ведения.
Изучение химических превращений в огурцах производилось в лабораторных условиях. Огурцы были засолены в 3-килограммовых {39} банках и залиты 8%-ным рассолом. Процесс ферментации проводился в подвале с температурой 10–12° после предварительной выдержки в течение первых двух дней при температуре 18–20°. Через 2, 5, 10, 15, 20, 30 и 40 дней производился химический анализ огурцов, сопровождавшийся изучением изменений их абсолютного веса.
Общее направление количественных изменений влаги в огурцах при ферментации намечено при рассмотрении процессов осмоса и диффузии. Химический анализ показывает постепенное снижение содержания влаги с 95,05 до 93,85% и постепенное повышение содержания сухих веществ с 4,95 до 6,15%. Однако вследствие того, что при ферментации изменяется и абсолютный вес огурцов, процентное содержание в них влаги и сухих веществ не отражает фактического движения этих элементов. Чтобы получить представление об этом, мы рассчитали содержание влаги и сухих веществ, в абсолютных количествах с учетом изменившегося веса огурцов. Расчет сделан на 100 кг свежих огурцов. Этот вес в процессе ферментации через 2, 5, 10, 15, 20, 30 и 40 дней изменялся таким образом: 98,2; 95,03; 95,8; 97,7; 99,3; 100,1 и 100,9 кг. Рассчитывая процентное содержание влаги и сухих веществ к этому изменившемуся весу, мы получили истинный характер движения этих элементов, который отражен в кривых на рис. 5.
Кривая влаги показывает резкое снижение ее содержания на 5,48 кг в течение первых пяти дней ферментации, затем небольшое повышение в последующие пять дней на 0,45 кг и постепенное увеличение к концу ферментации до 94,69 кг, что несколько меньше первоначального ее содержания в свежих огурцах (95,05 кг). Эти изменения в содержании влаги точно отражают течение рассмотренных уже нами процессов осмоса и диффузии. Вначале происходит осмос сока в рассол, по истечении пяти дней начинает преобладать диффузия рассола в огурцы, а через десять дней она становится уже основным процессом.
Содержание сухих веществ в огурцах, несмотря на отдачу ими сахара в рассол, возрастает в первые же два дня на 0,43 кг, т. е. больше чем во все последующие периоды, и в дальнейшем повышается до 6,21 кг, значительно превышая первоначальное их количество — 4,95 кг. Изменение веса и содержания влаги показывает, что с самого начала ферментации преобладает процесс осмоса.
В результате большой отдачи сока в рассол огурцы значительно теряют свой вес в течение первых пяти дней, так как увеличение содержания сухих веществ не в состоянии компенсировать потери влаги. В дальнейшем ходе ферментативного процесса, когда преобладает диффузия рассола в огурцы и в них постепенно возрастает количество влаги и сухих веществ,
| {40} |
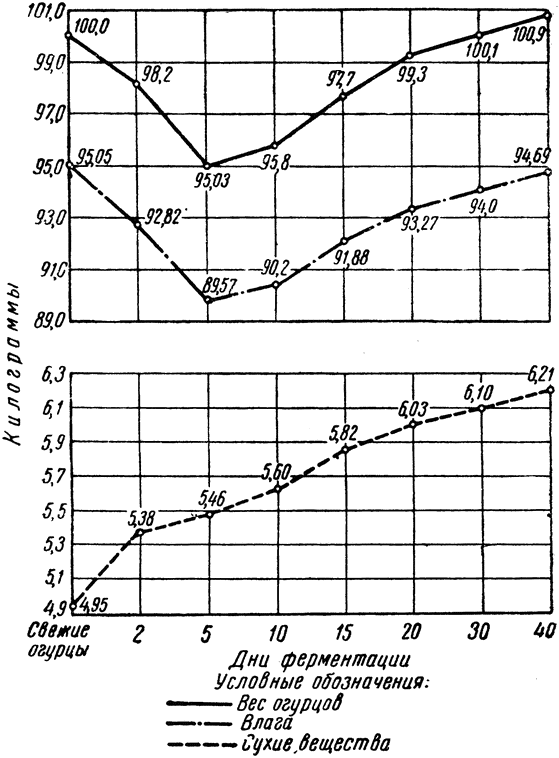 |
Рис. 5. Изменение веса 100 кг свежих огурцов и содержание в них влаги и сухих веществ |
абсолютный вес огурцов увеличивается, достигая 100,9 кг, что на 0,9 кг больше веса свежих.
В иных условиях ферментации, при более низких температурах, рассмотренные нами количественные изменения влаги и сухих веществ во времени будут происходить более замедленно, но общая тенденция остается неизменной.
Динамика общего количества сухих веществ в огурцах в процессе ферментации не отражает изменений основных сухих веществ, характерных для свежих огурцов, так как диффузия соли в плодовую ткань затушевывает их. Поэтому необходимо выделить соль из общего состава сухих веществ.
В табл. 20 приводятся расчеты, где процентное содержание сухих веществ пересчитывается на абсолютное количество, причем учитывается изменяющийся вес 100 кг свежих огурцов при ферментации.
| {41} |
ТАБЛИЦА 20
Периоды ферментации |
Изменение |
Общее количество сухих веществ (в кг) |
Количество соли в огурцах (в кг) |
Содержание сухих веществ в огурцах без соли |
|||||
в кг |
в % |
||||||||
Свежие огурцы . . . . |
100 |
4,95 |
0 |
4,95 |
4,95 |
||||
Через |
2 |
дня |
после |
засола |
98,2 |
5,38 |
1,57 |
3,81 |
3,88 |
„ |
5 |
дней |
„ |
„ |
95,03 |
5,46 |
2,51 |
2,95 |
3,10 |
„ |
10 |
„ |
„ |
„ |
95,8 |
5,60 |
2,70 |
2,90 |
3,03 |
„ |
15 |
„ |
„ |
„ |
97,7 |
5,82 |
3,05 |
2,77 |
2,83 |
„ |
20 |
„ |
„ |
„ |
99,3 |
6,03 |
3,40 |
2,63 |
2,65 |
„ |
30 |
„ |
„ |
„ |
100,1 |
6,10 |
3,53 |
2,57 |
2,57 |
„ |
40 |
„ |
„ |
„ |
100,9 |
6,21 |
3,61 |
2,60 |
2,58 |
Приведенные в таблице данные свидетельствуют о том, что повышение общего содержания сухих веществ в огурцах происходит за счет накопления в них соли. Особенно много соли (около 70% ее конечного содержания) накопляется в первые пять дней ферментации. Затем темпы диффузии соли замедляются.
Основные сухие вещества огурцов — сахар, азотистые, минеральные вещества и другие, до конца ферментации, заканчивающейся на 30-й день, все время убывают. К концу ферментации остается всего 52,5% сухих веществ без соли в процентах к абсолютному количеству. Следовательно, огурцы теряют основных сухих веществ 47,5%, т. е. почти половину, из которых 40,4% теряется, в основном, в первые пять дней ферментации.
Количество поступающей в огурцы соли превышает количество сухих веществ, уходящих из них. Это происходит в течение всего периода ферментации.
Как одно из важнейших явлений следует отметить непрерывность осмоса и диффузии растворимых веществ. Осмос и диффузия продолжаются до тех пор, пока не устанавливается равновесие по всей массе (огурцы + рассол). Это стремление к равновесию наблюдается и для молочной кислоты и других растворимых веществ.
Преобразование сахара в молочную кислоту является основным в цепи превращений сухих веществ в процессе ферментации. Образовавшаяся при ферментации огурцов молочная кислота выполняет, по крайней мере, две важнейшие функции — консервирующего средства и одного из главных вкусообразующих элементов. Естественен поэтому интерес к вопросу о том, как происходят превращения сахаров при ферментации, какие образуются при этом продукты и каково влияние внешних условий на ход этого процесса. Исследование динамики сахаров, как и всех других веществ, производилось нами в тех же опытах, в которых изучалась динамика сухих веществ и влаги в целом.
Динамика сахара по отдельным периодам ферментации в наших опытах представлена на рис. 6.
| {42} |
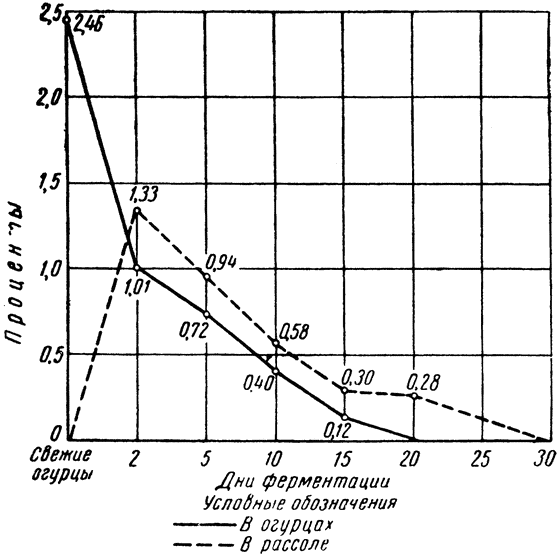 |
Рис. 6. Изменение содержания сахара в процессе ферментации |
Из этих данных следует, что в первые два дня ферментации вследствие усиленного осмоса в рассол перешла значительная часть сахара, как составная часть огуречного сока. В огурцах его осталось 1,01%, а в рассоле накопилось 1,33%. Общий расход сахара за этот период еще незначителен. В дальнейшем происходит постепенное снижение содержания сахара и в огурцах и в рассоле. При этом следует отметить исчезновение сахара в огурцах на 20-й день, а в рассоле — только на 30-й день ферментации. Эти данные являются следствием того, что основное сбраживание сахара происходит не в огурцах, а в рассоле по мере его поступления из огурцов. К этому выводу приводит и анализ кривых динамики сахара в огурцах и в рассоле. После первых двух дней ферментации содержание сахара в рассоле и в огурцах падает по почти параллельным кривым, причем содержание сахара в рассоле псе время выше, чем в огурцах. Конечно, это не исключает сбраживания небольшой части сахара и в самих огурцах, что подтверждается исследованиями Ф. Г. Саруханян и Р. С. Каримян.
Если динамика сахара идет по убывающей кривой, то накопление молочной кислоты — основного продукта брожения — происходит по кривой возрастающей, как это показано на рис. 7.
Однако характер этой кривой свидетельствует о неравномерности темпов накопления молочной кислоты.
Такая динамика кислотообразования вполне закономерна для данных условий ферментации. Следует напомнить, что первые
| {43} |
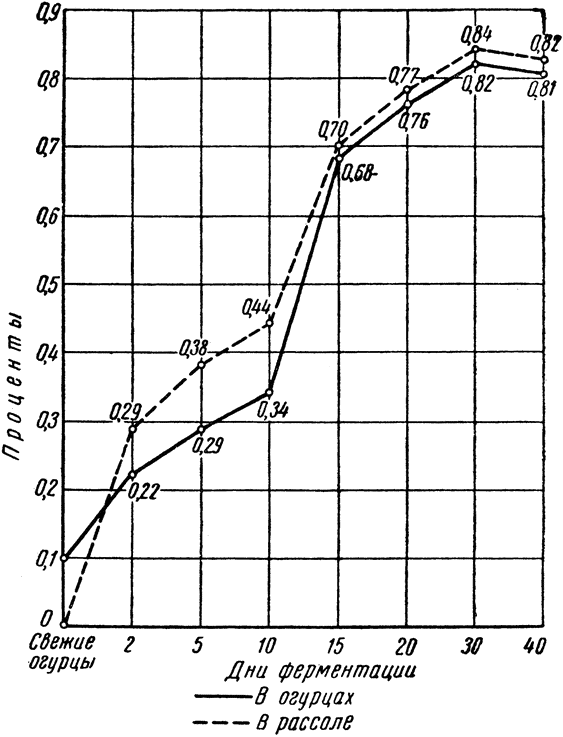 |
Рис. 7. Накопление молочной кислоты в процессе ферментации |
два дня засоленные огурцы выдерживались при температуре 18–20°, а затем были перенесены в подвал с температурой 10–12°. Это обстоятельство и обусловило сравнительно высокие темпы накопления кислоты в первые два дня, снижение их в последующие периоды и резкий подъем после того, как молочнокислые бактерии приспособились к новым температурным условиям.
В нашей литературе еще недостаточно освещен вопрос влияния температуры на развитие молочнокислых бактерий и быстроту кислотообразования при квашении овощей. Это констатируют Б. С. Алеев и Ф. М. Чистяков. Однако из их данных следует, что если брожение ведется при повышенной температуре, то быстрее идут подкисление и развитие молочнокислой флоры.
Н. Е. Насальская, специально исследовавшая соление огурцов, отмечает в своих опытах, что за 72 часа в сусле, зараженном молочнокислыми бактериями, кислоты образовалось при температуре 16–18° 0,20%, а при температуре 26° — 0,72%, т. е. в 3,6 раза больше. {44}
В более обширной литературе по микробиологии молока вопрос о влиянии температуры на развитие микроорганизмов освещен лучше.
А. Ф. Войткевич и другие приводят такие данные о размножении микрофлоры молока при интересующих нас температурах (в миллионах на 1 мл молока): за 24 часа при 12° — 8,2 и при 20° — 163, а за 48 часов при 12° — 27 и при 20° — 350. Это — данные о размножении всей микрофлоры молока, однако не надо забывать, что преобладающими здесь являются молочнокислые бактерии разных видов. Подтверждение этих данных имеется и у С. Панфилова, который говорит, что можно считать правилом увеличение количества микробов в молоке при температуре 10–12° в 1–5 раз, а при температуре 18–20° в сотни раз.
И по нашим исследованиям (41) в огурцах, проходивших ферментацию на леднике при температуре 1–2°, через 30 дней после засола кислоты накопилось 0,28%, а в огурцах, которые проходили ферментацию при 16–18°, — 0,81, т. е. в три раза больше.
Если с точки зрения приведенных исследований вполне закономерным является замедление темпов кислотообразования после перенесения огурцов в подвал с пониженной температурой, то таким же закономерным явлением надо считать и последующее резкое повышение темпов кислотообразования между 10-м и 15-м днями ферментации. Так, в первые восемь дней ферментации огурцов при пониженной температуре развитие молочнокислых бактерий замедлилось и несколько затормозилась их жизнедеятельность. Но за этот период бактерии постепенно приспособились к пониженной температуре, к новым условиям и стали вновь проявлять присущую им энергию кислотообразования.
Подтверждением наших выводов являются исследования А. Ф. Войткевича и других, которые указывают, что в опытах по длительному выдерживанию молока при 0° в течение первых трех—семи дней число бактерий увеличивалось очень медленно, а затем начинало возрастать быстро, достигая через две-три недели очень высокой цифры.
Уменьшение темпов образования кислоты в последующие периоды — на 20-й и 30-й дни ферментации, объясняется тем, что основное количество сахара сброжено за первые 15 дней и в дальнейшем происходит лишь дображивание его остатков.
В период между 30-м и 40-м днями соления огурцов происходит уже не увеличение, а уменьшение содержания кислоты. К 30-му дню весь сахар рассола и огурцов сброжен и, следовательно, иссякли источники образования кислоты, а деятельность микрофлоры, потребляющей кислоту, продолжалась и это сказалось на уменьшении содержания кислоты.
Микрофлора, потребляющая кислоту, начала развиваться в огурцах значительно раньше конца ферментации — возможно даже с самого ее начала. Но результаты жизнедеятельности этой микрофлоры не улавливались анализами до тех пор, пока шло {45} кислотообразование, так как темпы образования кислоты были значительно выше темпов ее разрушения.
Необходимо отметить, что, в конечном счете, к концу ферментации, т. е. через 30 дней, всего образовалось молочной кислоты в огурцах и в рассоле вместе по весу только 54% веса сахара, содержащегося в свежих огурцах. Это явление надо считать нормальным для данного способа консервирования. Большинство молочнокислых бактерий, в том числе наиболее часто встречающихся при солении огурцов вариететов В. cucumeris fermentath по мнению Т. Я. Палея, В. Семенова, Я. Я. Никитинского и Б. С. Алеева, являются газообразующими. Кроме того, в огурцах происходит спиртовое брожение, сопутствующее молочнокислому, возбудителем которого являются дрожжи. По нашим исследованиям в соленых огурцах обнаружено 0,14% спирта.
По данным Я. Я. Никитинского и Б. С. Алеева в огуречном рассоле обнаружены кислоты янтарная, уксусная и др. В процессе ферментации одновременно или через некоторый период после начала ферментации развиваются различные потребители молочной кислоты в виде дрожжей mycoderma, torula и плесеневых грибков oidium lactis, penicillium, aspergillus и др.
Наконец, следует иметь в виду, что весьма сложный биохимический процесс преобразования сахара, в частности в молочную кислоту, очевидно, растянут во времени и поэтому в огурцах и р рассоле всегда могут находиться промежуточные продукты молочнокислого и спиртового брожения, не обнаруживаемые нашими анализами.
Такой вывод подтверждается следующим. Одновременно с проведением анализов химического состава огурцов и рассола мы производили и точное их взвешивание, чтобы установить по отдельным периодам ферментации содержание сахара и кислоты в весовых количествах во всей кислой массе (огурцы + рассол). Это дало нам возможность подсчитать расход сахара и накопление молочной кислоты по периодам. Если пересчитать полученные весовые количества расхода сахара в процентах к его первоначальному содержанию, а кислоты — к ее наибольшему количеству в конце ферментации (на 30-й день), то получается такой ряд цифр:
Расход сахара |
Накопление |
||||
Первые |
2 |
дня |
ферментации . . . |
22,7 |
24,6 |
Спустя |
5 |
дней |
....... |
44,8 |
34,9 |
„ |
10 |
„ |
....... |
67,6 |
41,9 |
„ |
15 |
„ |
....... |
86,8 |
82,0 |
„ |
20 |
„ |
....... |
92,4 |
91,8 |
„ |
30 |
„ |
....... |
100,0 |
100,0 |
Разрыв между накоплением молочной кислоты и расходом сахара в период после первых двух дней ферментации свидетельствует о наличии в бродящей массе промежуточных продуктов молочнокислого брожения. Особенно показателен в этом отношении {46} период между 10-м и 15-м днями ферментации: сахара израсходовано только 19,2%, а кислоты накопилось 40,1%, что могло произойти только при условии образования в предыдущий период промежуточных продуктов, превращение которых в молочную кислоту закончилось между 10-м и 15-м днями ферментации.
В свежих огурцах, взятых нами для засолки, азотистых веществ было 1,33% и минеральных — 0,39%. К концу ферментации (на 30-й день) в соленых огурцах осталось азотистых веществ 0,82% и минеральных (без поваренной соли) — 0,30%. Таким образом, огурцы потеряли в процессе ферментации 38,3% азотистых и 23,1% минеральных веществ по сравнению с первоначальным их содержанием.
Динамика потерь этих веществ по отдельным периодам показана на рис. 8.
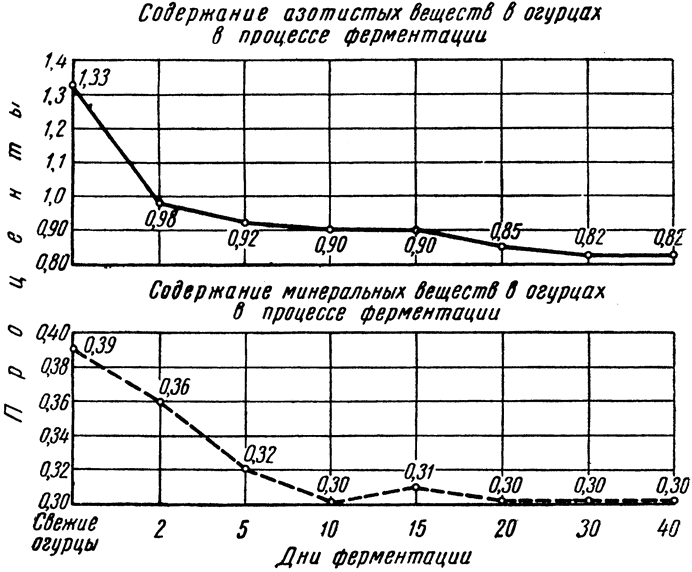 |
Рис. 8. Содержание азотистых и минеральных веществ в процессе ферментации |
Кривая динамики азотистых веществ имеет тот же характер, что и кривая динамики сахара. Это значит, что в первые два дня ферментации, в период усиленного осмоса сока 'в рассол, огурцы теряют наибольшее количество азотистых веществ. Затем темпы потерь снижаются, и на 30-й день падение содержания азотистых веществ в соленых огурцах стабилизируется на уровне 61–62% от первоначального содержания. {47}
По данным Ф. В. Церевитинова азотистые вещества огурцов состоят на 65% из белковых соединений и на 35% из небелковых. Небелковые соединения легче всего переходят в раствор, и наличием их в огуречном соке можно объяснить сравнительно быстрый их переход в рассол (по нашим данным 38,3% всего количества). Остальное же количество азотистых веществ входит в состав протоплазмы клеточной ткани и является наиболее устойчивой частью этой группы веществ.
Для развития микрофлоры в процессе ферментации наибольшее значение имеет именно та часть азотистых веществ, которая находится в растворенном состоянии, так как она более легко используется микроорганизмами. Для сохранения же структуры плодовой ткани огурцов имеет значение другая часть азотистых веществ — белки.
В связи с рассмотрением азотистых веществ необходимо отметить и изменение другой группы коллоидов — пектиновых веществ. Установлено, что в процессе соления огурцов часть пектиновых веществ разрушается, причем разрушение возрастает по мере увеличения размеров огурцов (одного и того же сорта). Так, при содержании в свежих корнишонах (50–70 мм) 0,28% пектиновых веществ в соленых осталось их 0,19%, в средних огурцах (91–120 мм) содержание их снизилось с 0,24 до 0,12% и в крупных (121–140 мм) — с 0,18 до 0,07%. Содержание пектина в соленых огурцах по сравнению со свежими уменьшилось в корнишонах на 32%, в средних огурцах на 50%, а в крупных на 61%.
Очевидно, разрушенная часть пектиновых веществ приходится на долю растворимого пектина, так как в соленых огурцах обнаружен только протопектин. Исключение составляют крупные огурцы, в которых найдено растворимого пектина 0,02%. Следует отметить, что крупные соленые огурцы были с дряблой мякотью, и обнаруженный в них растворимый пектин, видимо, был получен вследствие гидролиза протопектина, наличие которого характерно для прочной плодовой ткани.
Минеральные вещества огурцов израсходованы в процессе ферментации в меньшей мере, чем азотистые и пектиновые — всего в количестве 23,1% их первоначального состава. Основное количество минеральных веществ уходит из огурцов в первые пять дней ферментации, т. е. в период усиленного выделения сока огурцов в рассол. Следовательно, минеральные вещества, перешедшие в рассол, входили либо в состав растворимых небелковых азотистых соединений, либо фосфорной, кремневой, серной кислот, о наличии солей которых в огурцах указывает Ф. В. Церевитинов (89).
Минеральные вещества, не перешедшие в раствор, находятся в прочной связи с белковыми соединениями, которые составляют основу клеточной ткани огурцов и в рассол тоже не переходят.
| {48} |
В проведенном нами опыте было обнаружено, что свежие огурцы содержали 12,5 мг% витамина С. По окончании ферментации (на 30-й день) содержание его снизилось до 3,95 мг%, на 40-й день его осталось всего 3,70 мг%.
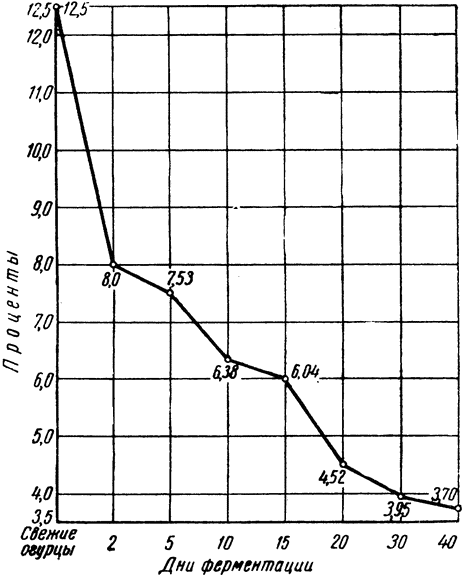 |
Рис. 9. Содержание витамина С в огурцах в процессе ферментации |
Кривая содержания витамина С (рис. 9) круто снижается в течение всего процесса ферментации. Наибольшее падение наблюдается в первые два дня ферментации, когда в огурцах еще только начался процесс накопления молочной кислоты. За этот период огурцы потеряли больше одной трети первоначального содержания витамина С. Но в последующие периоды темпы потерь витамина в огурцах замедляются, что является следствием повышения кислотности среды.
На степень изменения содержания в огурцах витамина С в процессе ферментации влияют условия ферментации, способы засолки и укладки огурцов в тару и ряд других факторов.
Проф. Г. Г. Скробанский (74) своими исследованиями установил, что шпаркой огурцов перед посолом нагретой до кипения водой в течение двух-трех минут можно добиться очень хорошего сохранения витамина С. Засоленные после шпарки огурцы, по его данным, содержали 9,8 мг% витамина С, а засоленные без {49} шпарки — всего 3–3,5 мг%. Это объясняется инактивацией аскорбиназы в процессе шпарки.
На конечное содержание витамина С в соленых огурцах, по данным Г. Г. Скробанского, влияет подбор специй, с которыми засаливают огурцы. Он нашел, что, применяя при засолке огурцов свежие хрен (корень и листья), горький стручковый перец, укроп, листья черной смородины, дуба, вишни, богатые витамином С, можно, не повышая количества специй, повысить содержание витамина С в соленых огурцах и улучшить их вкусовые достоинства.
По данным того же исследователя, плотная укладка огурцов в бочку способствует лучшему сохранению витамина С, чем рыхлая, так как при плотной укладке увеличивается масса огурцов (витаминоноситель) и уменьшается количество рассола (растворителя). Так, при укладке огурцов в количестве 40, 43 и 46 кг в бочонки одной и той же емкости через пять месяцев после засолки в соленых огурцах, соответственно, было обнаружено витамина С : 0,86; 1,53 и 3, 84 мг%.
Это же подтверждается и нашими исследованиями.
В бочках, где огурцы составляли 60% от веса всей массы с рассолом, витамина С сохранилось 5,39 мг%, в бочках с 55% огуречной массы — 4,94 мг%, 50% — 4,49 мг% и 45% — 4,02 мг%.
На сохранение витамина С оказывает значительное влияние также крепость рассола.
По нашим исследованиям в соленых огурцах, содержавших в свежем виде 12,6 мг% витамина С и залитых рассолом с разной концентрацией соли, было обнаружено следующее количество витамина С:
Концентрация |
Содержание |
|
7 | 4,22 | |
10 | 3,66 | |
12 | 2,41 | |
15 | 1,00 |
Повышение концентрации соли вызвало торможение развития молочнокислых бактерий и накопления молочной кислоты, что и привело к значительному разрушению витамина С.
Однако накопление молочной кислоты — фактор вторичного действия. Повышение концентрации соли вызывает усиление осмоса огуречного сока в рассол, а вместе с соком — и растворенной в нем аскорбиновой кислоты. Таким образом, с повышением крепости рассола происходит более значительное выщелачивание витамина С из огурцов.
Из всех факторов наиболее значительное влияние на сохранение витамина С в огурцах оказывает температура ферментации. По нашим исследованиям при проведении главного периода брожения в ледниках витамина С сохраняется в огурцах в 2–2,5 раза больше, чем в неохлаждаемых помещениях. Данные о влиянии {50} температуры ферментации на сохранение витамина С в соленых огурцах приводятся в табл. 21.
|
ТАБЛИЦА 21
| |||||||||||||||||||||||||||||||||||||
Как показывают эти исследования, при ферментации огурцов в неохлаждаемых складах в огурцах сохранялось витамина С от 24,12 до 29,63% первоначального содержания в свежих огурцах, а при ферментации в ледниках — от 52,06 до 70,07%. Эти исследования приводят к выводу о необходимости возможно более широкого внедрения в практику ледниковой ферментации огурцов. При хранении засоленных огурцов малого размера на льду можно достичь содержания в них 9–10 мг% витамина С. Крупные огурцы при неохлаждаемом хранении практически можно считать безвитаминными.
В главе о физических изменениях огурцов в процессе ферментации была показана зависимость характера этих изменений от степени зрелости огурцов. Изменения физических свойств находятся в закономерной зависимости от изменений их химического состава.
По нашим исследованиям в соленых огурцах при ледниковой ферментации сухие вещества (в процентах к содержанию их в свежих) составляют: в корнишонах — 100,5%, в мелких огурцах — 112,8, в средних — 120 и в крупных — 127%. Это объясняется большей прочностью ткани мелких огурцов, зависящей от большого содержания в них коллоидов и, в частности, азотистых веществ.
Сопоставление данных о нарастании сухих веществ в огурцах с данными о содержании в них азотистых веществ, приведенное в табл. 22, подтверждает правильность этого вывода.
Большая прочность огуречной ткани мелких огурцов обусловливает и большую сопротивляемость ее обмену с внешней средой. Этим объясняются и лучшие вкусовые и структурные качества мелких огурцов по сравнению с крупными. Обладая большей коллоидной системой, огурцы малых размеров меньше отдают в рассол своего сока и меньше впитывают из него соли.
| {51} |
|
ТАБЛИЦА 22
| |||||||||||||||||||||||||||||
Кроме того, в более мелких огурцах лучше используется сахар на образование молочной кислоты. Если содержание молочной кислоты в соленых огурцах (ледниковой ферментации) выразить в процентах к содержанию сахара в свежих, то получится такой ряд цифр:
в |
огурцах |
50–70 |
мм |
. . . |
73,8 |
„ |
„ |
71–90 |
„ |
. . . |
52,9 |
„ |
„ |
91–120 |
„ |
. . . |
43,3 |
„ |
„ |
121–140 |
„ |
. . . |
44,0 |
Проведенные нами исследования показывают, что при ледниковой ферментации образовывалось молочной кислоты больше, чем при ферментации в неохлаждаемых складах: в огурцах длиной 50–70 мм — на 24,2%, длиной 71–90 мм — на 19,3%, длиной 91–120 мм — на 18,2% ив крупных огурцах длиной 121 — 140 мм — на 22%. В среднем увеличение несколько превышает 20%.
При ферментации огурцов в неохлаждаемых помещениях молочной кислоты образуется в среднем около 50% израсходованного сахара, что объясняется особенностями молочнокислой микрофлоры, из которой основные виды газообразующие, и тем, что в этих условиях деятельное участие в брожении принимают дрожжи и другие виды микроорганизмов, расходующие сахар на образование разных побочных продуктов. При ледниковой ферментации благодаря большей направленности молочнокислого брожения в огурцах образуется молочной кислоты в среднем около 70% от содержания сахара.
Более эффективно происходит сбраживание сахара в менее развитых огурцах — мелких, вследствие большего содержания в них коллоидов и, в частности, азотистых веществ. Наличие большего содержания коллоидов обусловливает и лучшую структуру огуречной ткани.
Таким образом, на ход и результаты химических превращений в огурцах в процессе их ферментации особое влияние имеют температура ферментации и содержание коллоидов в сырье.
| {52} |
Глава восьмая
Физико-химические процессы, происходящие в соленых огурцах при их хранении, резко отличаются от процессов ферментационного периода.
В процессе хранения абсолютный вес огурцов постепенно падает, уменьшается их объем, содержание воздуха в плодовой ткани несколько повышается, снижается удельный вес плодов и содержание сухих веществ, а содержание влаги соответственно возрастает (см. табл. 23).
|
ТАБЛИЦА 23
| ||||||||||||||||||||||||||||||
Для периода ферментации характерны превращения сахаров и интенсивный обмен растворимыми веществами между плодами и рассолом до установления равновесия в бродящей среде. При хранении огурцов превращения сахаров и такого обмена уже нет. Происходящее в этот период уменьшение сухих веществ и, в частности, азотистых веществ и кислоты, сопровождающееся некоторым ухудшением структуры плодовой ткани, является результатом разрушительного действия микрофлоры, потребляющей молочную кислоту, химического взаимодействия образовавшихся к концу ферментации веществ и некоторых других факторов (давление, температура).
Чем длиннее срок хранения, тем глубже происходящие изменения.
Изменения физических свойств огурцов при хранении зависят от температуры хранения. При хранении огурцов на льду физические свойства изменяются более медленно, чем при хранении их в неохлаждаемых помещениях. Об этом свидетельствуют данные по хранению огурцов, засоленных в 125-литровых бочках на Корчаковском засолочном заводе (см. табл. 24).
| {53} |
|
ТАБЛИЦА 24
| ||||||||||||||||||||||||||||||||||
При хранении на леднике огурцы меньше теряют в весе и содержание в них воздуха почти не изменяется, а в неохлаждаемом помещении заметно незначительное увеличение содержания воздуха в огурцах. Увеличение содержания воздуха в плодовой ткани связано с ухудшением ее структуры, которое вызывается частичным распадом белков и является одним из признаков старения ткани.
Следовательно, ледниковое хранение огурцов тормозит процесс их старения.
Огурцы мелких размеров по сравнению с крупными при хранении, как и при ферментации, более стойки. Физически это проявляется в лучшем-сохранении абсолютного веса. По наблюдениям, проведенным в производственных условиях, вес огурцов разных размеров, хранящихся в 125-литровых бочках, за шесть месяцев хранения изменился (в процентах к их весу по окончании ферментации) таким образом:
На леднике |
В неохлаж- |
|||
Корнишоны |
(50–70 мм) . . . |
100,2 |
99,6 |
|
Мелкие |
огурцы |
(71–90 мм) . |
99,5 |
99,3 |
Средние |
„ |
(91–120 мм) . |
99,5 |
99,2 |
Крупные |
„ |
(121–140 мм) . |
99,3 |
99,0 |
Корнишоны в течение шестимесячного хранения на льду не только не потеряли в своем весе, но продолжали «набухать». Огурцы всех остальных размеров и корнишоны при хранении в неохлажденном складе несколько уменьшили свой вес и тем в большей степени, чем они крупнее. В конечном итоге это явление связано с прочностью плодовой ткани, обусловливаемой содержанием белков, которое уменьшается по мере развития плодов. Более богатая коллоидами ткань огурцов, как это мы видели при рассмотрении процесса ферментации, обладает большей водо-удерживающей способностью и меньшей способностью к обмену с окружающей средой (рассолом). Поэтому на незначительные химические изменения рассола, происходящие при хранении, {54} прежде всего и больше всего реагируют огурцы с менее прочной мякотью.
Изменения химического состава огурцов при хранении ни по интенсивности, ни по своему характеру не могут быть сравнимы с процессами, происходящими при ферментации. Часто эти изменения количественно очень незначительны, но они могут оказать большое влияние на качество продукции, так как отдельные из них носят характер ничем не восстанавливаемых разрушений (азотистые вещества, кислота).
Вышесказанное подтверждается опытами, которые были про--ведены с огурцами размером 91–120 мм, засоленными в 8%-ном рассоле в 18-килограммовых бочонках.
Изменение химического состава этих огурцов при хранении приведено в табл. 25.
|
ТАБЛИЦА 25
| |||||||||||||||||||||||||||||||||||||||||||
Увеличение содержания влаги (табл. 25) только кажущееся. Если учесть, что при хранении огурцы несколько теряют в весе, и если пересчитать содержание влаги на фактический вес, то оказывается, что через 3 месяца хранения содержание влаги составляет 93,76 и через 6 месяцев — 93,52%. Таким образом, абсолютное количество влаги в огурцах уменьшается.
Сухие вещества и все их составные элементы также обнаруживают тенденцию к уменьшению.
Азотистых веществ за весь период хранения потеряно 0,10% и кислоты 0,14%, что вместе составляет 0,24%. Это — небольшие потери, которые можно было бы не принимать во внимание. Но азотистые вещества, оставшиеся в огурцах после ферментации, вместе с клетчаткой составляют основу плодовой ткани. Малейшее уменьшение их количества ухудшает структуру плодовой мякоти: вызывает увеличение содержания воздуха, потерю эластичности и пр.
| {55} |
Сопоставим ряд цифр:
Через 3 |
Через 6 |
|
Уменьшение содержания азотистых веществ (в % на сухое вещество) ................. |
0,3 |
0,9 |
Увеличение содержания воздуха в плодовой ткани (в %) . |
0,11 |
0,30 |
Абсолютная потеря влаги (в % к начальному количеству) . |
0,10 |
0,40 |
Сокращение объема плодов (в %)......... |
0,14 |
0,56 |
Из этих цифр видно, что с течением времени потеря азотистых веществ в огурцах возрастает. С возрастанием потерь азотистых веществ уменьшается водоудерживающая способность плодовой ткани и, как следствие этого, возрастает потеря влаги и увеличивается содержание воздуха в плодовой ткани. Все это приводит к сокращению объема плодов. Эти изменения сопровождаются ухудшением консистенции плодов: Плоды становятся все более дряблыми, т. е. стареют.
Таким образом, можно безошибочно утверждать, что потеря азотистых веществ при хранении, происходящая в результате распада белков ткани, приводит к старению огурцов.
Плоды огурцов в разных стадиях развития обладают коллоидной системой разной прочности. По нашим исследованиям огурцы, засоленные в производственных условиях (в 125-литровых бочках), содержали через 6 месяцев хранения следующее количество азотистых веществ (в процентах к началу хранения):
Размер плодов |
Хранение |
Хранение в не- |
||
51–70 |
100 |
93,1 |
||
71–90 |
97,3 |
90,8 |
||
91–120 |
94,4 |
87,6 |
||
121–140 |
90,8 |
82,1 |
Из этих данных следует, что для хранения на продолжительный срок желательно оставлять огурцы более мелких размеров, особенно корнишоны, так как при хранении они меньше теряют азотистых веществ, вследствие чего процесс старения тормозится. Огурцы лучше сохраняются (меньше теряют азотистых веществ) при хранении в ледниках, чем в неохлажденных складах.
По данным табл. 25 соле-кислотный коэффициент соленых огурцов, являющийся основой их вкусовой оценки, изменился в процессе хранения довольно резко. Так, в начале хранения отношение соли к кислоте было равно 3,58/0,81 = 4,4, а в конце 3,55/0,67 = 5,3. Надо сказать, что наилучшими вкусовыми качествами обладают огурцы с соле-кислотным коэффициентом в пределах от 4 до 5.
Огурцы с отношением соли к кислоте выше 5 будут по вкусу излишне солеными и по вкусовым достоинствам их необходимо переводить в более низкий сорт. {56}
Процесс старения огуречной ткани при хранении значительно ускоряется с потерей кислотности. Снижение же кислотности огурцов при хранении в бочках явление почти неизбежное. Выше указывалось, что при солении огурцов одновременно с развитием молочнокислых бактерий, накапливающих кислоту, развиваются и ее потребители. Жизнедеятельность этих бактерий незаметна до тех пор, пока происходит кислотообразование, пока темпы образования кислоты превышают темпы ее разрушения различными потребителями. Но с окончанием кислотообразования пагубное действие потребителей молочной кислоты сразу же сказывается. Поэтому при хранении огурцов наблюдается систематическое снижение кислотности.
При неудовлетворительных условиях хранения (недолив рассола, создающий аэробные условия, высокая температура) в огуречном рассоле развивается поверхностная пленка, состоящая из пленчатых дрожжей и плесеней (mycoderma, toruia, oidium lactis, penicillium, aspergillus и пр.), которые в течение очень короткого периода могут разрушить почти всю накопившуюся при ферментации кислоту.
В анализируемом нами случае (см. табл. 25) содержание кислоты в огурцах за 3 месяца хранения уменьшилось на 7,7% (в абсолютных количествах) и за 6 месяцев — на 17,9%, благодаря чему кислотность их снизилась с 0,81 до 0,67% к концу хранения.
Ледниковая ферментация огурцов с последующим хранением их в ледниках способствует большему накоплению и лучшему сохранению молочной кислоты в огурцах, чем ферментация и хранение в неохлаждаемых складах.
Заслуживает внимания интересное явление, наблюдавшееся нами при хранении огурцов разных размеров. В табл. 26 приводятся данные по сохранению кислотности (через 6 месяцев хранения) огурцами сорта нежинские, засоленными в 125-литровых бочках, залитыми одним и тем же рассолом и хранившимися в ледниках и неохлаждаемых помещениях.
|
ТАБЛИЦА 26
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {57} |
Из данных таблицы видно, что в ледниках кислотность огурцов сохраняется лучше, чем в неохлаждаемых складах. Кислота хуже сохраняется в тех огурцах, в которых ее было меньше к началу хранения.
Таким образом, чем выше кислотность в начале хранения, тем лучше она сохраняется. Это вполне понятно: чем выше концентрация кислоты, тем сильнее ее консервирующее действие и тем хуже, следовательно, условия для развития всякой микрофлоры и в том числе потребителей кислоты. Размер огурцов также имеет значение. В огурцах небольших размеров количество накопленной кислоты больше и сохранность ее лучше.
Учитывая прогрессивный характер разрушения кислоты при длительном хранении огурцов в неохлаждаемых складах, огурцы с кислотностью ниже 0,9% не следует закладывать на хранение. В огурцах с кислотностью 0,8% к концу хранения кислоты может остаться менее 0,6%, что приведет к переводу продукции в нестандартное качество.
Витамин С при хранении разрушается. Из приведенных в табл. 23 и 24 данных видно, что через 3 месяца хранения витамина С в огурцах осталось 60,5%, а через 6 месяцев — 57,3% его содержания к началу хранения. Почти такое же явление мы наблюдали в огурцах, засоленных на Корчаковском засолочном заводе в 125-литровых бочках, хранившихся в неохлаждаемом складе. Через 3 месяца в этих огурцах осталось 59,8% исходного содержания витамина С, а через 6 месяцев — 57,1%.
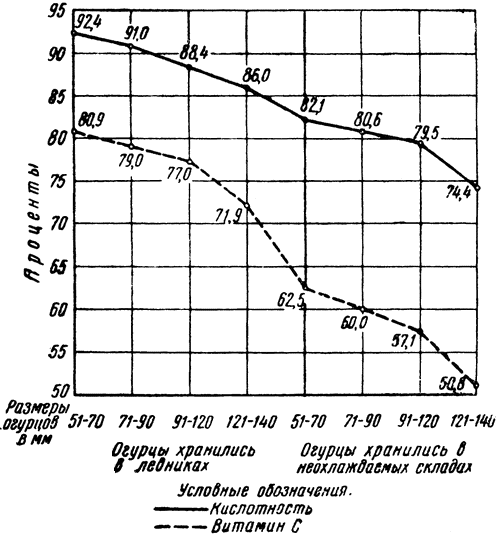 |
Рис. 10. Наличие кислоты и витамина С через 5 месяцев хранения (в процентах к содержанию в огурцах после ферментации) |
| {58} |
Однако нами установлено, что в некоторых случаях витамин С в течение 6 месяцев сохраняется на 70–80%, а конечное его содержание в огурцах колеблется в пределах от 1,25 до 7,66 мг%.
Изучая содержание витамина С в нежинских огурцах различных размеров, мы получили такие данные (см. рис. 10).
На рис. 10 сопоставлены в зависимости от содержания кислоты к началу хранения две кривые — кривая сохранения кислотности и кривая витамина. Характер этих кривых очень показателен. С понижением кислотности усиливается разрушение витамина С, причем это разрушение идет быстрее, чем разрушение молочной кислоты.
Рассматривая хранение соленых огурцов, мы попытались изложить сущность происходящих в них физико-химических изменений и выяснить факторы, влияющие на характер и скорость этих изменений.
Все физико-химические изменения в соленых огурцах при хранении носят разрушительный характер, приводящий к ухудшению их качества и количественным потерям. Однако происходящие процессы при правильном хранении могут быть заторможены и потери сведены к минимуму.
В подтверждение этих выводов в табл. 27 приводятся средние данные исследований авторов по изменению веса огурцов разных
|
ТАБЛИЦА 27
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
размеров при хранении в ледниках и неохлаждаемых складах. Для исследований были взяты огурцы сорта нежинские, засоленные в таре емкостью 125 л.
Глава девятая
Современные исследования в области соления огурцов дают возможность по-новому осветить некоторые явления и внести ряд усовершенствований в существующую технологию. Так, изучение роли отдельных физических свойств и химического состава сырья {59} позволяют установить объективные показатели пригодности для соления разных хозяйственно-ботанических сортов огурцов.
Опытными исследованиями и результатами промышленного соления доказано, что при засолке зеленых огурцов размером до 120 мм в таре малой емкости (до 40 л) и мелких огурцов до 70 мм в таре емкостью до 125 л не только нет убыли при ферментации, но наблюдается некоторое увеличение веса. Установлено решающее значение содержания коллоидов на сохранение плотности структуры плодовой ткани огурцов. Указаны пути наиболее эффективного сбраживания сахара и накопления кислоты, а также наилучшего сохранения витамина С при солении огурцов и пр.
Многие из этих вопросов нашли освещение в предыдущих главах и требуют только некоторого обобщения, а часть из них нуждается в дополнительном освещении.
Содержание настоящей главы не предусматривает изложения технологии соления огурцов — это предмет специальных инструкций1. Здесь будут рассмотрены лишь те вопросы, правильное разрешение которых должно быть положено в основу построения рациональной технологии.
Для того чтобы определить пригодность огурцов для соления, нами было изучено влияние различных физических свойств и химического состава свежих огурцов на качество соленых и на размер потерь при ферментации. Кроме того, было выяснено значение отдельных составных частей свежих огурцов в процессах
|
ТАБЛИЦА 28
| |||||||||||||||||||||||||||||||||||
| {60} |
Размеры |
Степень пригодности для засола |
|||||
при хранении огурцов в ледниках |
при хранении огурцов в не- |
|||||
отличная |
хорошая |
удовлетво- |
отличная |
хорошая |
удовлетво- |
|
50–70 |
1,3 |
1,3 |
1,2 |
1,7 |
1,7 |
1,7 |
71–90 |
1,7 |
1,7 |
1,5 |
2,0 |
2,0 |
2,0 |
91–120 |
— |
1,9 |
1,6 |
— |
2,4 |
2,4 |
121–140 |
— |
— |
1,6 |
— |
— |
2,4 |
ферментации и хранения соленых огурцов. На основании полученных данных были выявлены объективные показатели, которые сведены в табл. 28.
Пользуясь данными этой таблицы, можно на основе анализа свежих огурцов любого хозяйственно-ботанического и товарного сорта, заранее определить степень их пригодности для соления с большим или меньшим приближением, что значительно облегчит экспериментальное испытание технологических свойств свежих огурцов.
Ввиду того, что эффект превращения сахара в кислоту в огурцах находится в зависимости от температурных условий проведения главного процесса брожения и содержания коллоидов в огурцах, показатели содержания сахара приведены дифференцированно по стадиям развития огурцов при ферментации в ледниках и неохлажденных складах. Как известно, содержание коллоидов в огурцах по мере их развития падает, что снижает возможность использования сахара для образования кислоты.
Общепринятым правилом считается засолка огурцов в день их сбора. Огурцы, хранившиеся на сырьевой площадке в течение 2–3 дней, теряют часть влаги, несколько увядают и технологические свойства их ухудшаются. Среди соленых огурцов, полученных из такого сырья, появляются плоды сморщенные, с наличием пустот. Устранить эти дефекты или уменьшить их можно предварительной замочкой огурцов в воде в течение 5–6 часов. В процессе замочки огурцы восстанавливают частично потерянную влагу и первоначальный объем. В результате этого в первые дни ферментации, когда происходит усиленное выделение клеточного сока в рассол, объем плодов и их ткань не претерпевают значительных изменений. Огурцы же, засоленные без предварительной замочки, потеряв часть влаги во время хранения, сильно обезвоживаются в первые дни ферментации, что приводит к сморщиванию и образованию пустот.
Благотворное влияние замочки лежалых огурцов на качество соленой продукции иллюстрируется данными табл. 29.
Физико-химические исследования процессов ферментации и хранения соленых огурцов показали, что эти процессы в плодах различных стадий развития протекают по-разному и вызывают
| {61} |
|
ТАБЛИЦА 29
Примечание. Засолены огурцы первого сорта нежинские, крепость рассола 8%. |
неодинаковые изменения плодовой ткани и плодов в целом. В корнишонах, вследствие особенностей их химического состава и структуры мякоти, более эффективно сбраживаются сахара в молочную кислоту, чем в плодах средних размеров, от 91 до 120 мм. Огурцы, засоленные в более ранней стадии развития, при хранении дольше не стареют. Весовые и объемные изменения в процессе соления в огурцах разных стадий развития происходят тоже неодинаково.
Все эти исследования являются достаточной теоретической основой давно принятого в практике правила — перед засолкой сортировать огурцы по размерам.
Теперь необходимо это правило сделать обязательным. В такой же мере это правило должно быть отнесено и к сортировке огурцов по хозяйственно-ботаническим сортам, так как каждый сорт огурцов обладает присущими ему специфическими особенностями, влияющими на течение процесса ферментации, на качество и выход готового продукта.
Влияние чистоты соли на качество соленых огурцов давно отмечено практиками и некоторыми исследователями. Поэтому по стандарту на соленые огурцы для засолки применяется только пищевая соль. Несоблюдение этого требования и применение нефильтрованных рассолов для заливки огурцов приводит к оседанию на огурцах нерастворимого в воде осадка, напоминающего тонкий налет сероватой плесени, который ухудшает товарный вид продукции.
Наличие в соли повышенного против нормы содержания сернокислых солей магния и кальция особенно отрицательно сказывается на качестве соленых огурцов, приводя к образованию неприятных привкусов и порой к размягчению плодовой мякоти.
Роль соли при солении овощей, в том числе и огурцов, разнообразна. Она вызывает быстрое выделение сока из плодов и в значительной мере направляет происходящий на основе диффузии {62} обмен между огурцами и рассолом, способствует уплотнению плодовой ткани и образованию гармоничных вкусовых ощущений и является вместе с тем консервирующим веществом. Совершенно ошибочным надо считать мнение некоторых авторов (38) о том, что соль в количествах, содержащихся в соленых огурцах, не оказывает значительного консервирующего действия. Оба консерванта — кислота и соль, — взятые порознь, поскольку они находятся в небольших количествах, не обеспечивают консервирования огурцов и только во взаимодействии они создают необходимую консервирующую среду, действие которой усиливается соответствующим набором специй.
Установлено, что соль в концентрации 2% уже значительно ослабляет развитие маслянокислых бактерий. Для прекращения дрожжевого брожения необходимы растворы с содержанием соли 1% и молочной кислоты 2,52% или 3% соли и 1,53% молочной кислоты.
Особенно важно значение соли как консерванта в самом начале «брожения, когда еще только начинается образование молочной кислоты.
Выше уже было сказано о влиянии соли и ее различных концентраций на ход физико-химических процессов при солении огурцов и установлено, что наилучшими для заливки огурцов являются рассолы крепостью в 6–8%. Рассолы такой концентрации способствуют лучшему сохранению структуры плодовой ткани, нормальному накоплению кислоты и образованию наилучших вкусовых ощущений.
На качество соленых огурцов влияет не только крепость рассола, но и плотность укладки огурцов в бочках.
Процентное содержание огурцов в бочке в зависимости от плотности укладки резко колеблется — от 53 (рыхлая насыпь) до 67% (плотная шаровая вертикальная укладка). Соответственно и содержание рассола изменяется от 47 до 33%. Естественно, что при одной и той же крепости рассола содержание соли в продукте будет зависеть от количества вливаемого в бочку рассола. Зная, что в конечном счете соль равномерно распределяется между огурцами и рассолом, нетрудно рассчитать содержание соли в продукте в зависимости от количества рассола и его крепости.
В табл. 30 приводится расчет содержания соли в соленых огурцах в зависимости от крепости рассола и плотности укладки в бочках.
Таким образом, чтобы получить огурцы соленые с содержанием соли от 2,8 до 3% при плотности укладки огурцов в бочки 53, 60, 64 и 67%, надо заливать их рассолом крепостью, соответственно, 6, 7, 8 и 9%. Если требуется получить конечное содержание соли в продукте от 3,2 до 3,3%, то следует при соответствующей плотности укладки применять рассолы крепостью 7, 8, 9 и 10% и т. д.
| {63} |
|
ТАБЛИЦА 30
| ||||||||||||||||||||||||||||||||||
Следовательно, при выборе крепости заливочного рассола нельзя исходить из принятого в практике шаблона: для корнишонов — 6%-ный рассол, для полуводянки — 7%-ный, для водянки — 8%-ный и т. д. При выборе крепости заливочного рассола надо исходить из заданного содержания соли в готовом продукте и плотности укладки огурцов в тару.
В производственных инструкциях, кроме постоянных норм крепости заливочного рассола, должны быть указаны и нормы плотности укладки огурцов в тару.
Если исходить из данных практики, то нормальным следует считать содержание соли в соленых огурцах в пределах от 2,4 до 4%. При этом наименьшее содержание соли наблюдается в корнишонах и наибольшее — в огурцах размером от 91 до 120 мм и выше. Конечно, это характерно только для огурцов, не подвергавшихся вторичной заливке. Исходя из данных практики, следует считать наиболее типичным такое содержание соли в соленых огурцах:
Для |
корнишонов . ...... |
от |
2,4 |
до |
2,8 |
„ |
полуводянки (71–90 мм) . |
свыше |
2,8 |
до |
3,2 |
„ |
водянки (91–120 мм) . . |
„ |
3,2 |
до |
3,75 |
„ |
крупных (121–140 мм) . . |
„ |
3,75 |
до |
4,00 |
Снижение содержания соли в огурцах по мере уменьшения их размеров не ослабляет консервирующего действия всей кислой массы. Как установлено исследованиями, при ферментации больше накопляется кислоты в мелких огурцах. Так, в корнишонах (51–70 мм) — 1–1,1%, в мелких (71–90 мм) — 0,9–1%, в средних (91–120 мм) — 0,8–0,85% и в крупных (121–140 мм) — 0,7–0,8%.
Так как сила консервирующего действия кислой среды в огурцах является результатом взаимодействия кислоты и соли, то уменьшение содержания соли в мелких огурцах компенсируется увеличением содержания в них кислоты. Правильность этого вывода подтверждается расчетами, приведенными в табл. 31.
За характеристику силы консервирующего действия кислой среды огурцов нами принято произведение содержания соли на
| {64} |
|
ТАБЛИЦА 31
|
содержание кислоты. Как видно из табл. 31, во всех случаях эта характеристика находится в пределах 2,8–3,2, т. е. очень близких чисел.
Вкусовые достоинства соленых огурцов и их приятный аромат зависят не только от качества сырья и нормального течения ферментативного процесса, но в большой степени от употребляемых специй.
Специи не только влияют на вкусовые достоинства готового продукта, но и обогащают последний витаминами, уравновешивают ферментативный процесс, затормаживают процессы гнилостного распада веществ и удлиняют срок хранения соленых огурцов.. Таким образом, влияние специй весьма благотворно и многообразно.
Нами были проведены специальные работы по выяснению влияния порознь взятых укропа, чеснока, перца, хрена и эстрагона, а также разных наборов специй при солении нежинских огурцов размером 90–120 мм. Качество соленых огурцов по органолептическим показателям оценивалось по 100-балльной системе, предложенной проф. С. Ф. Церевитиновым, но с более детальной балльной характеристикой отдельных показателей. По отдельным показателям баллы распределялись следующим образом: внешний вид — 15, консистенция — 20, вкус — 30, запах — 20 и цвет — 15.
В зависимости от суммы баллов соленые огурцы относились к одному из следующих сортов:
Высший |
сорт |
. . . |
100–95 |
баллов |
Первый |
„ |
. . . |
94–85 |
„ |
Второй |
„ |
. . . |
84–70 |
„ |
Качество огуречного рассола также оценивалось по 100-балльной системе, без указания количества баллов за каждый органо-лептический показатель (вкус, запах, цвет). Безупречный по своим показателям огуречный рассол оценивался в 100 баллов.
При дегустации огурцы, засоленные с отдельными видами специй, получили следующую балльную оценку (см. табл. 32).
| {65} |
|
ТАБЛИЦА 32
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Результаты дегустации показали, что ни один вид специй, взятых порознь, не может обеспечить получение соленых огурцов отличного качества. Только полный набор специй дал возможность получить огурцы отличного качества: они отнесены не к высшему, а первому сорту, вследствие больших размеров (91–100 мм).
В своих работах мы выяснили также значение каждого вида специй при солении огурцов.
Укроп — Anethum graveolens, семейство зонтичных.
Важнейшей составной частью укропа как пряности является эфирное масло, содержание которого в различных частях растения в зависимости от стадии его зрелости колеблется от 0,5 до 4%.
По исследованиям Шалимовой во всей наземной части укрепа обнаружено такое количество эфирных масел по стадиям развития растения (в процентах на сухое вещество): до образования зонтика — 0,577, после образования зонтика до цветения — 0,877, в период цветения — 0,902, в период отцветания — 1,211 и после образования семян — 2,204. В листьях и зонтиках обнаружено масла в период цветения — 1,283%.
Согласно этим исследованиям накопление эфирного масла в растении происходит по мере его роста. В стадии отцветания содержание эфирного масла наибольшее. По растительному организму эфирное масло распространено неравномерно. Наибольшее его количество содержится в плодах укропа — от 2,5 до 4%.
Свежий укроп сравнительно богат витамином С. Разные авторы нашли в укропе следующее количество витамина С: В. Н. Букин — 135 мг%, Г. Г. Скробанский — 72–117 мг%, Л. П. Шалимова — от 120 до 195 мг%. Высушенный укроп теряет свою витаминную активность. Г. Г. Скробанский обнаружил в сухом укропе только 34 мг% витамина. При солении укроп употребляют больше всех других специй (3%) и он может служить хорошим источником обогащения витамином С соленых огурцов.
Экспериментальный засол огурцов был произведен с использованием укропа в стадии отцветания. Рассол помутнел, стал вязким {66} и приобрел неприятный запах. Данные об изменении физических свойств огурцов, засоленных только с укропом, приведены в табл. 33.
|
ТАБЛИЦА 33
| ||||||||||||||||||||||||||||||||
Отсутствие других специй (кроме укропа) вызвало резкое ухудшение плотности ткани и появление пустот у значительного количества плодов (10,5%). Вследствие этих изменений, а также низких вкусовых достоинств огурцов они были оценены как нестандартные.
Чеснок — Allium sativum L., семейство лилейных.
Чеснок содержит довольно значительное количество эфирного масла, придающего огурцам характерный запах и острый вкус, но очень мало витамина С.
По данным Г. Б. Дубровы и Б. П. Токина, чеснок обладает антисептическими и бактерицидными свойствами.
Рутовский нашел в луковицах чеснока 0,06–0,1% эфирного масла с удельным весом 1,0525.
Качество огурцов, засоленных только с одним чесноком, немногим уступает огурцам, засоленным с полным набором обязательных пряностей (табл. 34).
|
ТАБЛИЦА 34
| ||||||||||||||||||||||||||||||||
| {67} |
Хотя соленые огурцы и были отнесены ко второму сорту, но это было вызвано лишь незначительным ухудшением вкуса и отсутствием ароматического букета, свойственного огурцам и рассолу при использовании всех обязательных пряностей.
Очень важно отметить, что чеснок обладает сильным бактерицидным действием. Б. П. Токин делает такой вывод из изучения бактерицидных свойств чеснока:
«Ни одному автору не удалось встретиться в своих опытах с представителями простейших, как патогенных для животных и человека, так и непатогенных, которые оказались бы резистентными в отношении летучих веществ, выделяющихся из только что приготовленной кашицы из луковиц лука и чеснока, а также в отношении соков этих растений. Мы спокойно утверждаем: протистоцидные свойства этих растений универсальны».
По данным этого же автора летучие вещества чеснока убивают дрожжевую клетку. Вместе с тем бактерии молочнокислого брожения оказались устойчивыми в отношении фитонцидов лука и чеснока.
Данные этих исследований являются весьма ценными для практики соления огурцов: они дают возможность избежать действия на продукты дрожжей, плесеней и разных бактерий.
Перец стручковый острогорький — Capsicum annum L. var. microcarpum, семейство пасленовых — Solanaceae.
Жгучий и острый вкус перца зависит от содержания в нем капсаицина, который и придает соленым огурцам специфический острый вкус.
Острый перец, по данным А. Н. Обухова и Д. Л. Понпа, содержит до 0,2% капсаицина, причем в зрелом перце его больше, чем в зеленом.
Перец богат витамином С, что подтверждается весьма многочисленными исследованиями. Поданным Л. Г. Гомоляко, в разных сортах горького перца в стадии физиологической зрелости содержится от 238 до 355 мг% витамина С. Г. Г. Скробанский нашел в перце витамина С от 179 до 184 мг%, а Л. П. Шалимова в зрелом астраханском перце обнаружила от 212,7 до 364 мг%. Таким образом, перец, безусловно, можно считать С-витаминным обогатителем огурцов.
Исследованиями Б. П. Токина обнаружено, что красный перец обладает бактерицидными свойствами.
Вкусовые достоинства соленых огурцов, засоленных с применением в качестве пряностей одного лишь перца, уступают по качеству огурцам, засоленным только с чесноком, но лучше засоленных с укропом.
Приведенные в табл. 35 данные показывают, что физические свойства соленых огурцов, засоленных с одним перцем, не подверглись резким изменениям, но все же они изменились к худшему по сравнению с огурцами, при солении которых был использован полный набор специй.
| {68} |
|
ТАБЛИЦА 35
| ||||||||||||||||||||||||||||||||
Хрен — Cochlearia armoracia L., семейство Cruciferae — крестоцветных.
Острый вкус и запах хрена зависят от наличия в нем эфирного аллилового горчичного масла, выход которого, по данным Рутовского, составляет 0,05%.
Аллиловое горчичное масло находится в хрене не в свободном состоянии, а входит в состав глюкозида синигрина — C10H16KNS2O9, который под действием содержащегося в хрене фермента мирозина расщепляется на сахар, кислую сернокалиевую соль и горчичное масло:
C10H16KNS2O9 |
+ |
Н2О |
= |
C3H5NCS |
+ |
С6Н12O6 |
+ |
KHSO4 |
Синигрин |
+ |
вода |
= |
Аллиловое |
Глюкоза |
Кислая серно- |
Наличие в корне хрена синигрина способствует улучшению вкусовых свойств соленых огурцов, придавая им оттенок приятной остроты. Однако это наблюдается в том случае, если хрен входит как один из компонентов в полный набор специй, — сам по себе он не дает соответствующего эффекта. (При слепой дегустации огурцов, засоленных только с одним хреном, все участники дегустации отдали предпочтение огурцам, засоленным с чесноком).
Хрен обладает большой С-витаминной активностью. Так, проф. Г. Г. Скробанский нашел в корне хрена 259 мг% витамина С и в листьях — от 101 до 410 мг%, Л. П. Шалимова обнаружила в период засолки огурцов (август) в корне хрена 168 и в листьях — 698 мг%. Большое содержание витамина С в корне хрена нашли В. Т. Соколова и 3. В. Черникова и ряд других авторов. Г. Г. Скробанский считает, что применение хрена, особенно его листьев, при солении огурцов будет способствовать обогащению их витамином С.
Но хрен, кроме того, обладает бактерицидными свойствами.
Проф. Б. П. Токин установил своими исследованиями, что летучие вещества (фитонциды) хрена, измельченного в кашицу, убивают дрожжевую клетку так же быстро, как и летучие вещества чеснока и лука. {69}
По нашим исследованиям огурцы, засоленные только с корнем хрена, сохранились хорошо. Среди них обнаружено незначительное количество плодов сморщенных и с внутренними пустотами (2 и 2,1%). Плотность мякоти огурцов была удовлетворительная, но рассол мутноватый.
Эстрагон — Artemisia dracunculus L., семейство сложноцветных — Gompositae.
Эстрагон обладает прекрасным пряным ароматом и превосходным вкусом благодаря наличию особого эфирного масла, главной составной частью которого является эстрагон или метилхавикол — С10Н12О.
По данным Рутовского содержание эфирного масла в целом растении эстрагона составляет 0,54%. Такие же примерно данные мы встречаем у С. В. Жилинского (0,25–0,55%) и у Г. В. Пигулевского (0,5–0,72%).
Содержание витамина С в эстрагоне несколько меньше, чем в укропе. Г. Г. Скробанский определил в нем витамина С 55,8 мг%, а Л. П. Шалимова — 39,4 мг%. Листья эстрагона более богаты витамином, чем стебли.
Однако огурцы, засоленные только с одним эстрагоном, получаются невысокого качества. Вкусовые достоинства их выше, чем огурцов, засоленных с применением укропа или хрена; что же касается других качественных показателей и физических свойств, то, как видно из данных табл. 36, они мало чем отличаются от свойств огурцов, засоленных без использования специй.
|
ТАБЛИЦА 36
| ||||||||||||||||||||||||||||||||
Кроме указанных выше специй (укроп, чеснок, хрен, перец и эстрагон), очень редко при посоле огурцов используются еще и другие пряные растения, рекомендуемые стандартом на соленые огурцы как желательные: майоран, чабер, базилик, иссоп, листовой сельдерей, листья петрушки, кориандр, душица и пр.
Применение их обусловлено в основном наличием эфирных масел приятного аромата. Некоторые из пряных растений богаты витамином С и содержат в своем составе ряд органических веществ (дубильные, глюкозиды и др.), оказывающих положительное {70} влияние на вкусовые достоинства и сохранение структуры ткани огурцов.
Содержание эфирных масел и витамина С в указанных пряных растениях изучали многие исследователи: Рутовский, Г. В. Пигулевский, М. В. Саданосский, Д. Н. Бекетовский, Е. И. Якубец-Якубчик, Ф. В. Церевитинов, Г. Г. Скробанский, С. В. Жилинский, В. Ф. Васильев, Е. В. Вульф, Л. П. Шалимова, В. Н. Букин, А. Базаров, Н. Н. Иванов, Е. А. Столетов и др. В табл. 37 приведена сводка из этих исследований.
ТАБЛИЦА 37
Содержание эфирных масел и витамина С в пряных растениях
Наименование пряных растений |
Содержание |
Содержание витамина С (в мг %) |
Наименование пряных растений |
Содержание |
Содержание витамина С (в мг %) |
Майоран . . . |
0,13–1,00 |
— |
Сельдерей листовой . . . |
0,07–0,1 |
61–95 |
Базилик . . . |
0,12–0,49 |
45–49 |
Листья петруш- |
0,02–0,22 |
100–216 |
Иссоп . . . . |
0,11–0,75 |
80–94 |
|||
Чабер душистый |
0,1–0,5 |
68–95 |
Листья вишни . |
— |
154–286 |
Кориандр (плоды) . . . . |
0,18–0,93 |
4,8 |
Листья черной |
0,013 |
199–239 |
Душица обык- |
0,2–0,59 |
39–87 |
Листья дуба . |
— |
156–160 |
Мята кудрявая |
0,13–0,2 |
123 |
Листья грецко- |
— |
337–500 |
Мята перечная |
0,3 |
100-103 |
Наибольшим количеством эфирных масел характерны майоран, кориандр, иссоп, чабер, душица обыкновенная, базилик. Однако сила аромата этих растений обусловливается не только количеством, но и свойствами эфирных масел. Листья черной смородины, петрушки, сельдерея содержат незначительные количества эфирных масел, однако способствуют образованию в соленых огурцах приятного букета.
После листьев хрена наибольшее содержание витамина С обнаружено в листьях грецкого ореха, черной смородины, вишни, петрушки, дуба. Сравнительно бедны витамином С душица обыкновенная и базилик, а плоды кориандра можно считать практически безвитаминными.
Наибольшее содержание эфирных масел у пряных растений обычно совпадает с периодом цветения, а витамином С они наиболее богаты в ранней стадии развития.
Майоран широко употребляется при засолке огурцов в Чехословакии и Польше, сельдерей — в Молдавской ССР. Проф. Ф. В. Церевитинов рекомендует использование для этих целей чабера, а проф. Г. Г. Скробанский — листьев дуба, черной смородины, вишни и хрена.
Нами установлено, что прибавление пряных растений к стандартному набору специй в количестве 1 кг на 1 ц огурцов улучшает их качество. Так, базилик, иссоп, кориандр придают огурцам {71} приятный и ярко выраженный аромат. Чабер, кроме приятного запаха, усиливает остроту вкуса соленых огурцов. Свежие дубовые, вишневые и черносмородиновые листья, кроме придания огурцам специфического аромата и слегка вяжущего вкуса, содействуют сохранению у огурцов плотной структуры мякоти.
Л. П. Шалимова, изучавшая влияние разных пряностей на вкусовые достоинства соленых огурцов, кроме листьев дуба и черной смородины, особенно рекомендует прибавлять к обычному набору специй по 1 кг на центнер огурцов свежих листьев петрушки и сельдерея. Огурцы с этими пряностями получили наивысшую дегустационную оценку. Огурцы, засоленные с прибавлением кориандра, душицы обыкновенной, мяты, майорана, имели приятный, специфический аромат. Отрицательное влияние на качество соленых огурцов, по мнению Л. П. Шалимовой, имеет портулак, рекомендуемый стандартом в числе желательных специй. Он не придает огурцам аромата, сообщает неприятный привкус, вызывает сгущение рассола и содержит мало витамина С.
К воде, используемой для соления огурцов, кроме санитарно-гигиенических требований предъявляется одно специфическое — это нормы ее жесткости. Жесткость воды сказывается на качестве соленых огурцов. Однако в опенке влияния жесткости воды на качество продукции нет единого мнения. Я. Я. Никитинский и Б. С. Алеев считают, что вода, употребляемая для засолки огурцов, должна быть мягкой, так как в жесткой воде часть молочной кислоты нейтрализуется кальцием карбонатов. В переводе на градусы жесткости мягкой можно считать воду до 8–12°. В инструкции по солению огурцов и томатов Министерства торговли СССР от 30 июля 1949 г. лучшей для приготовления рассола считается вода с жесткостью от 20 до 35°. По исследованиям М. Е. Мельмана (48) наиболее пригодной признана вода с жесткостью в 30–40°. НИИТОП (58) предлагает воду с жесткостью в 30–45°. А. А. Каменев (31), Всеукраинский научно-исследовательский институт ферментативной и плодоовощной промышленности (14) и Всесоюзный научно-исследовательский институт плодоовощной промышленности (15) пришли к выводу, что наилучшей является вода с жесткостью от 43,5 до 45,6°. К этому следует добавить, что Нежинский засолочный завод готовит соленые огурцы, известные своим высоким качеством, на воде из артезианской скважины с общей жесткостью 17,7–29,2°.
Отсутствие единства мнений по этому вопросу свидетельствует о том, что он еще недостаточно изучен. Однако имеющиеся данные дают возможность, хотя и не полностью, выяснить, в чем сказывается влияние жесткости воды при солении огурцов.
А. А. Каменев, проводя экспериментальную засолку огурцов, получил в опытах с применением дождевой воды 59% огурцов {72} с пустотами, причем у 15% огурцов мякоть была резиновой консистенции и у 6% — не хрустящая, а в целом огурцы получили неудовлетворительную качественную оценку. В то же время огурцы, засоленные в воде с жесткостью 43,5–45,6°, все были хрустящие, с цельной плотной поверхностью, хлопушек было обнаружено 9,3% и по качеству огурцы были признаны хорошими.
Обобщая данные своих исследований, Каменев приходит к выводам:
а) что наилучшей для засолки является вода с жесткостью 43,5–45,6°;
б) мягкая вода отрицательно влияет на сохранение ткани и вкус огурцов;
в) слишком жесткая вода (67,2°) также отрицательно влияет на качество продукции.
М. Е. Мельман, засаливая огурцы нежинские в 8%-ном рассоле, приготовленном на воде разной жесткости, получил весьма характерные данные по изменению веса, объема и кислотности огурцов. Так как эти данные представляют теоретический интерес, приводим их в табл. 38.
|
ТАБЛИЦА 38
| |||||||||||||||||||||||||||||||||||||||
По этим данным наилучшие результаты по сохранению объема, веса и содержания кислоты получены при засолке огурцов в воде жесткостью 30–40°. Ниже и выше этого предела уменьшается объем, вес и кислотность. По плотности мякоти и вкусовым качествам наилучшими оказались те же огурцы, засоленные в воде жесткостью 30 и. 40°.
Если в исследованиях А. А. Каменева и М. Е. Мельмана нет единства мнений о норме жесткости воды, что, как мы покажем в дальнейшем, вполне закономерно, то оба эти исследования помогают понять сущность действия жесткости воды на огурцы. С повышением жесткости воды до 40° объем огурцов повышается, что сопровождается увеличением их веса, улучшается структура плодовой ткани — она становится плотной, хрустящей. Одновременно с этим нарастает кислотность. Эти явления возможны только при улучшении набухания коллоидов под влиянием {73} образующейся кислоты. Следовательно, повышение жесткости воды до определенных пределов не только не снижает кислотности, как это предполагают Я. Я. Никитинский и Б. С. Алеев, но даже повышает эффект ее накопления, а последнее вызывает лучшее набухание коллоидов, резко повышающее качество соленых огурцов.
Увеличение жесткости воды за определенными пределами (в данных исследованиях выше 40 или 45,6°) приводит к нейтрализации кислоты, уменьшение ее содержания ухудшает набухание коллоидов и их водоудерживающую способность. Академик А. В. Думанский, отмечая характерное свойство коллоидных систем — способность удерживать воду и набухать в ней, говорит, что происходящее в кислой среде набухание коллоидов можно умерить прибавлением соли. Очевидно, и другие минеральные соли, составляющие жесткость воды в известной концентрации, оказывают на коллоиды подобное же действие, как об этом свидетельствуют приведенные исследования.
Различие мнений и результатов исследований при изучении жесткости воды для соления огурцов объясняется разным подходом к решению этого вопроса. На качество соленых огурцов и, следовательно, на процесс ферментации, оказывает влияние общая жесткость рассола. А жесткость рассола составляется из жесткости воды и жесткости соли. Учитывая только одно из слагаемых жесткости, естественно, исследователи не могли дать единого ответа о нормах жесткости воды.
В соли стандартного качества допускается примесь тех же кальциевых и магниевых солей, которые растворены в воде и составляют ее жесткость. Так, по ГОСТу 153–41 установлены такие нормы содержания кальция и магния по сортам соли (в процентах на сухое вещество):
Са |
Mg |
|||
Экстра | . . . . | . . . . | — | 0,03 |
Высший | сорт | . . . . | 0,6 | 0,1 |
Первый | „ | . . . . | 0,6 | 0,1 |
Второй | „ | . . . . | 0,8 | 0,25 |
Если бы все эти кальциевые и магниевые соли были в растворимом состоянии и всегда находились в пределах установленных норм, то жесткость, составляемая одной только солью, была бы следующей (в градусах):
1%-ный |
8%-ный |
|||
Соль экстра | . . . . | 0,42 | 3,36 | |
Высший | сорт | . . . . | 9,25 | 74,0 |
Первый | „ | . . . . | 9,25 | 74,0 |
Второй | „ | . . . . | 14,0 | 112,0 |
Так как обычно для соления огурцов применяют соль преимущественно первого и второго сортов, то готовя для заливки огурцов 8%-ный раствор, мы можем увеличить его жесткость за счет {74} соли на 74–112°. По сравнению с этой жесткостью жесткость воды играет только вспомогательную роль, являясь меньшим слагаемым в общей сумме жесткости.
Практически, получаемая с промыслов соль содержит меньше кальциевых и магниевых солей и не все они растворимы. Для проверки практической жесткости солевых растворов мы произвели анализ на жесткость трех растворов соли на дестиллированной воде. Два образца соли были взяты с засолочного завода и один куплен в магазине. Результаты анализа приведены в табл. 39.
|
ТАБЛИЦА 39
|
Как видно из данных таблицы, растворы соли по своей жесткости превышают жесткость воды.
Однако следует заметить, что жесткость приготовляемых рассолов не составляет, видимо, полной суммы жесткостей воды и соли, а несколько меньше ее. Приготовленный нами 8%-ный раствор первого образца соли на воде с общей жесткостью 13,5° оказался жесткостью в 41,5°, вместо ожидавшейся суммы 49,5°, т. е. при приготовлении рассолов соли происходит некоторое «умягчение» общей жесткости с выпадением нерастворимых осадков.
Из сказанного можно сделать следующие выводы:
1. В практике соления имеет значение жесткость приготовляемых рассолов, а не только жесткость воды. Исследователи, изучавшие только одно из слагаемых жесткости — воду, — не разрешили этого вопроса и, что вполне естественно, дали разноречивые показатели.
2. Вопрос об оптимальной жесткости рассолов еще не изучен. На основании ориентировочных расчетов можно лишь предполагать, что оптимальная жесткость рассолов должна находиться в пределах 60–75°.
3. Определив оптимальную жесткость рассолов, можно будет легко регулировать ее на каждом предприятии, употребляя при данной жесткости воды соль различной жесткости и разной концентрации.
Сила давления на огурцы в процессе ферментации значительно влияет на изменение их физических свойств (объема, веса, структуры ткани) и связанного с ними качества готовой продукции. {75}
Ввиду значительной отдачи сока в рассол в первые дни ферментации уменьшаются объем и вес огурцов. В последующий период ферментации вследствие интенсивного проникновения рассола в огурцы значительно восстанавливается объем огурцов, почти полностью замещается рассолом воздух в плодовой ткани и вес соленых огурцов не только полностью восстанавливается, но в известных условиях на 1–2% превышает вес свежих. Но так проходят эти изменения в тех случаях, когда диффузия рассола в плоды происходит свободно. Если же огурцы под влиянием давления своей массы в крупной таре в первые дни несколько спрессовываются, диффузия рассола в плодовую ткань ограничивается пределами вновь полученного стабилизированного объема плодов. В этом случае огурцы теряют в своем объеме и весе и тем больше, чем сильнее давление, т. е. чем крупнее тара.
Нами экспериментально установлено, что при использовании тары емкостью до 40 л все зеленые огурцы размерами до 120 мм восстанавливают свой первоначальный вес к концу ферментации. Корнишоны полностью восстанавливают свой вес даже в более крупной таре — до 125 л, а в мелкой — несколько увеличивают его.
Утверждение Министерством торговли Союза ССР новой инструкции по солению огурцов, предусматривающей уменьшение емкости тары, будет способствовать сокращению потерь при ферментации и общему улучшению технологии засолки огурцов.
Однако влияние тары на качество продукции не ограничивается ее емкостью. Неизмеримо большее значение имеет качество деревянной тары. Бочки из мягких пород дерева, за исключением осиновых из колотой клепки, как показала практика, мало пригодны для соления овощей. Без специальной обработки клепка (особенно пиленая) большинства мягких пород пропускает рассолы.
Огурцы, засоленные в таких бочках со строжайшим соблюдением всех правил технологии, получаются низкого качества вследствие необходимости частой доливки их свежими рассолами.
Обработка этих бочек парафином, бакелитовым или другим лаком не достигает цели, так как при укупорке их целостность внутреннего покрытия нарушается. Использование древесины мягких пород для изготовления бочек под соления будет возможно только после специальных работ по уплотнению древесины. До этого для соления желательно использовать бочки из древесины твердых пород и осины, а также стеклянные баллоны.
Весьма существенной для качества соленых огурцов является плотность укладки их в бочки.
Проведенными нами опытами (1938 г.) установлено, что увеличение плотности укладки огурцов не только приводит к экономии тары, но к сокращению многих других расходов и к значительному повышению качества продукции. При специальной рядовой укладке огурцов увеличивается только затрата рабочей силы {76} на их укладку, причем общая затрата рабочей силы на весь процесс засолки возрастает очень незначительно.
Соответствующие расчеты затраты рабочей силы на тонну огурцов при разных способах укладки и расчеты экономической эффективности плотной укладки их в бочки приведены нами в табл. 40 и 41.
ТАБЛИЦА 40
Наименование процессов |
Расход в чел.-смену, на одну тонну продукции |
||
насыпью1 |
горизон- |
вертикаль- |
|
Прием и взвешивание сырья........ |
0,06 |
0,06 |
0,06 |
Подноска к сортировке .......... |
0,27 |
0,27 |
0,27 |
Сортировка на столах .......... |
1,32 |
1,32 |
1,32 |
Подноска к мойке............ |
0,13 |
1,13 |
0,13 |
Мойка ручная............ . |
0,26 |
0,26 |
0,26 |
Подкатка пустых бочек на расстояние до 50 м под закладку............ |
0,13 |
0,12 |
0,11 |
Подноска к бочкам........... |
0,26 |
0,26 |
0,26 |
Подготовка рассола и специй ........ |
0,15 |
0,137 |
0,13 |
Укладка в бочки ............ |
0,23 |
0,69 |
0,92 |
Укупорка бочек ............ |
0,30 |
0,274 |
0,26 |
Взвешивание готовой продукции ...... |
0,13 |
0,12 |
0,11 |
Маркировка.............. |
0,13 |
0,12 |
0,11 |
Подкатка к леднику и спуск ........ |
0,26 |
0,24 |
0,22 |
Подготовка траншей и укладка бочек . . . . |
1,0 |
0,9 |
0,88 |
Выемка бочек из ледника и проверка..... |
0,25 |
0,225 |
0,21 |
Итого чел.-дней...... |
4,88 |
5,126 |
5,25 |
%...... |
100 |
105 |
107,6 |
|
ТАБЛИЦА 41
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {77} |
Данные этих таблиц свидетельствуют, что в то время как затрата рабочей силы на тонну продукции при плотной укладке повышается всего на 5–7,6%, потребность в бочках и их стоимость уменьшается на 10,6%, вес брутто 1 т огурцов сокращается на 9,5%. Это в свою очередь вызывает такое же сокращение транспортных расходов, площади хранения и расходов по хранению.
Кроме экономической эффективности, уплотненная укладка огурцов в бочки вызывает повышение качества огурцов, способствует большему накоплению в них молочной кислоты, следовательно, повышению их стойкости при хранении и сравнительному увеличению их абсолютного веса. Характеристика качества огурцов, уложенных в бочонки с разной плотностью, приведена в табл. 42.
|
ТАБЛИЦА 42
|
Вес огурцов после 5 месяцев хранения составил в процентах к весу свежих: при укладке насыпью — 100,2, горизонтальными рядами — 101,1 и вертикальными — 102,1.
Нет ничего удивительного в том, что с увеличением плотности укладки повышается качество огурцов. В одном случае в 100-литровой бочке во всей кислой массе растворены сухие вещества 60 кг огурцов, а в других случаях — 66–67 кг.
Естественно, что концентрация всех растворимых веществ огурцов при весе их 66–67 кг, будет более высокой, а это вызывает повышение вкусовых достоинств, концентрации кислоты, витамина С и пр.
При обычной нормально плотной укладке огурцов насыпью в бочки, как показала практика, их вмещается по весу 60% емкости бочек.
Проведенными нами в 1947 г. на Нежинском засолочном заводе опытами по выяснению вмещаемости огурцов в бочки разных размеров было установлено, что в среднем в перечислении на бочку 100-литровой емкости вмещается (в кг): корнишонов 60, мелких огурцов (71–90 мм) — 61,1, средних (91–120 мм) — 61,7 и крупных (121–140 мм) — 62,6. Таким образом, есть все основания считать, что содержание в бочке менее 60% огурцов от общего веса огурцов с рассолом есть явление ненормальное.
Это признано уже многими ведомствами, которые планируют на тонну огурцов от 16 до 17 100-литровых бочек, что соответствует {78} плотности укладки от 62,5 до 58,8. При допустимой стандартом 505 плотности укладки в 53%. потребовалось бы бочек (в столитровом исчислении) 18,8.
Направленность процесса ферментации и качество готового продукта в основном обусловливаются подбором сырья, емкостью и качеством тары, качеством воды, качеством и концентрацией соли, набором и качеством специй, плотностью укладки огурцов в тару, т. е. факторами, предшествующими ферментации. Однако качество готового продукта окончательно решается правильным ведением процесса ферментации и условиями хранения.
Для получения огурцов высокого качества и стойких при хранении, а также во избежание излишних потерь необходимо ферментацию их вести с строгим соблюдением условий предварительного теплого и основного холодного брожения.
Иногда при проведении ферментации в неохлаждаемых помещениях в огурцах, кроме обычных молочнокислых бактерий, характерных для огурцов — В. cucumeris fermentati, — развивается еще особый вид слизеобразующих бактерий — В. abderhaldi. Развитие этих бактерий вызывает ослизнение огуречного рассола, а огурцы приобретают несколько более кислый и острый вкус, не теряя своего внешнего вида и качества.
П. Г. Шугаевская, изучавшая явление ослизнения рассола и обнаружившая разновидность В. abderhaldi, считает, что этот вид молочнокислых бактерий попадает в рассол с сырьем. Оптимальная температура слизеобразования и кислотообразования этих бактерий 30–37°; максимальная температура роста 45°, минимальная 5–6°.
При правильном проведении основного холодного периода брожения огурцов можно избежать развития слизеобразующих бактерий.
Шугаевская указывает, что при энергичном взбалтывании бочонков слизистый рассол теряет свою тягучесть и приобретает почти нормальный вид. К еще лучшим результатам приводит продувание воздуха через шпунтовое отверстие. Добавление при солении огурцов чистой культуры В. cucumeris fermentati тормозит развитие слизеобразующих бактерий.
Весьма отрицательное влияние на качество соленых огурцов оказывает доливка бочек рассолом. Причиной вытекания рассола является недоброкачественная тара. Вытекающий рассол содержит кислоту и другие растворимые в воде вещества.
Желая восполнить недостатки рассола, на практике огурцы чаще всего доливают свежим солевым раствором. Это, конечно, никак не может восполнить количество потерянных с«рассолом молочной кислоты и других органических веществ. В результате многоразовых доливок огурцы теряют большую часть молочной {79} кислоты и перенасыщаются солью. Нередко в таких огурцах кислотность снижается до 0,3–0,5%, а содержание соли повышается до 5–6%, к тому же огурцы утрачивают аромат и привкус специй, цвет их становится темным, грязнозеленым. Вследствие потери кислоты в огурцах обильно развиваются плесени, придающие им неприятный запах и приводящие в конечном результате к разложению плодовой ткани. Зачастую огурцы настолько теряют качество, что их приходится переводить в нестандартные.
Естественно, что кардинальным средством устранения этого нежелательного явления надо считать использование для засола огурцов только доброкачественной непротекающей тары. Но в вынужденных случаях доливки огурцов или замены полностью вытекшего рассола следует применять доброкачественный огуречный же рассол, оставшийся после реализации огурцов (что применимо главным образом в торговой сети), или специально приготовленный рассол.
Рассол, приготовленный для доливки огурцов, должен содержать молочную кислоту и соль в таких количествах, в каких они содержатся в огурцах нормального качества, т. е. кислоты 0,6— 0,9% и соли 3–4%.
При обнаружении в огурцах пониженной кислотности рассол надо готовить с таким содержанием кислоты, чтобы довести кислотность всей среды до 0,8–0,9%. Кроме того, в рассол желательно добавлять в растертом виде чеснок, сухой горький перец и свежий хрен по той же рецептуре, что и при засолке огурцов. Заливка огурцов таким рассолом поможет почти полностью сохранить их, не ухудшая качества.
Если добавление в рассол специй является желательным для сохранения ароматических и вкусовых достоинств огурцов и придания им большей стойкости в хранении, то составление рассола из двух главных компонентов — кислоты и соли — необходимо считать совершенно обязательным. Только такой рассол может компенсировать потерю основных консервантов и основных вкусовых веществ.
В случае отсутствия молочной кислоты ее следует заменять уксусной (0,5–0,6% в рассоле).
Б. С. Алеев и Ф. М. Чистяков рекомендуют при потере огурцами кислотности добавлять в рассол 1–2% сахара, что должно привести, по их мнению, к образованию кислоты. Это будет верным, очевидно, только для тех случаев, когда еще продолжается процесс ферментации (на льду до 60 дней) и молочнокислые бактерии не утратили своей активности. По окончании ферментации это мероприятие не всегда дает положительный эффект, как об этом свидетельствуют опыты И. М. Стовпивского1 на Нежинском засолочном заводе.
| {80} |
Вкус и запах соленых огурцов есть результат сложного взаимодействия веществ, содержащихся в свежих огурцах, специй и соли с веществами, образовавшимися в процессе брожения, — кислотами, спиртами, сложными эфирами и пр. Только сложное сочетание и взаимодействие всех перечисленных факторов может привести к получению приятного «букета», что так высоко ценится в огурцах.
При наличии в огурцах соответствующего набора специй решающую роль в формировании вкусовых ощущений будет играть содержание в них соли и кислоты и правильное их сочетание. Содержание, например, 5% соли и 0,6% кислоты делает огурцы неприятно солеными, ощущение кислого в них затушевывается резким ощущением соленого. Содержание 1,4% кислоты при наличии 3% соли вызывает резко кислое ощущение.
Наиболее гармоническое вкусовое ощущение вызывают огурцы, в которых отношение содержания соли к содержанию кислоты в процентах находится в пределах от 3 до 4. По аналогии с сахаро-кислотным коэффициентом, предложенным в свое время Ф. В. Церевитиновым для вкусовой оценки плодов, в огурцах это отношение можно назвать соле-кислотным коэффициентом.
Ввиду особенностей химического состава корнишонов и преимущественно их ферментации на льду они могут быть несколько острее огурцов всех остальных размеров, к чему привык потребитель. Поэтому в корнишонах даже при соле-кислотном коэффициенте, равном 2,4, вкусовое ощущение воспринимается как приятное. Огурцы с соле-кислотным коэффициентом ниже 2,4 воспринимаются как острокислые, с коэффициентом выше 4 до 6 — как излишне соленые и с коэффициентом свыше 6 до 8 — как резко-соленые.
Содержание кислоты и соли в огурцах можно регулировать и в технологии соления огурцов строго учитывать для получения продуктов высоких вкусовых достоинств.
Необходимо в стандарте и производственных инструкциях дифференцировать химические показатели по сортам.
Это легко осуществить, так как содержание соли в соленых огурцах разных сортов предусматривается рецептурами производственных инструкций, а наличие кислоты фиксируется многочисленными анализами разных производственных, заготовительных и торговых организаций.
Корнишоны, например, принято солить рассолами крепостью 6–7%, мелкие огурцы (до 90 мм) — крепостью 7–8%. При нормальном соотношении огурцов и рассола, равном 60: 40, содержание соли в этих огурцах, которые могут быть отнесены к высшему сорту по размерам, должно быть в пределах 2,4–3,2%.
Огурцы средние, размером от 91 до 120 мм, относящиеся к первому сорту, обычно засаливают 8%-ным рассолом, реже {81} 9%-ным. Если допустить возможность для этого сорта менее плотной укладки с содержанием в единице упаковки 55% плодов и 45% рассола, то в этих огурцах количество соли может быть максимум 4%. Минимум соли определяется по корнишонам, которые тоже могут быть отнесены к первому сорту. Таким образом, содержание соли в этом сорте допустимо от 2,4 до 4%.
Ко второму сорту стандарт относит огурцы крупные размером от 121 до 140 мм. Эти огурцы солят рассолами крепостью 8–10%. Даже при рыхлой укладке их в бочки с содержанием 45% рассола, при максимальной крепости рассола, соли в таких огурцах должно быть не более 4,5%. Поскольку во второй сорт могут быть отнесены и корнишоны, минимальное содержание соли должно быть ограничено 2,4%.
При установлении норм кислотности необходимо учитывать указанные выше сочетания соли и кислоты, вызывающие разные вкусовые ощущения. Естественно, что огурцы высшего сорта должны обладать наиболее высокими вкусовыми достоинствами и снижение их может быть допустимо по мере снижения сортности.
Нормальным было бы установление таких химических показателей по отдельным сортам:
Соль |
Кислота |
|||
Высший |
сорт |
. . |
2,4–3,2 |
0,8–1,0 |
Первый |
„ |
. . |
2,4–4,0 |
0,7–1,1 |
Второй |
„ |
. . |
2,4–4,5 |
0,6–1,2 |
Такое содержание кислоты наиболее типично для всех сортов и, кроме того, обеспечивает дифференциацию вкусовых достоинств при всех других равных условиях соления. Соле-кислотный коэффициент в огурцах высшего сорта колеблется в пределах от 2,4 до 4, в первом сорте — от 2,2 до 5,7 и во втором — от 2 до 7,5.
| {82} |
Глава десятая
Белокочанная капуста (Brassica oleraceae) является одной из самых старых и распространенных овощных культур.
Вследствие большого разнообразия в сроках созревания (с июня по октябрь включительно), легкости переработки и хорошей сохраняемости поздних сортов капусту издавна используют в кулинарии. Этому способствует наличие в ней до 2% азотистых веществ, 4–5% сахаров и 25–60 мг% витамина С, что характеризует ее как ценный пищевой продукт с высокой С-витаминной активностью.
Для квашения имеют значение такие хозяйственные признаки капусты: плотность кочанов, их вес и глубина вхождения кочерыги в кочан. Чем плотнее свит кочан, тем белее и нежнее внутренние листья. При очистке и механической резке плотных кочанов получается меньше отходов и более равномерная капустная стружка, чем при очистке и резке рыхлых кочанов. Крупные кочаны для производства более выгодны, чем мелкие, так как при очистке их получается меньше отходов и листовой массы в процентах к весу кочана в них больше. При глубине вхождения кочерыги до 1/3 высоты кочана отходы от удаления ее составляют 4–5%, при глубине вхождения до 2/3 — 8–9%. Кроме того, чем менее углублена кочерыга, тем меньше грубых листовых жилок и тоньше лист.
При квашении капусты имеет значение химический состав капусты. Особенно важно знать количество сахара, содержание которого желательно в пределах около 4% для накопления достаточного количества молочной кислоты и получения вкусного продукта. Роль азотистых веществ и, в частности, белков в квашении еще не изучена, но есть основания предполагать, что от содержания их в значительной мере зависит плотность структуры листовой ткани квашеной капусты.
По времени созревания наиболее пригодны для квашения сорта средние и поздние, так как они богаче ранней капусты сухими веществами и лучше по плотности листовой ткани.
В Советском Союзе выращивается много разных среднеспелых и позднеспелых хозяйственно-ботанических сортов капусты, {83} из которых одни являются общими почти для всей территории Союза, другие же имеют местное значение. Для квашения пригодны многие сорта. Из наиболее распространенных следует отметить славу — средних сроков созревания, брауншвейгскую и белорусскую — среднепоздних и амагер — поздних сроков созревания.
По важнейшим хозяйственным признакам эти сорта характеризуются такими данными (табл. 43):
|
ТАБЛИЦА 43
| |||||||||||||||||||||||||||
Средний вес капусты приведен по данным проф. Ф. В. Церевитинова, а глубина вхождения кочерыги — по П. А. Бычкову. Плотность и вес кочанов капусты изменяются в зависимости от климатических, почвенных условий и количества влаги при выращивании.
Исходя из приведенных данных, по совокупности всех хозяйственных признаков наиболее ценным сортом для квашения следует признать белорусскую, отличающуюся к тому же хорошо отбеленным листом. Второе место занимает слава, третье — брауншвейгская и четвертое — амагер. Амагер, хотя и отличается высокой плотностью, однако имеет много грубых листовых черешков, что снижает качество листовой стружки. Этот сорт занимает первое место по лежкости и наиболее пригоден для хранения.
По данным биохимической лаборатории ВИРа, содержание сахара и белков в капусте довольно значительно колеблется по годам, очевидно в зависимости от климатических условий, количества влаги и удобрения.
В табл. 44 приведены данные по содержанию сахара и белков в капусте указанных четырех сортов.
|
ТАБЛИЦА 44
| |||||||||||||||||||||||||||||
| {84} |
Средний химический состав капусты из Киевской области урожаев 1947, 1948 и 1949 гг. по нашим исследованиям показан в табл. 45 (средние данные за три года исследований).
|
ТАБЛИЦА 45 Химический состав свежей капусты
| |||||||||||||||||||||||||||||||||||||||||||
По данным ВИРа сорт капусты белорусская наиболее богат сахаром, на втором месте по содержанию сахара — брауншвейг-ская, затем амагер и на последнем — слава. В таком же порядке расположены сорта по содержанию сахара и в наших исследованиях. Больше всего витамина С (в среднем 51 мг%) содержит амагер, на втором месте — брауншвейгская (46,7 мг%) и на третьем — слава (44,1 мг%). В таком же порядке располагаются сорта и по содержанию азотистых веществ.
Удельный вес шинкованной капусты, ее сока и содержание в ней воздуха по отдельным сортам приведены в табл. 46 (средние данные за два года исследований).
|
ТАБЛИЦА 46
| ||||||||||||||||||
Чем меньше в капусте воздуха, тем меньше она изменяет свой объем при квашении, что необходимо признать положительным явлением. В этом отношении лучшими сортами являются амагер и брауншвейгская. Эти же сорта характеризуются и наибольшим удельным весом шинкованных листьев и сока.
В целом по химическому составу, физическим свойствам и хозяйственным признакам наиболее ценной для квашения следует признать белорусскую капусту, затем, в нисходящем порядке, брауншвейгскую, амагер и славу. {85}
Химический состав отдельных частей капусты неодинаков. Поданным Ф. В. Церевитинова, приведенным в табл. 47, наиболее богаты сухими веществами зеленые листья и кочерыга капусты. В них же содержится наибольшее количество безазотистых экстрактивных веществ, золы и клетчатки. По содержанию азотистых веществ на первом месте — белые внутренние листья.
Витамин С нарастает в капусте по мере углубления к центру кочана: меньше всего его в зеленых листьях, в белых — содержание его увеличивается, достигая максимума в кочерыге.
Та часть капусты, которая в основном используется для квашения — масса из белых листьев, наиболее богата азотистыми веществами и витамином С, вместе с тем она является и наиболее нежной, так как содержит наименьшее количество клетчатки.
|
ТАБЛИЦА 47
| ||||||||||||||||||||||||||||||||||||||||||||
По нашим исследованиям (см. табл. 48) отдельные части капустного кочана отличаются также по удельному весу и содержанию воздуха.
|
ТАБЛИЦА 48
|
Как видно и по этим показателям, белые листья более ценны для квашения, чем зеленые, так как их удельный вес выше и они содержат меньше воздуха. В кочерыге меньше воздуха, чем во всех остальных частях кочана, и удельный вес ее наиболее высокий.
| {86} |
Глава одиннадцатая
Подготовка капусты к квашению состоит из ряда производственных операций — очистки, шинковки, загрузки дошников, трамбовки, солки, пригнетания. Каждая из этих операций в зависимости от способа и условий проведения имеет значение для последующего процесса ферментации и влияет на качество квашеной капусты. В связи с этим заслуживает внимания изучение физико-химических изменений сырья в процессе его подготовки к квашению в зависимости от обусловливающих их факторов.
При очистке капусты снимают с кочанов облегающие их верхние зеленые листья и иногда вырезают кочерыгу. Нередки случаи, особенно при оборудовании цеха дошниками больших емкостей (10–30 т), когда для загрузки одного дошника накапливают очищенную капусту в течение двух-трех суток. Наши исследования свидетельствуют о том, что даже такое непродолжительное хранение очищенной капусты вызывает разрушение сахаров, азотистых веществ и витамина С в поверхностных слоях кочанов. В табл. 49 приведены данные о влиянии сроков хранения очищенной капусты на изменение ее химического состава.
|
ТАБЛИЦА 49
| |||||||||||||||||||||||||||||||||||||||||||||||||
Согласно приведенным данным, через 72 часа хранения в белых верхних листьях содержание сахара уменьшилось на 6,7%, азотистых веществ на 9,4% и витамина С на 2,7% первоначального их содержания. Гораздо интенсивнее разрушаются эти вещества в местах выреза кочерыги — там, где надрезана ткань. {87} Здесь через 72 часа сахара разрушилось 13%, азотистых веществ 7,8% и витамина С 24% первоначального содержания. Это настолько значительные разрушения, что игнорировать их ни в коем случае нельзя.
В этой же связи следует рассмотреть и другой вопрос, связанный с очисткой капусты. Работницы, очищая капусту сидя, зачастую придвигают к себе по соседству расположенные кочаны, натыкая их на нож, повреждая этим кочан на большую глубину. Естественно, что эти повреждения вызывают разрушение химического состава капусты. Есть и другой вид повреждений, связанный с очисткой капусты, — это потертости, раздавливание и разрыв листа очищенной капусты в корзинах. Экономя место, работницы складывают корзины с очищенной капустой одна на другую иногда в три-четыре ряда по высоте. Это вызывает не только указанные повреждения, но и загрязняет уже очищенную капусту.
В табл. 50 приведены данные анализов химического состава капусты в местах повреждений.
|
ТАБЛИЦА 50
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
В местах проколов через 72 часа разрушилось сахара 11,6%, азотистых веществ 12,5% и витамина С 12,3%. Почти в такой же мере азотистые вещества и сахар разрушаются в раздавленных и потертых листьях. Что же касается витамина С, то вследствие большой площади повреждения ткани в раздавленных листьях и, следовательно, большой возможности окисления разрушение его огромно: через 24 часа хранения содержание витамина С в поврежденных листьях уменьшилось на 28%, через 48 часов — на 36,5% и через 72 часа — на 60% исходного его количества.
Производственники должны сделать из приведенных фактов соответствующие выводы, которые напрашиваются сами собой: {88} очищенную капусту перерабатывать в день ее чистки, не допуская хранения, и при очистке избегать проколов и других повреждений кочанов.
Изучение вопроса о величине отходов в связи с очисткой капусты показало, что размер отходов обусловлен характером очистки (с высверливанием кочерыги или с оставлением ее), а затем величиной кочанов, их качеством и хозяйственно-ботаническим сортом.
В табл. 51 нами приведены средние данные большого количества опытов по изучению влияния веса и качества кочанов (без удаления кочерыги) на размер отходов.
|
ТАБЛИЦА 51
| |||||||||||||||||||||||||||||||||||||||||||||||||
При проведении опытов деление капусты на первый и второй сорта производилось в точном соответствии с требованиями стандарта. Как известно, основное отличие второго сорта от первого состоит в том, что в первом сорте кочаны должны быть плотные, а во втором — менее плотные, но не рыхлые. Данные приведенной таблицы показывают, что размер отходов в значительной мере обусловлен размером кочанов и затем качеством капусты и прежде всего плотностью кочана в капусте стандартного качества. При этом по мере уменьшения веса кочанов размер отходов возрастает прогрессивно. Так, уменьшение веса крупных кочанов на 0,5 кг вызывает увеличение отходов на 0,7%, средних — на 1% и мелких — на 1,7%.
Во втором сорте отходы на 0,5% выше, чем в первом, в кочанах одинакового веса.
Размеры отходов при очистке капусты нестандартного качества чрезвычайно разнообразны и зависят от степени повреждения кочанов и их рыхлости. Чем больше рыхлость кочана, тем больше и отходов. Наши исследования и практика работы перерабатывающих предприятий показывают, что отходы по нестандартной капусте могут колебаться в пределах от 10 до 30 и более процентов. {89}
При очистке капусты с высверливанием кочерыги отходы соответственно увеличиваются. В наших опытах при частичном высверливании кочерыги отходы колебались от 3,3 до 5,3%, составив в среднем из 24 опытов 4,5%. Эта группа отходов, как уже сказано выше, зависит от глубины вхождения кочерыги в кочан.
Следует отметить, что чем тоньше стружка капусты при шинковании, тем выше ее удельный вес. По нашим исследованиям полоски капусты шириной 25 мм имели удельный вес 0,868 при содержании воздуха 16,3 объемного процента, шириной 15 мм — соответственно 0,898 и 13,3 объемного процента и шириной 5 мм — 0,942 и 8,9 объемного процента. Объясняется это тем, что при измельчении капусты на шинковальных машинах происходит разрыв листовой ткани и уплотнение стружки за счет вытеснения воздуха, находящегося в листовой ткани. Чем значительнее измельчается ткань, тем больше выделяется из нее воздуха и тем она плотнее.
Из этого явления следует сделать полезный практический вывод, что при большем измельчении лучше будет использована емкость дошников.
Тонна утрамбованной капусты при измельчении ее на стружку в 25 мм шириной займет объем 1205 л, в 15 мм — 1165 л, и в 5 мм — 1110 л.
Иначе говоря, если объем нашинкованной и уложенной в дошники капусты, измельченной в стружку 5 мм шириной, принять за 100, то при измельчении капусты в стружку 15 мм шириной она займет объем на 5% и при резке в стружку 25 мм шириной — на 8,6% больший.
Нашинкованная капуста после закладки в дошники и трамбовки занимает несколько меньший объем вследствие перемешивания ее с солью и измельченной морковью. Фактический объем, занимаемый капустой в дошнике после трамбовки, приведен в табл. 52 (капусты — 94,5%, моркови — 3%, соли — 2,5%).
|
ТАБЛИЦА 52
| |||||||||||||||||||||||||||||
Как видно из приведенных данных, объем тонны капусты изменяется незначительно в зависимости от температуры загрузки {90} дошника и его емкости. Все же в больших дошниках под тяжестью собственной массы капуста укладывается плотней.
При загрузке капусты в дошники следует учитывать, что в первые дни брожения из нее выделяется огромное количество газов, разрыхляющих массу и выталкивающих на ее поверхность выделившийся сок. По нашим подсчетам каждый килограмм заложенной в дошники капусты выделяет за период ферментации до 8 л газов, из которых основное количество приходится на первые 3–4 дня брожения. Чем выше температура брожения, тем больше газов выделяется в первые дни брожения и, следовательно, тем более значительно расширяется объем капусты. Специально произведенными опытами и расчетами установлено, что объем всей бродящей массы в первые дни брожения увеличивается:
При |
температуре |
брожения |
21° |
на |
3,15% |
„ |
„ |
„ |
17° |
„ |
2,5% |
„ |
„ |
„ |
12,5° |
„ |
2,2% |
„ |
„ |
„ |
2° |
„ |
0% |
Это расширение объема капусты под влиянием выделяющихся газов приводит к тому, что при загрузке дошников капустой вровень с их краями происходит значительная потеря капустного сока.
На рис. 11 показано количество вытекшего через края дошников капустного сока в зависимости от температуры брожения.
 |
Рис. 11. Вытеснение капустного сока из дошников, заполненных в уровень с краями (в процентах к весу уложенного в дошники сырья) |
Несравненно большие потери сока происходят в тех случаях, когда капусту в дошники укладывают с «шапкой», т. е. когда дошник перегружается. В наших опытах из двух рядом стоящих пятнадцатитонных дошников вытекло сока через края дошника в первые три дня ферментации в процентах к весу заложенной капусты: {91}
из дошника, загруженного с «шапкой» высотой 25 см — 7,22%,
из дошника, загруженного вровень с краями — 2,44%.
Эти данные наглядно отражены на рис. 12.
 |
Рис. 12. Вытеснение капустного сока из дошников в первые три дня ферментации (в процентах к весу уложенного в дошники сырья) |
Потеря капустного сока, содержащего сахара и прочие растворимые вещества, обедняет капусту и, кроме того, составляет прямые, ничем не оправдываемые, весовые потери. Поэтому следует загрузку дошников производить с учетом расширения объема капусты в первые дни брожения при разных температурах, т. е. соответственно не догружать их доверху. И, конечно, необходимо отказаться от загрузки дошников с «шапкой», как рекомендуют очень многие авторы различных инструкций и пособий.
Кроме прямых весовых потерь от вытекания сока, укладка «шапки» или просто полная загрузка дошников приводит к ухудшению качества капусты.
В табл. 53 приведен химический состав верхнего слоя капусты из дошника, загруженного с «шапкой», в сравнении с верхним слоем капусты нормально загруженного дошника.
На качество квашеной капусты и на процесс ее ферментации влияет правильная посолка капусты при загрузке в дошники. В наших исследованиях мы обнаружили случаи получения «мраморной» капусты, в которой чередовались светлая капуста и с темными пятнами. Произведенными анализами было установлено, что «мраморность» капусты была вызвана неравномерной
| {92} |
ТАБЛИЦА 53
Уровень укладки капусты в дошник |
Содержание в верхнем слое капусты после ферментации (в %) |
||||
общего |
общей кислотности (на молочную) |
витамина С (мг%) |
свободно |
овершья |
|
С «шапкой» высотой 25 см, равной 10% от глубины чана |
0,28 |
1,26 |
27,5 |
10,7 |
0,78 |
В уровень с краями дошника (без «шапки»).......... |
1,64 |
1,28 |
33,0 |
11,9 |
— |
посолкой ее. В местах большого скопления соли капуста потемнела. Химическим анализом установлен такой состав светлых и темных частей капусты (табл. 54).
|
ТАБЛИЦА 54
| ||||||||||||||||||||||
Необходимо отметить, что по окончании ферментации такой капусты (в данном случае через 30 дней после загрузки чана) в темных слоях вследствие большого скопления соли (8,77%) сахар в большей своей части остался несброженным, а кислотность достигла всего 0,36%, в то время как в светлых слоях ее образовалось 1,45%.
Глава двенадцатая
Существующий способ квашения капусты в дошниках весьма своеобразен. Будучи одним из видов переработки, он не является, однако, чисто производственным процессом, а совмещает процессы производства и хранения. Вернее, это — хранение методом квашения, так как производственный процесс здесь не прекращается и постепенно переходит в процесс хранения, продолжающийся до {93} момента реализации. В течение всего периода нахождения в дошниках, продолжительностью от 10–15 до 250 дней, а в редких случаях и более, химический состав капусты непрерывно изменяется под влиянием микрофлоры и внешних условий. Естественно, что химический состав квашеной капусты, равно как и ее физические свойства и вкусовые достоинства, весьма непостоянен. Он находится в зависимости от химического состава сырья, температуры и влажности воздуха в период главного брожения (собственно ферментации) и в период хранения, технологии квашения, ухода за капустой, величины дошников, микрофлоры брожения и пр.
Основные изменения химического состава сырья происходят в период главного брожения, или ферментации капусты, после чего капуста приобретает свойства и качества готового продукта. Ферментация капусты проводится при разных температурных условиях, находящихся в большой зависимости от температуры наружного воздуха. Температура ферментации колеблется от 25–30 до 0°. В зависимости от температуры колеблется и продолжительность ферментации — от 5–10 до 60–90 дней. Наиболее типичной для осеннего времени следует считать ферментацию продолжительностью в 30 дней. Обычно ферментацию считают законченной, когда исчезают видимые признаки брожения — образование пены и выделение газов. К этому времени в большинстве случаев и кислотообразование в капусте достигает своего максимума.
В табл. 55 приведен химический состав квашеной капусты 30-дневной ферментации в сравнении со средним химическим составом сырья. Эти данные дают основание лишь для общей характеристики изменений химического состава, происшедших в сырье за период ферментации.
|
ТАБЛИЦА 55
| |||||||||||||||||||||||||||||||||||||||||
| {94} |
Изменения некоторых составных частей очень глубоки. В квашеной капусте осталась лишь незначительная часть сахара, всего 32,4% его содержания в сырье, а вместо него появилось 1,38% кислот, из которых 0,16% летучих, 0,35% спирта; прибавилась соль, уменьшилось на 18% содержание витамина С. Изменения азотистых и минеральных веществ сырья незначительны. Содержание сухих веществ в квашеной капусте уменьшилось по сравнению с исходным сырьем на 11,4%.
Как известно, химический состав квашеной капусты в некоторой степени зависит от условий ее ферментации и, прежде всего, температуры. Для характеристики влияния последнего фактора в табл. 56 приводим химический состав капусты, ферментация которой прошла при температуре 21, 11,5 и 5,8° и длилась, соответственно 15, 30 и 60 дней.
|
ТАБЛИЦА 56
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Как видно из данных табл. 56, ферментация при наиболее высокой температуре (21°) обеспечивает лучший химический состав квашеной капусты по сравнению с ферментацией при пониженных температурах. В этом случае в квашеной капусте больше остается сахара, лучше сохраняется витамин С, меньше накопляется летучих кислот и спирта. Лучшее качество квашеной капусты, ферментация которой проходила при 21°, достигнуто вследствие большей направленности молочнокислого брожения. Энергичное брожение обеспечило быстрое накопление кислоты и вызвало усиленное выделение углекислого газа, что затормозило некоторые побочные микробиологические процессы. Лучшие результаты квашения при повышенных температурах отмечают {95} также Я. Я. Никитинский и Б. С. Алеев, А. А. Колесник и многие другие исследователи.
Однако не всякое повышение температуры ферментации вызывает улучшение химического состава капусты. По ряду показателей капуста, бродившая при 11,5°, хуже капусты, ферментация которой проведена при 5,8°. В частности, в этой капусте образовалось наибольшее количество продуктов побочных брожений — спирта и летучих кислот, наименьшее количество молочной кислоты. Все это является свидетельством того, что при промежуточной температуре наиболее интенсивно развивались побочные брожения — спиртовое, уксуснокислое и пр.
В капусте, проходившей ферментацию при температуре в среднем 5,8°, побочные брожения тормозились низкой температурой, вследствие чего в ней обнаружено незначительное содержание летучих кислот и спирта и наибольшее количество молочной кислоты.
Сохранение витамина С, как и следовало ожидать, тесно связано с энергией брожения, определяемой температурой и связанной с ней быстротой кислотообразования. Поэтому по мере понижения температуры брожения содержание витамина С падает.
Квашение капусты в больших дошниках емкостью от 5 до 30 т, в которых капуста лежит слоем толщиной от 1,6 до 3,5 м, создает разные условия брожения в смысле доступа кислорода, влияния наружной температуры, относительной влажности воздуха, освещения, давления и пр. Если верхние слои лучше аэрируются и подвержены непосредственному воздействию внешних условий, то внутренние слои находятся в анаэробных условиях, насыщены углекислым газом и температура в них в процессе ферментации на 2–3° выше наружной. Все это приводит к тому, что в различных по глубине слоях процесс ферментации проходит по-разному, что обусловливает некоторые различия в химическом составе уже сферментированной капусты в разных слоях дошника.
На рис. 13 графически представлены колебания химического состава квашеной капусты в разных слоях в сравнении со средним составом этой же капусты, принятым за 100. Верхний, наиболее омываемый воздухом слей характеризуется наименьшим содержанием витамина С, сахара, кислоты и наибольшей концентрацией соли, что вполне закономерно. В верхних слоях происходит более энергичное сбраживание сахара, в котором принимают участие, кроме многочисленных бактерий, пленчатые дрожжи и другие микроорганизмы. Вследствие развития поверхностной пленки, состоящей в основном из потребителей молочной кислоты, в этом слое кислотность понижена. Повышение концентрации соли вызвано испарением влаги и, обычно, концентрация соли тем выше, чем более дефицит влажности воздуха в квасильном цехе. В более глубоких слоях у квашеной капусты иной химический состав. При глубине дошника в 200 см наибольшее содержание сахара наблюдается на глубине 50 см от поверхности и затем
| {96} |
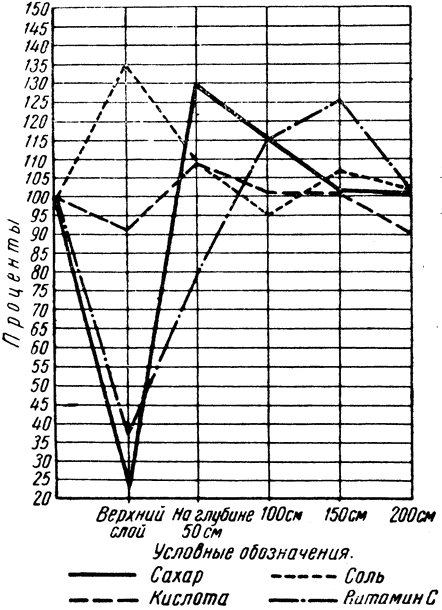 |
Рис. 13. Колебания химического состава |
постепенно падает по глубине, доходя до среднего содержания у дна дошника. Кислотность достигает максимума тоже в слое глубиной в 50 см и затем постепенно снижается, падая в самом нижнем слое ниже уровня среднего содержания. Содержание витамина С по мере углубления все время возрастает и лишь в самом нижнем слое у дна падает до уровня среднего содержания. Такое различие химического состава на разных глубинах и, в частности, у дна дошника вызвано, кроме указанных выше условий, еще и тем, что в самом нижнем слое дошника обычно скопляется капустный рассол; в этом слое наиболее высокое давление и наибольшая концентрация газов.
Таким образом, верхний слой капусты или сока в дошнике никогда не отражает действительного ее среднего качества.
В герметически закрытой посуде брожение капусты проходит несколько иначе, чем в открытой, что сказывается на химическом составе квашеной капусты. Мы изучали закрытое брожение в лабораторных и производственных условиях. В лаборатории капусту заквашивали в 3-килограммовых банках, из которых 50% герметически закупоривали и периодически удаляли из них излишек газов. На производстве из двух рядом стоящих выделенных для опыта 15-тонных дошников один тщательно герметировался с отводом газов через резиновые трубки в воду. {97}
Спустя 60 дней, по окончании ферментации, проходившей при 7° в среднем, был произведен химический анализ капусты, заквашенной в банках. Данные анализа (в %) приведены в табл. 57.
|
ТАБЛИЦА 57
| ||||||||||||||||||||||||||||||||||||||||||||||
Сравнение этих данных указывает на преимущества закрытого брожения. И действительно, даже при несколько большем накоплении кислоты в капусте закрытого брожения в ней больше сохранилось сахара и остальных сухих веществ, лучше сохранился витамин С, меньше образовалось летучих кислот и спирта.
В производственных условиях мы наблюдали аналогичное явление, за исключением содержания спирта, которого оказалось больше в капусте закрытого брожения. Но производственная проверка эффективности закрытого брожения показала еще ряд его преимуществ. Ферментация капусты в дошниках продолжалась 55 дней при средней температуре 7,4°. Изменение химического состава сырья при открытом и закрытом брожении приведено в табл. 58.
ТАБЛИЦА 58
Изменения за период ферментации |
В открытых |
В герметично |
Испарилось влаги (в % от веса загруженного сырья)............... |
2,17 |
0,08 |
Безвозвратно потеряно сухих веществ (в % от веса загруженного сырья)........ |
1,63 |
1,36 |
Израсходовано сахара (в % от первоначального его содержания)........... |
75,9 |
62,3 |
Накопилось молочной кислоты (в %) . . . . |
1,17 |
1,20 |
Накопилось спирта (в %)........ |
0,32 |
0,58 |
Накопилось летучих кислот (в %)..... |
0,22 |
0,18 |
Содержание витамина С (в мг%)...... |
31,4 |
36,5 |
Кроме отмеченного уже большого накопления кислоты, лучшего сохранения сухих веществ, в частности сахара, витамина С {98} и меньшего образования летучих кислот следует отметить ничтожную потерю влаги в закрытом дошнике. Потеря эта составила всего 0,08%, тогда как в открытом дошнике она достигла 2,17%.
Изменения отдельных веществ капусты в процессе ферментации находятся в тесной зависимости от температуры брожения. Последняя определяет энергию брожения, а также скорость кислотообразования и накопления газов в бродящей массе.
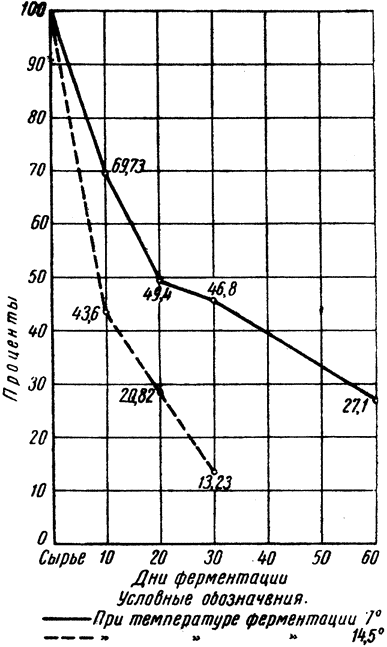 |
Рис. 14. Содержание общего количества сахара в капусте в разные периоды процесса ферментации |
Об изменении содержания сахара капусты в процессе ферментации при температурах 7 и 14,5° можно судить по кривым, представленным на рис. 14. При 14,5° ферментация проходила более энергично и закончилась в 30 дней, при 7° она затянулась до 60. Несмотря на более продолжительное время, израсходовано сахара на брожение (в процентах к исходному содержанию) на 14% меньше, чем за 30 дней брожения при 14,5°.
Следует отметить, что при разных температурах брожения расход сахара неодинаково эффективен, так как не сопровождается эквивалентным ему накоплением молочной кислоты.
Молочная кислота накапливается более энергично при повышенных температурах. Это общеизвестное явление отмечено всеми микробиологами и специальными исследователями в области соления и квашения овощей — Я. Я. Никитинским и Б. С. Алеевым, П. Г. Шугаевской, А. А. Колесником и др. На рис. 15 показана зависимость скорости кислотообразования от температуры брожения.
Накопление кислоты до 0,7%, т. е. минимального предела для квашеной капусты, происходит при 21° — на 5-й день, при 11,5°—
| {99} |
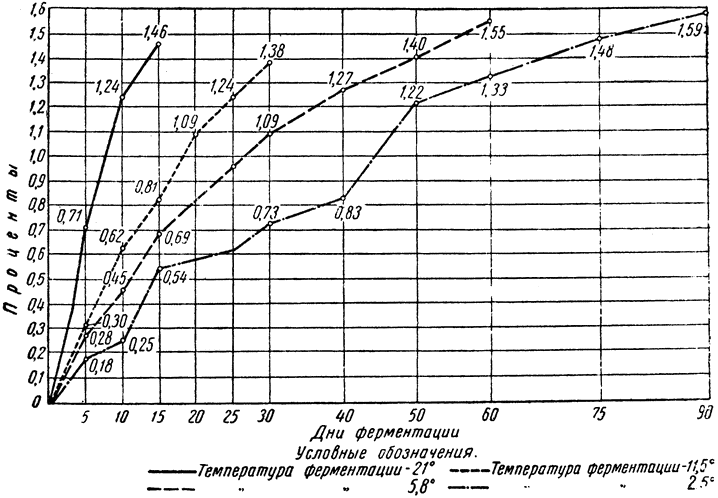 |
Рис. 15. Скорость кислотообразования в капусте при разных температурах ферментации |
между 10-м и 15-м днями, при 5,8° — между 15-м и 20-м и при 2,5° — только на 30-й день брожения. Максимум же кислотности и конец брожения достигнут при 21° на 15-й день, при 11,5° — на 30-й, при 5,8° — на 60-й и при 2,5° — на 90-й день. Следует здесь отметить, что максимальное содержание кислоты к концу брожения накапливается при наиболее высоких и низких температурах, т. е. при 21 и при 2,5–5,8°. При средних температурах брожения наблюдается наименьшее накопление кислоты к концу ферментации, вследствие обильного развития потребителей кислоты и побочных процессов брожения.
Эти наблюдения дают возможность ориентировочно определить время, необходимое для приготовления квашеной капусты. Совершенно необязательно и даже нежелательно для получения продукта высоких вкусовых достоинств доводить брожение до конца. Как показывает практика, наивысшую оценку у потребителя получает капуста с кислотностью 0,7–1,0% и наличием в ней несброженных сахаров. Так как при 21° брожения 0,7% кислоты накапливается уже на 5-й день, то, следовательно, продолжительность изготовления квашеной капусты при такой кислотности может ограничиться пятью днями. Это очень существенно для производства, так как дает возможность значительно повысить производительность предприятий, если имеются помещения для хранения квашеной капусты при низких температурах.
Рассматривая вопросы кислотообразования, мы должны отметить разные темпы накопления кислоты при высоких и низких {100} температурах в верхних слоях капусты и в глубине дошников (в %) (см. табл. 59).
|
ТАБЛИЦА 59
| |||||||||||||||||||||||||||||||||||||||
В то время как при 21° в верхнем слое капусты кислотообразование проходит энергичнее, чем во внутренних слоях в течение всего периода ферментации, при 5,8° это характерно только для первых 15 дней, а в дальнейшем во внутренних слоях капусты накапливается кислоты больше, чем в верхних. Это объясняется тем, что в первые 15 дней более интенсивного брожения выделяющиеся на поверхности капусты газы, скопляясь в значительных количествах, препятствуют развитию потребителей кислоты и благоприятствуют развитию молочнокислых бактерий. Но условия эти меняются по окончании первого периода наиболее бурного брожения. В верхнем слое развиваются потребители молочной кислоты, которые непрерывно снижают ее концентрацию. В этот период больше всего накапливается кислоты в глубинных слоях, не доступных для образования пленки.
Иначе проходит процесс кислотообразования при закрытом брожении. В наших лабораторных опытах изучалось накопление кислоты в герметически закрытых банках в течение 180 дней. Параллельно шло изучение кислотообразования в той же капусте, заквашенной в открытых банках. На рис. 16 кривые с достаточной показательностью характеризуют эффект кислотообразования при закрытом и открытом брожении. До 60-го дня накопление кислоты в закрытых и открытых банках шло почти одинаковыми темпами, лишь несколько быстрее в закрытых банках.
На 90-й день темпы кислотообразования в закрытых банках уже значительно выше, чем в открытых. На 120-й день содержание кислоты в открытых банках начало снижаться и к 150-му снизилось до 0,87%. Вследствие большого развития пленки и утраты качества капусты хранение ее в открытых банках пришлось прекратить. В закрытых же банках, начиная с 90-го дня и до 180-го, темпы кислотообразования повысились, и к концу хранения кислотность капусты поднялась до 2,12%. Развития поверхностной пленки не наблюдалось. Подобный же эффект достигнут нами в производственных условиях.
| {101} |
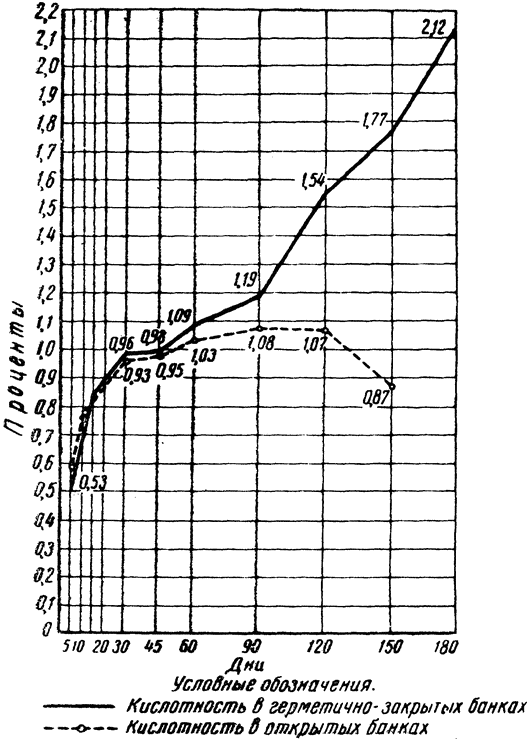 |
Рис. 16. Содержание общей кислотности в квашеной капусте |
С производственной точки зрения представляет значительный интерес влияние температуры и обусловливаемой ею продолжительности ферментации на образование в капусте продуктов
|
ТАБЛИЦА 60
| ||||||||||||||||||||||||||||||||||
| {102} |
побочных брожений — спирта и летучих кислот. В табл. 60 приведены соответствующие данные наших исследований.
Эти данные показывают, что наиболее эффективными температурами брожения в смысле наименьшего развития побочных брожений являются наивысшая (21°) и наинизшая (5,8°). При этих температурах образуется минимальное количество спирта и летучих кислот.
Содержание витамина С в капусте при ферментации изменяется в зависимости от продолжительности ее и емкости тары. При средней температуре ферментации 7° наиболее значительное разрушение витамина С происходит в первые пять дней брожения, что вызвано незначительным содержанием молочной кислоты в этот период. По мере накопления молочной кислоты разрушение витамина С замедляется. К концу ферментации — через 60 дней — витамина С в капусте, заквашенной в мелких дошниках, осталось 57% исходного его содержания в сырье.
Витамин С в квашеной капусте лучше сохраняется при энергичном брожении и в более крупных дошниках.
В табл. 61 показана зависимость сохранения витамина С от продолжительности ферментации и емкости дошников. Общая
|
ТАБЛИЦА 61
| ||||||||||||||||||||||||||||||||||||||||||||||||||
тенденция в дошниках одинаковой емкости (15-тонных) вполне закономерна: по мере снижения температуры брожения, а следовательно, увеличения его продолжительности, снижается содержание витамина С к концу брожения. Здесь обнаружена, как и в других случаях, прямая зависимость от энергии кислотообразования, которая с понижением температуры брожения снижается. Конечное содержание витамина С в квашеной капусте зависит также от размера поверхности дошника на 1 т капусты. Как известно, чем крупнее дошник, тем меньше его поверхности приходится на единицу емкости, и наоборот, с уменьшением емкости (при одних и тех же формах) увеличивается размер поверхности на единицу емкости. По данным табл. 61 на тонну емкости 15-тонных {103} дошников приходится 0,35 м2 поверхности, 3-тонных дошников — 0,69 м2 и 1,5-тонных — 0,75 м2. Увеличение относительной поверхности дошника, улучшающее условия аэрации продукта, отрицательно сказывается на сохранении витамина С. Несмотря на то, что при 15- и 20-дневной продолжительности ферментации энергия кислотообразования выше, чем при 25-дневной, витамин С в наших опытах при наиболее высокой температуре сохранялся хуже, так как брожение проводилось в малых дошниках с большой относительной поверхностью. И чем больше относительная поверхность и, следовательно, лучше условия аэрации, тем хуже сохранялся витамин С. Все же необходимо отметить высокое сохранение витамина С при продолжительности ферментации от 15 до 30 дней — от 89,3 до 95,5% исходного содержания в сырье. В крупных же дошниках сравнительно хорошо сохранился витамин С и при более продолжительной ферментации. Даже при 60-дневной ферментации в квашеной капусте сохранилось 76,2% исходного содержания витамина.
Рассматривая изменения химического состава капусты в процессе ферментации, следует остановиться на некоторых показателях, характеризующих направленность ферментативного процесса. Как уже было выше отмечено, энергичное брожение при повышенных температурах наиболее эффективно, так как приводит к быстрому кислотообразованию, лучшему подавлению всех сопутствующих микробиологических процессов и хорошему сохранению С-витаминной активности квашеной капусты. Однако направленность процесса брожения и его химическая эффективность становятся наиболее наглядными, если сравнить коэффициенты кислотообразования при разных температурах брожения. Коэффициентами кислотообразования мы называем количество весовых единиц сухих веществ и сахара, затраченных на одну такую же весовую единицу образовавшейся кислоты. Таким образом, следует различать коэффициент кислотообразования по сахару и по сухим веществам.
В табл. 62 приведены вычисленные нами коэффициенты кислотообразования при разных температурах ферментации капусты в производственных условиях. Эти показатели, являющиеся итоговым выражением суммы всех микробиологических процессов, наиболее верно характеризуют чистоту брожения. В то время как при 21° на образование единицы кислоты израсходовано 1,06 единицы сухих веществ и 1,92 сахара, при 15° коэффициенты кислотообразования возросли соответственно до 1,8 и 2,45, что свидетельствует о значительном развитии побочных процессов при этой температуре.
| {104} |
|
ТАБЛИЦА 62
| ||||||||||||||||||||||||||||||||||||||||||||||
В дальнейшем, по мере снижения температуры брожения снижаются и коэффициенты кислотообразования, характеризующие понижение активности сопутствующих микробиологических процессов. Все же, даже при самой низкой температуре ферментации, 5,8°, химическая эффективность ниже, чем при 21°. В этом случае расход сухих веществ на единицу кислоты такой же, как и при 21°, а расход сахара значительно выше. Таким образом, коэффициенты кислотообразования подтверждают, что ферментация капусты при повышенных температурах проходит наиболее эффективно.
Данные табл. 62 дают возможность сделать и другой вывод, а именно: расход сахара на единицу образовавшейся кислоты выше общего расхода сухих веществ. Это свидетельствует о том, что не весь израсходованный в процессе брожения сахар составляет прямые издержки брожения, а часть его в виде промежуточных продуктов сложного процесса превращения в молочную кислоту или спирт сохраняется в квашеной капусте. Издержки брожения могут характеризовать только безвозвратные потери сухих веществ.
Коэффициенты кислотообразования подтверждают преимущества закрытого брожения в сравнении с открытым. В табл. 63 показан расход сахара на единицу кислоты в разные периоды
|
ТАБЛИЦА 63
| |||||||||||||||||||||||||||||||||||||||||||||||||
| {105} |
ферментации и хранения квашеной капусты закрытого и открытого брожения в наших лабораторных опытах. В течение всего периода ферментации и хранения при закрытом брожении сахар более эффективно расходовался на образование кислоты. Но после 90-го дня накопление кислоты в открытых сосудах закончилось, достигнув 1,08%, и вследствие развития потребителей кислоты на поверхности сосудов содержание ее стало резко снижаться. В то же время в закрытых сосудах окончательно или в более значительной мере были подавлены все побочные микробиологические процессы, темпы кислотообразования повысились, и на 150-й день содержание кислоты поднялось до 1,77%. Расход сахара на единицу кислоты достиг на 150-й день в закрытых сосудах 2,38, а в открытых на 90-й день — 3,19.
Таким образом, закрытое брожение обеспечивает не только большую чистоту брожения, но и способствует лучшему сохранению продукта по окончании основного брожения.
Глава тринадцатая
Под влиянием соли, химических процессов брожения и физического воздействия на капусту, вызываемого ее измельчением и пригнетанием, первоначальные физические свойства ее во время ферментации значительно изменяются. Капуста выделяет сок, вытесняется из тканей воздух, вследствие чего происходит уплотнение ткани и увеличение ее удельного веса, испаряется влага и теряются сухие вещества, меняется объемный и абсолютный вес, консистенция и пр.
Наиболее полное изучение происходящих при квашении капусты физических изменений представляет интерес, прежде всего, с точки зрения производственно-практической, так как помогает вскрыть факторы, обусловливающие те или иные изменения и их закономерности. А знание их дает возможность более активно воздействовать на производственный процесс и, в конечном итоге, на качество продукта производства.
Как мы уже отмечали выше, измельчение капусты приводит к увеличению удельного веса ее частиц. В дальнейшем, при ферментации, удельный вес их, как это видно из данных табл. 64, увеличивается с 0,947 до 1,0404 к концу ферментации. Увеличение удельного веса капусты не вызывается увеличением содержания сухих веществ. Наоборот, если говорить о растворимых веществах, количество их в капусте несколько снижается, на что указывает небольшое уменьшение удельного веса капустного сока. В процессе ферментации капустная ткань теряет сухих веществ больше, {106} чем приобретает. Увеличение удельного веса измельченной капустной ткани происходит за счет вытеснения из нее воздуха. Наиболее резкая потеря воздуха тканью происходит в первые дни ферментации, под влиянием большого давления в период выделения сока. При 30-дневной продолжительности ферментации уже на 15-й день воздуха в тканях практически не содержится.
|
ТАБЛИЦА 64
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Но в капусте, уложенной в дошник, кроме содержащегося в тканях воздуха, некоторое количество его остается между частицами капусты, несмотря на трамбовку и пригнетание, причем содержание его зависит от степени трамбовки и силы пригнетания.
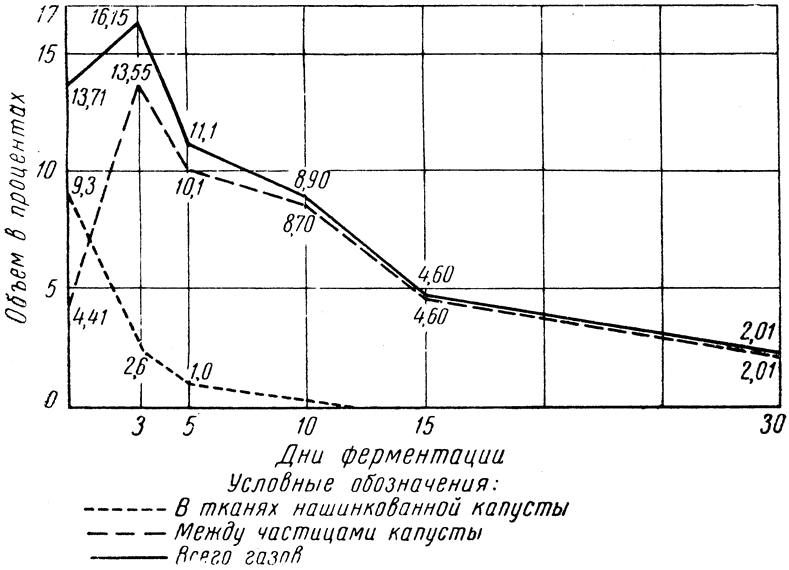 |
Рис. 17. Содержание воздуха и других газов в капусте в процессе ферментации |
| {107} |
В процессе брожения, сопровождающегося вначале бурным выделением углекислого и других газов, общее количество газов между частицами капусты в первые дни брожения увеличивается. На рис. 17 показана динамика газов в капусте в период ферментации (в объемных процентах). В то время как содержание воздуха в тканях постепенно снижается, содержание газов между частицами капусты в первые три дня резко увеличивается — на 9,14%, что вызывает и общее увеличение газов в капусте. Однако в дальнейшем, по мере того как процесс брожения приобретает большую направленность и темпы кислотообразования несколько снижаются, содержание газов между частицами капусты и в целом уменьшается. Это происходит вследствие того, что с уменьшением темпов кислотообразования снижается и количество выделяющихся в единицу времени газов, следовательно понижается внутреннее давление их. Под влиянием внешнего давления пресса и всей массы капусты образующиеся газы постепенно вытесняются из дошника. Уже на 5-й день брожения общее количество газов в капусте меньше начального (11,1 против 13,71%). К концу ферментации — на 30-й день — содержание газов падает до 2,01%, незначительно снижаясь в процессе длительного хранения.
Изменение содержания газов в капустной массе вызывает изменение ее объема. Вначале вследствие бурного выделения газов и создаваемого ими внутреннего давления над подгнетным кругом увеличивается количество капустного сока, выталкиваемого газами изнутри дошника, и объем всей бродящей массы увеличивается. В последующие дни после выхода газов наружу и понижения внутреннего давления количество сока над подгнетным кругом постепенно убывает и, если его было в начале брожения немного, он исчезает совсем, замещая внутри дошника вытесненные газы.
Для точного определения изменений объема капусты в процессе ферментации нами были поставлены специальные опыты квашения капусты в стеклянных банках. Результаты опытов приведены в виде кривых на рис. 18. Изменение объема капусты в открытых банках при разных температурах брожения (18–20° и 6–8°) носит одинаковый характер. При более высокой температуре брожения в первые дни объем капусты увеличивается до 4%, в то время как при низкой (6–8°) — всего на 1,4%. Такое различие в увеличении объема капусты в первые дни брожения вполне естественно, если учесть, что при более высокой температуре брожение происходит более энергично и, следовательно, в единицу времени выделяется больше газов. В конечном счете на 30-й день ферментации объем квашеной капусты, бродившей в одной банке при 18–20°, в другой при 6–8°, почти уравнялся, достигнув примерно 86% первоначального.
Такой же характер имеют изменения объема капусты и при закрытом брожении, однако здесь увеличение объема в первые дни брожения более значительно. При 18–20° максимальное
| {108} |
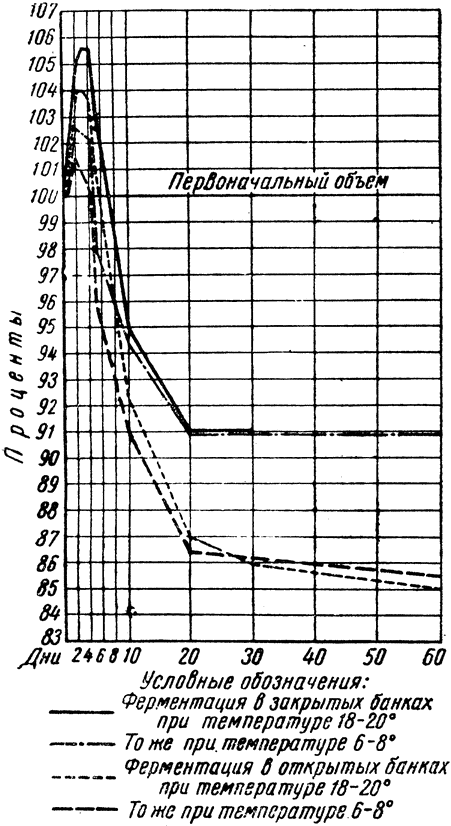 |
Рис. 18. Изменение объема капусты в процессе ферментации |
увеличение объема достигло 5,6% и при 6–8° — 2,7%. Большее увеличение объема при закрытом брожении вызвано тем, что здесь не было свободного выхода газов, их удаляли из сосудов периодически. Это обстоятельство вызвало повышение внутреннего давления газов в капустной массе и большее выталкивание ими на поверхность капустного сока. Но, если характер кривых изменения объема при открытом и закрытом брожении примерно одинаков, окончательное уменьшение объема при закрытом брожении не доходит до тех пределов, которые наблюдаются при открытом брожении. На 30-й день ферментации объем квашеной капусты в закрытых сосудах составил 91% первоначального, т. е. примерно был на 5% выше объема в открытых сосудах. Произошло это вследствие того, что из открытых сосудов не только удалялись {109} газы, но и испарялась вода из капустного сока, а в закрытых сосудах испарения влаги почти не было.
Каково влияние испарения влаги и других факторов на уменьшение объема капусты в процессе ферментации в открытых дошниках, видно из данных по нашим опытам производственного квашения капусты, приведенных в табл. 65. Уменьшение объема капусты вследствие испарения влаги составляет от 2,13 до 4,78% и тем больше, чем выше температура ферментации. Количеством испарившейся влаги и определяется разница в уменьшении объема капусты, бродившей при разных температурах, что видно из сопоставления данных, приведенных в табл. 65. Когда ферментация
|
ТАБЛИЦА 65
| |||||||||||||||||||||||||||||||||||||||||||||
капусты протекала при 21°, объем ее уменьшился на 17,29 %, а при 8,5° — на 14,96%. При ферментации, проведенной при 21°, сокращение объема капусты было на 2,33% больше, чем при 8,5°, но в первом случае влаги испарилось на 2,65% больше. Потеря сухих веществ влияет на изменение объема капусты незначительно.
К вопросам большой практической важности следует отнести величину выделяемого при брожении капусты сока.
Она зависит от структурных факторов, обусловленных особенностями самого продукта, и внешних, привносимых в процессе производства.
Из структурных факторов несомненное значение имеют коллоиды, которые обладают большой влагоудерживающей способностью и способностью набухать под действием кислот. Из азотистых веществ в этом отношении существенно содержание в капусте белков.
К сожалению, состав азотистых веществ отдельных хозяйственно-ботанических сортов капусты еще недостаточно изучен.
По данным исследований опытной станции Московского института народного хозяйства им. Плеханова, белокочанная капуста (без названия сорта) в одном случае содержала азотистых веществ 1,59% и из них белков — 1,10%, а в другом — 1,06%, в том числе белков — 0,60%. В первом случае белковые вещества {110} составляли 70% общего количества азотистых, а во втором случае — 56,6. По исследованиям М. И. Богомоловой, белокочанная капуста (без указания сорта) содержала протеинового азота 53,56% от его общего количества. Очевидно, во всех этих случаях исследовались разные сорта капусты, из чего следует сделать заключение, что содержание белков в разных сортах колеблется от 0,6 до 1,1%. Такая значительная разница в содержании белков может существенно отразиться на процессе квашения капусты.
В наших исследованиях установлена такая связь между содержанием азотистых веществ в капусте и количеством выделившегося при брожении сока (см. табл. 66).
|
ТАБЛИЦА 66
| |||||||||||||||||||||||
Из данных табл. 66 следует, что чем больше в капусте азотистых веществ и чем меньше влаги приходится на каждую их единицу, тем меньше сока выделяет капуста при квашении и тем, следовательно, больше удерживает его в тканях. Возможно, что незначительным содержанием белков в первую очередь и вызывается большое соковыделение у некоторых сортов капусты, замеченное производственниками.
Из внешних факторов, влияющих на отдачу сока капустной тканью, следует отметить внесение соли, температуру ферментации, силу гнета и количество пригнетаний.
Влияние соли на соковыделение общеизвестно. Несомненно, что увеличение содержания соли способствует увеличению и соковыделения. При этом влияние соли двоякое. Во-первых, она вызывает диффузию сока из тканей и тем в большей мере, чем выше ее концентрация. Во-вторых, по мнению академика Думанского (23), она умеряет набухание коллоидов под влиянием кислот.
В наших производственных опытах получено разное количество свободно стекаемого сока при квашении капусты в различных температурных условиях. Так, в августе, при средней температуре ферментации в 21° свободного сока в капусте образовалось 13,9%, в сентябре (средняя температура 10–15°) — 11,1–11,3% и в октябре — ноябре (температура 5–8°) — 9,2–10,5%. Поскольку при квашении использовались разные хозяйственно-ботанические {111} сорта, на образование сока оказали свое влияние особенности сортов, но, очевидно, известное действие оказала температура, силу действия которой нам не удалось установить. Возможно, действие повышенных температур ограничивалось только известным уже ускорением диффузии сока, опережающим процесс набухания коллоидов под влиянием образующихся кислот. Специально поставленными опытами при квашении капусты в дошниках нам удалось установить, что многократное пригнетание капусты вызывает дополнительное выделение сока. Приводим соответствующие данные:
Содержание |
Количество |
|
1 | 11,2 | |
2 | 11,9 | |
3 | 12,7 | |
6 | 13,2 | |
10 | 14,1 |
Обычно по окончании ферментации, сопровождающейся удалением газов из толщи капусты, сок с поверхности и верхних слоев устремляется вниз и сосредоточивается в основной своей массе у дна дошника. Повторное (более сильное) пригнетание не вызывает подъема сока со дна дошника, а приводит к отжатию его из верхних слоев капусты.
Чем чаще и сильнее повторные пригнетания с целью вызвать сок на поверхность капусты, тем больше отжимается его из верхних слоев. При многократном пригнетаний, несмотря на испарение, свободно стекаемого сока образуется значительно больше, чем при одно- и двухразовом пригнетаний. В производственной практике это следует учесть, так как получение излишнего сока не только ведет к прямым потерям, но и, обезвоживая капусту, ухудшает ее качество.
Основной вид молочнокислых бактерий при квашении капусты — В. brassicae fermentati — газообразующий. Вследствие этого чистое молочнокислое брожение сопровождается безвозвратной потерей сухих веществ (главным образом сахара) в виде выделяющихся газов. Но если образование молочной кислоты из сахара происходит с выделением газов, то в несравненно большей мере выделяется газов при всех сопутствующих брожениях, вызываемых дрожжами, маслянокислыми, уксуснокислыми бактериями и бактериями группы coli aerogenes. Чем больше развиваются во время ферментации капусты все эти побочные брожения, тем выше безвозвратные потери сухих веществ.
В результате брожения в капусте накапливается молочная кислота в пределах от 1 до 2% (чаще всего около 1,5%) и 0,5% {112} спирта и летучих кислот. В среднем взамен сбродившего сахара образуется около 2–2,5% новых веществ. В свежей капусте содержится сахаров 4–5%. При условии полного сбраживания всех сахаров безвозвратные потери сухих веществ составили бы разницу между количеством сброженных сахаров и образовавшихся новых продуктов брожения, т. е. 2–3%. Однако, как мы уже говорили выше, фактические потери сухих веществ всегда несколько меньше потерь сахаров, что свидетельствует об образовании в квашеной капусте каких-то промежуточных продуктов брожения, не обнаруживаемых анализами на содержание сахара, кислот и спирта. Следовательно, рассуждая теоретически, фактические потери сухих веществ при ферментации в среднем должны быть несколько меньше 2–3%.
Стремясь точно изучить фактические потери веществ, мы, экспериментируя в производственных условиях, точно взвешивали закладываемое в дошники сырье и производили химический анализ. По окончании ферментации выгружаемую из дошников квашеную капусту вновь взвешивали и производили анализ ее химического состава. Вычисляя по общему весу сырья и квашеной капусты абсолютные количества составных частей на основании химических анализов, мы имели возможность по каждому в отдельности дошнику составить баланс всех составных частей в отдельности и в общей сумме. В течение трех лет на трех предприятиях были поставлены опыты по квашению. Всего было заквашено около 470 т капусты в 58 дошниках емкостью 1,5, 2,5, 3, 5, 10 и 15 т. Проведение опытов с большими количествами давало возможность более точно определять динамику сухих веществ в процессе ферментации. Соответствующие средние данные опытов приведены в табл. 67.
|
ТАБЛИЦА 67
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Эти данные полностью подтверждают теоретические предположения: фактические потери сухих веществ колеблются в пределах от 1,55 до 2,59% при расходе сахара от 2,81 до 3,53%. Средняя разница между потерей сухих веществ и расходом сахара {113} колеблется в зависимости от температуры и продолжительности брожения от 0,94 до 1,76%.
Наименьшее количество сухих веществ потеряно при температуре брожения 21° — 1,55%, и наибольшее — 2,59% — при температуре 15°. По мере снижения температуры (ниже 15°) абсолютные потери уменьшаются, но даже при наиболее низкой температуре (5,8°) они все же несколько выше, чем при 21°.
Это явление вполне закономерно, если учесть, что при наиболее высоких и самых низких температурах брожение проходит более направленно, как это нами отмечено выше. Направленность ферментативного процесса при разных температурах характеризуется также накоплением побочных продуктов брожения и молочной кислоты.
Каждой температуре брожения свойственна характерная для нее безвозвратная потеря сухих веществ на единицу образовавшейся кислоты. Соответствующие коэффициенты нами приведены выше, в табл. 62. Если известны кислотность квашеной капусты по окончании ферментации, средняя температура за период брожения, то можно, пользуясь приведенными коэффициентами, произвести ориентировочный расчет безвозвратных потерь сухих веществ. Обозначив кислотность квашеной капусты по окончании ферментации через n и коэффициент кислотообразования (он же в данном случае является коэффициентом потери сухих веществ) через f, получим, что b = nf, где b — потеря сухих веществ в процентах к весу загруженного в дошники сырья.
Анализ динамики сухих веществ дает возможность сделать вывод, что квашение капусты при более высоких температурах (21–23°) вследствие большой направленности процесса брожения приводит к уменьшению безвозвратных потерь.
Безвозвратные потери сухих веществ сокращаются при закрытом брожении. В наших опытах квашения капусты в открытых дошниках потери составили 1,63%, а в закрытых — 1,36% при температуре брожения 8–10°. Опытное квашение в лабораторных условиях (в банках) привело к более резкой разнице в потере сухих веществ. Они составили за 60-дневный срок ферментации «в открытых банках 2,01, а в закрытых — всего 0,74%. Это свидетельствует о том, что при лучшей герметизации производственной посуды (дошников) потери сухих веществ могут быть значительно сокращены за счет опять-таки большей направленности молочнокислого брожения.
Основные потери при ферментации капусты в открытых дошниках вызываются испарением влаги с поверхности капустного сока. Эти потери подчиняются общим закономерностям испарения с учетом всей специфики обстановки и испаряющейся жидкости. {114}
Скорость испарения влаги с поверхности, т. е. количество испаряющейся жидкости в килограммах с одного квадратного метра поверхности в час, зависит главным образом от температуры, относительной влажности воздуха, скорости движения его, формы и размеров сосудов, природы жидкости и некоторых других факторов.
Для расчетов скорости испарения влаги со свободной поверхности предложено много теоретических и эмпирических формул, но все они построены на законе Дальтона, установившего прямую пропорциональность скорости испарения влаги дефициту влажности и скорости движения воздуха.
Под дефицитом влажности понимают разность между упругостью насыщающих паров при температуре поверхности воды и действительным содержанием пара в воздухе. Упругость или парциальное давление пара выражается в миллиметрах ртутного столба.
Наиболее просто расчет скорости испарения М можно произвести но формуле
М = b0(Е – е), |
(1) |
где: М — скорость испарения в килограммах с одного квадратного метра в час; Е — парциальное давление насыщающих воздух паров воды при температуре испаряющей поверхности; е — парциальное давление паров воды, фактически содержащихся в воздухе; b0 — эмпирически устанавливаемый коэффициент испарения, состоящий из двух величин: А — коэффициента испарения влаги в неподвижный воздух и В — ветрового фактора, т. е. коэффициента, учитывающего влияние скорости движения воздуха на величину испарения.
Обозначение (Е – е), входящее в формулу, выражает дефицит влажности. По температуре мокрого термометра, показывающей в естественных условиях температуру поверхности жидкости, находят в соответствующих таблицах величину Е. Величину е вычисляют по относительной влажности воздуха, определяемой при помощи психрометра, пользуясь формулой:
e = |
Е φ 100 |
, |
где φ — относительная влажность воздуха в процентах.
Сушильная лаборатория ВТИ (39) предлагает такие числовые обозначения коэффициента испарения:
b0 = 0,023 + 0,017 W,
где W — скорость движения воздуха в метрах в секунду.
При испарении из чаш в струе воздуха предложено еще такое значение b0:
b0 = 0,031 + 0,0135 W.
| {115} |
Если испарение происходит в неподвижный воздух, вторая часть коэффициента b0, т. е. В, равна 0, так как испарение происходит в неподвижном воздухе, где W = 0.
Нашими экспериментальными данными по изучению испарения капустного сока с поверхности дошников в процессе хранения квашеной капусты величина А установлена равной 0,030. Подставляя значение коэффициента А из наших исследований в формулу, применяемую в химико-технологических процессах, находим числовое значение b0:
b0 = 0,030 + 0,0135 W.
Итак, для расчетов скорости испарения влаги с поверхности дошников во время хранения квашеной капусты могут быть использованы такие формулы:
М = 0,030 (Е – е) |
(2) |
в квасильных цехах при отсутствии движения воздуха, или
М = (0,030 + 0,0135 W)(Е – е), |
(3) |
если над поверхностью чанов воздух находится в движении.
В квасильных цехах, оборудованных в закрытых помещениях, воздух находится в состоянии относительного покоя, поэтому для. расчетов скорости испарения следует пользоваться формулой (2).
Зная скорость испарения М, т. е. количество килограммов воды, испаряющейся в час с одного квадратного метра поверхности, легко вычислить количество испаряющейся влаги с дошников любой поверхности по формуле:
Q = 0,030 (Е – е) S, |
(4) |
где: Q — количество килограммов воды, испаряющейся в час со всей поверхности дошника; S — поверхность дошника в квадратных метрах.
Форма испаряющей поверхности оказывает незначительное влияние на величину испарения, а потому этот фактор можно игнорировать при расчете величины испарения из больших сосудов типа дошника.
На величину испарения оказывает существенное влияние площадь испаряющей поверхности. Однако величина испарения изменяется не прямо пропорционально изменению испаряющей поверхности.
Как указывает В. Н. Кедроливанский, условия диффузии пара неодинаковы по всей испаряющей поверхности; они лучше у краев, чем в ее середине, потому что у краев имеется некоторое «добавочное испарение». {116}
Поэтому величина испарения с единицы поверхности в малых чанах будет большей, чем при одинаковых условиях испарения в больших. Как установлено (85), испарение с круглой поверхности будет пропорционально величине:
|
π R2 √D |
, |
где: R — радиус чана; D — диаметр чана.
Эта зависимость величины испарения для сосудов круглой формы, по нашим расчетам, может быть распространена на сосуды квадратной и приближающейся к квадратной прямоугольной формы.
Для квадратной поверхности она будет пропорциональна величине
|
a2 √a |
, |
где а — сторона квадрата; а для прямоугольной поверхности
|
BL √0,5(B + L) |
, |
где: В — ширина и L — длина прямоугольника.
В дальнейшем формулы расчетов испарения влаги приводятся применительно к дошникам с круглой поверхностью, с учетом, что для дошников с другой формой поверхности величина
|
π R2 √D |
в формулах должна быть заменена соответствующей ей другой величиной.
Таким образом, учитывая влияние поверхности на величину испарения, общую формулу (4) для вычисления величины испарения можно преобразовать так:
|
(5) |
Из других факторов, влияющих на скорость и, следовательно, величину испарения, необходимо отметить барометрическое давление, природу жидкости, высоту краев дошников, возвышающихся над поверхностью капустного сока и состояние поверхности жидкости.
Влияние барометрического давления на величину испарения при среднемесячных подсчетах потерь в закрытых помещениях сводится к нулю. Этот фактор мы считаем возможным не учитывать. {117}
Указанные нами коэффициенты испарения рассчитаны для воды. Каждой жидкости свойственна скорость испарения, обусловленная ее природой. Капустный сок, представляет собой раствор разных органических веществ и соли, испаряет влагу медленнее воды. По нашим лабораторным исследованиям скорость испарения влаги из сока квашеной капусты составляет в среднем 95,3% скорости испарения чистой воды из сосудов с одинаковой поверхностью и при одинаковой температуре и влажности воздуха. Следовательно, для расчета потерь влаги из капустного сока надо было бы ввести дополнительный коэффициент — 0,953. Ввиду того, что фактические среднемесячные потери влаги из капусты при хранении составляют 0,3–0,6%, введение этого коэффициента привело бы к получению 0,286–0,572%, т. е. величин, обычно в практике округляемых до десятых долей единицы, т. е. опять-таки к числам, установленным без применения поправочного коэффициента. Этот фактор можно игнорировать в расчетах, предназначенных для практическая применения.
На скорость испарения влияет также и высота краев дошника над уровнем капустного сока. Исследованиями различных авторов и нашими лабораторными опытами установлено, что чем больше края сосудов возвышаются над поверхностью испаряющейся жидкости, тем медленнее проходит испарение. Это происходит потому, что над поверхностью жидкости образуется слой воздуха, насыщенного парами воды, который препятствует свободной диффузии паров воды в воздух. Чем толще слой насыщенного воздуха, тем больше замедляется испарение.
На основании теоретических уравнений скорости испарения в неподвижном воздухе (85) можно установить величину влияния высоты краев сосуда над испаряющей поверхностью на скорость испарения. Она может быть выражена формулой
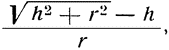
где: h — высота воздушного слоя от поверхности испаряющейся жидкости до краев сосуда; r — радиус сосуда.
Назовем эту величину высотой слоя воздушного пространства и обозначим ее Нв.
Как видно из формулы, на величину Нв оказывает влияние не только высота воздушного слоя (h), но и радиус поверхности (r). По мере увеличения радиуса при одинаковой величине h Нв будет приближаться к единице и, следовательно, влияние этого фактора будет незначительным.
Так, по нашим расчетам при h = 0,1 м, Нв будет равно для дошника с радиусом поверхности, равным 0,7 м,— 0,871 и для дошника с радиусом, равным 1,27 м, — 0,925.
Влияние высоты слоя воздушного пространства (h) на скорость испарения значительно. Приводим значение Нв, рассчитанное {118} нами для 15-тонного дошника с радиусом поверхности, равным 1,27 м:
при |
h = 0,1 |
м |
Нв = 0,925 |
„ |
h = 0,2 |
„ |
Нв = 0,856 |
„ |
h = 0,3 |
„ |
Нв = 0,791 |
„ |
h = 0,4 |
„ |
Нв = 0,732 |
Для получения точных данных возможных потерь от испарения величину Нв следовало бы ввести одним из множителей в формулы расчета потерь на испарение. Однако в формуле (5) этот фактор частично нашел свое отражение в предложенном нами коэффициенте испарения (А = 0,030), выведенном нами из производственных опытов, в которых, как правило, края дошника возвышались над поверхностью капустного сока до 20 см, что характерно для капустных цехов.
Для расчета потерь в тех случаях, когда h более 0,2 м, следует вводить коэффициент Нв.
Предложенная нами формула расчета испарения влаги дает возможность вычислить потерю влаги в час времени. Поскольку в практике производства потери учитываются помесячно или по дням, следует и формулы расчета их привести к среднедневным показателям. Помножив числовое выражение предложенного нами коэффициента А = 0,030 на 24, получим среднедневную величину коэффициента, равную 0,72. При вычислении потерь за более продолжительное время коэффициент 0,72 умножается на t — число дней.
Если обозначить потери от испарения влаги Ив за некоторый отрезок времени в процентах, то для дошников с круглой поверхностью
|
(6) |
где Р — вес капусты, находящейся в дошнике, в килограммах.
При расчете дефицита влажности (Е – е) по формуле (6) необходимо пользоваться средней температурой и относительной влажностью за расчетный период. Для расчетов потерь за период в несколько месяцев в целях получения более точных результатов необходимо потери рассчитывать за каждый месяц отдельно, пользуясь для этого среднемесячной температурой и относительной влажностью воздуха.
Для ускорения расчетов потерь влаги от испарения удобно формулу (6) преобразовать, заменив величину е ее значением, равным
|
Еφ 100 |
, |
где φ — относительная влажность воздуха в процентах. Таким образом, выражение Е – е примет вид
E – |
Еφ 100 |
, |
или, после преобразования, 0,01Е(100 – φ). {119}
Обозначив в формуле (6) значение Е – е новым выражением и произведя умножение цифровых величин, получим:
|
(7) |
Приведенная формула расчета потерь влаги от испарения применима в тех случаях, когда испарение происходит со спокойной поверхности в неподвижный воздух. При ферментации капусты поверхность покрывающего капусту сока не находится в спокойном состоянии. Выделяющиеся при ферментации газы приводят поверхность капустного сока в движение, она бурлит более или менее интенсивно в зависимости от условий ферментации. На поверхности в результате брожения образуется пена. Естественно, что все это должно изменять скорость испарения влаги в процессе ферментации.
Для изучения влияния указанных факторов на скорость испарения нами были поставлены лабораторные опыты. В две банки одинаковой формы и площади поверхности была налита вода. Обе эти банки находились в одинаковых условиях испарения — в лаборатории. Через толщу воды одной из банок пропускали углекислый газ, который, выходя, бурлил воду.
Вода в другой банке находилась в спокойном состоянии.
Оказалось, что скорость испарения влаги из банки, через воду которой пропускали углекислый газ, в 2,5 раза превышала скорость испарения из другой банки, в которой вода находилась в спокойном состоянии.
Изучение экспериментальных данных по квашению капусты в производственных условиях показало, что величина испарения влаги из дошников в процессе ферментации зависит от обычного испарения и количества выделяющихся при ферментации газов.
Выделяющиеся при ферментации газы, отрываясь от поверхности жидкости, увлекают за собой пары воды. Количество испарившейся при этом воды будет находиться в прямой зависимости от количества выделившихся газов, которое в свою очередь будет определяться безвозвратной потерей сухих веществ сбраживаемого сырья.
При одинаковых условиях чистоты и направленности ферментации количество выделившихся газов в килограммах с единицы поверхности в день q будет прямо пропорционально величине
|
P b 100 t · π R2 |
, |
где: P — масса капусты в килограммах; b — процент безвозвратных потерь сухих веществ; t — продолжительность ферментации в днях.
Нас, однако, интересует не величина q, характеризующая скорость выделения газов, а влияние этой величины как ускорителя испарения влаги. Если бы испарение влаги при разных {120} температурах и разном дефиците влажности было одинаково, то, очевидно, дополнительное испарение влаги под влиянием выделяющихся газов было бы пропорционально q, т. е. скорости выделения газов.
Однако с повышением температуры и дефицита влажности значительно повышается и интенсивность испарения влаги, вследствие чего действие q как ускорителя испарения значительно снижается. И наоборот, при низких температурах и при незначительном дефиците влажности, когда отрыв частиц воды с поверхности затруднен, действие q на увеличение испарения повышается.
Вследствие этого, а также потому, что капустный сок представляет собой специфическую среду, мы пришли к выводу о необходимости установить эмпирический коэффициент для дополнительного испарения влаги из капустного сока при разных температурах.
Таким образом, дополнительное испарение влаги под влиянием выделяющихся газов в процентах к весу капусты Q1 должно составить величину — b К, где: b — процент безвозвратных потерь сухих веществ и К — эмпирический коэффициент выноса паров воды выделяющимися газами.
В результате трехлетних исследований квашения капусты в производственных условиях нами были найдены следующие эмпирические величины коэффициента К:
Температура | Коэффициент | ||||
Свыше | 20 | 0,50 | |||
„ | 16 | до | 20 | 0,65 | |
„ | 13 | „ | 16 | 0,80 | |
„ | 10 | „ | 13 | 1,00 | |
„ | 5 | „ | 10 | 1,10 | |
Разумеется, этот коэффициент, выведенный эмпирическим путем, не может претендовать на абсолютную точность, но, как показало применение его в практике вычислений дополнительного испарения влаги, он приводит к практически верным результатам.
Величина b — потери сухих веществ в процентах к весу сырья — определяется по кислотности по приведенной выше (см. Потери сухих веществ) формуле b=nf, где n кислотность капусты по окончании ферментации и f — кислотный коэффициент потери сухих веществ. Подставив в выражение bK значение b, определенное по кислотности, получим, что дополнительное испарение влаги, вызванное выделением газов, Q1 = nfK.
Дополнительное испарение воды Q1 можно вычислить, пользуясь средними данными о потерях сухих веществ из наших исследований, приведенных в табл. 67. Округляя эти потери до 0,1%, применительно к тем же температурным периодам, по которым вычислен K, получим такое значение b:
| {121} |
Температура | b - потеря сухих | ||||
Свыше | 20 | 1,6 | |||
„ | 16 | до | 20 | 2,0 | |
„ | 13 | „ | 16 | 2,5 | |
„ | 10 | „ | 13 | 2,0 | |
„ | 5 | „ | 10 | 1,6 | |
При пользовании этими величинами Q1 = bK. В этом случае результат получается несколько менее точный, но практически вполне применимый, так как дает отклонения в пределах 0,1%.
С учетом дополнительного испарения влаги Q1 общие потери от испарения влаги в процессе ферментации Q составят:
|
(8) |
или
|
(9) |
Приведенные формулы дают возможность рассчитать потери при ферментации капусты в любых условиях, т. е. при разных температурах и относительной влажности воздуха, разных размерах поверхностей и емкостей дошников. Для определения практической применимости этих формул при расчете потерь в табл. 68 приводим данные по сравнению фактических потерь влаги (в %) при ферментации с потерями, рассчитанными по формулам.
|
ТАБЛИЦА 68
| ||||||||||||||||||||||||||||||||||||||||||
Сопоставление фактических потерь влаги, полученных нами при трехлетнем изучении промышленного квашения капусты, с потерями, рассчитанными по формуле, показывает отклонения в сторону увеличения или уменьшения от 0 до 0,09%.
Такие незначительные отклонения фактических потерь от расчетных свидетельствуют о полной применимости предложенных формул для практических расчетов.
| {122} |
Общие естественные потери при ферментации капусты, обусловленные сущностью самого процесса брожения (Пф), состоят из рассмотренных выше потерь сухих веществ и влаги. Расчет их может быть произведен по формулам испарения влаги (8–9) с прибавлением потерь сухих веществ (b). Для дошников с круглой поверхностью они примут такое выражение:
Пф = |
0,72t Е · (100 – φ) π R2 P · √D |
+ bK + b. |
или после преобразования
|
(10) |
Если потерю сухих веществ определяют по кислотности, — в формулах b следует заменять выражением nf, где n — кислотность в процентах и f — кислотный коэффициент потери сухих веществ.
Фактические нормальные весовые потери при ферментации в дошниках емкостью от 1,5 до 15 т, по исследованиям авторов, колеблются при разных температурах и продолжительности брожения в пределах от 3,28 до 6,24%. Для характеристики этих потерь по дошникам разных емкостей и в зависимости от условий ферментации в табл. 69 и 70 приводим данные опытного квашения капусты на Грушковском засолочном заводе и на Чоколовском плодокомбинате.
|
ТАБЛИЦА 69
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {123} |
|
ТАБЛИЦА 70
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Приведенные в таблицах расчеты весовых потерь капусты при ферментации, основанные на физических законах и учете сущности биохимических процессов брожения, сходны или незначительно разнятся от фактических потерь. Это является наиболее веским доказательством того, что нормальные весовые потери действительно находятся в пределах, установленных опытами. Расхождения средних фактических и расчетных данных по Грушковскому засолочному заводу на 0,03% и по Чоколовскому плодокомбинату на 0,026% подтверждают также, что предложенные формулы расчета правильно учитывают все многообразие процессов брожения в разных условиях. Отклонения фактических потерь по отдельным дошникам от расчетных следует считать отклонениями от нормы, какой должны быть признаны расчеты. А эти отклонения могут легко возникнуть по отдельным дошникам в производственных условиях: вылилось немного сока или дошник стоит вблизи дверей — потери увеличились; поверхность капустного сока опустилась ниже 0,2 м от уровня краев дошника, или значительная часть поверхности укрыта прессом — потери уменьшились и пр.
Иллюстрацией общих тенденций в динамике весовых потерь в зависимости от температуры, продолжительности и дефицита влажности могут служить кривые потерь влаги, сухих веществ и общих весовых потерь, изображенные на рис. 19. В то время как потери сухих веществ в основном определяются температурой и продолжительностью брожения, на потери влаги основное влияние оказывает дефицит влажности. Кривая потерь сухих веществ поднимается при средних температурах и снижается при более высоких и низких, что является верным отражением направленности ферментативного процесса. Потери влаги наибольшие при самой высокой температуре и наибольшем дефиците влажности и кривая их обнаруживают общую тенденцию снижения по мере понижения дефицита влажности. Кривая общих потерь является функцией двух первых и носит на себе их отпечаток, но больше
| {124} |
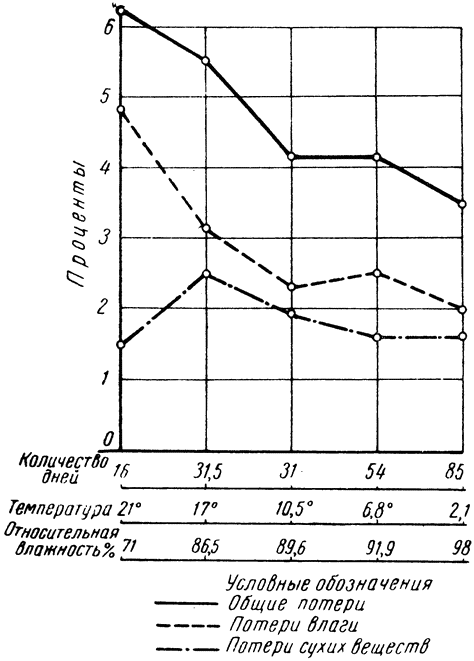 |
Рис. 19. Средние потери веса капусты при ферментации (в процентах) |
находится под влиянием потерь влаги, падая по мере снижения температуры и относительной влажности воздуха. Таким образом, общие потери, как и потери влаги, в основном регулируются температурой и относительной влажностью воздуха.
Динамика потерь при ферментации в закрытых сосудах имеет иной характер. Поскольку потери влаги при закрытом брожении сведены к минимуму, практически едва поддающемуся учету, общие весовые потери целиком находятся под влиянием потерь сухих веществ. Наши наблюдения над динамикой весовых потерь в лабораторных условиях, приведенные в табл. 71, не только отражают весовые изменения в процессе ферментации, но и определяют содержание потерь в сравнении с брожением в открытых сосудах (средняя температура за период ферментации 7° и относительная влажность — 74%).
Потери влаги при закрытом брожении составили через пять дней после начала ферментации всего 0,08% и на этом уровне оставались до 60-го дня. За этот же период потери влаги при открытом брожении с 1,47% на 5-й день поднялись до 4,94% на 60-й день. Потери сухих веществ в закрытых банках нарастали очень медленно, поднявшись с 0,16% на 5-й день до 0,74% на 60-й. В открытых банках за этот же период времени потери сухих
| {125} |
|
ТАБЛИЦА 71
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
веществ выросли с 0,59 до 2,01%. Соответственно этому к концу ферментации капусты в открытых банках общие весовые потери капусты в них достигли 6,95%, в то время как в закрытых банках они составили всего 0,82%, т. е. в 8,5 раза меньше. Правда, в закрытых банках процесс ферментации еще не закончился к 60-му дню и нарастание кислотности в них продолжалось еще в течение пяти месяцев. Но все это свидетельствует о том, что введением закрытого брожения в практику можно повысить качество готового продукта, увеличить продолжительность его хранения, значительно сократив при этом потери.
Снижение потерь значительно улучшает качество продукции.
В 1948 г. по предложению авторов Министерство торговли Украинской ССР снизило для своей системы нормы потерь при ферментации капусты с 17 до 12%, которые в 1950 г. Министерство торговли СCCP утвердило, как обязательные по всему Союзу. В начале 1950 г. украинское совещание технологов и мастеров Министерства торговли УССР констатировало повышение качества продукции за истекшие два года. Что же касается фактических потерь при ферментации, то в сезон 1948/49 г. они по восьми учтенным областям составили в среднем 10,94% и в сезон 1949/50 г. по четырем областям — 12,6%. В среднем за два года по учтенному количеству заквашенной капусты потери выразились в 11,55% вместо 17% по старым нормам.
ВЫВОДЫ
Исследование технологии квашения капусты дало возможность вскрыть сущность всего разнообразия отдельно взятых физико-химических и микробиологических процессов и явлений, объединяемых понятием «квашение», а также установить направляющие их факторы. Это в свою очередь является основой для перестройки {126} существующей технологии квашения, задачей которой должно быть повышение качества продукции, максимальное сокращение производственных потерь, ликвидация непроизводительных трат и — на этой основе — снижение себестоимости продукции.
Прежде всего, изучение квашения капусты дает возможность сделать вывод, что применяемая до настоящего времени технология квашения капусты, представляющая собой «заготовку впрок», в существе своем порочна, так как совмещает процессы брожения и хранения, требующие различных условий для их проведения. Брожение капусты наиболее эффективно проходит при 21–24°, а хранение готовой квашеной капусты при –2–0°. Совмещение этих столь различных по условиям прохождения процессов заканчивается на практике тем, что ни один из них не проводится в наиболее эффективных условиях. А если создаются благоприятные условия для одного из них, то исключается возможность проведения другого без ухудшения качества продукта. Кроме того, при существующей технологии невозможно приостановить процесс брожения на желаемой стадии и фиксировать качество полученного продукта низкими температурами хранения. Поэтому брожение произвольно заходит иногда очень глубоко, вплоть до полного сбраживания сахаров, вследствие чего продукт лишен постоянного химического состава и вкусовых достоинств. Рациональная технология квашения должна предусмотреть отделение процесса брожения капусты от ее хранения и обеспечить выпуск продукта постоянного качества. При такой постановке технологии откроются большие возможности для механизации трудоемких процессов и повышения производительности труда.
Вместе с тем исследования указывают и средства улучшения существующей технологии квашения. Основные из них следующие:
1. Отказ от перегрузки дошников, и укладки так называемой «шапки», приводящей к непроизводительной трате капустного сока, что способствует обеднению продукта водой и ценными сухими веществами.
2. Правильное пригнетание капусты в дошниках, которое позволит избавиться от получения излишнего свободно стекаемого сока и от образования овершья.
3. Ведение ферментации капусты при высокой относительной влажности (не ниже 80%) приведет к сокращению потерь на испарение влаги из капусты.
Введение этих и других мероприятий по улучшению технологии квашения должно быть стимулировано установлением и новых обязательных норм производственных потерь, сниженных до пределов, обусловливаемых нормальным проведением технологического процесса. Как это доказывается экспериментальным квашением и теоретическими расчетами, естественные потери производства, связанные с его сущностью, должны находиться в пределах норм, определяемых физическими условиями ферментации. Поскольку эти условия нашли свое отражение в предложенных {127} формулах расчета, ими и следует руководствоваться при расчетах нормальных потерь.
Предложенные формулы расчета потерь пригодны для применения в различных климатических условиях для дошников 30-тонной емкости и 100-литрового бочонка, для 5-дневной и 100-дневной продолжительности ферментации.
Нет никаких сомнений, что под влиянием новых более жестких нормативов производственных потерь и дальше быстро будет улучшаться технология квашения, повышаться качество готовых продуктов, а вместе с этим будет достигнуто и дальнейшее снижение производственных потерь.
Глава четырнадцатая
По окончании ферментации и с наступлением периода хранения в квашеной капусте продолжаются микробиологические процессы, свойственные периоду ферментации, но в иных темпах и ином соотношении. Основной процесс — молочнокислое брожение — затухает и после израсходования остатков сахара совершенно прекращается. В то же время активизируются побочные процессы, главным образом спиртовое и уксуснокислое брожения, которые становятся преобладающими. Развивается поверхностная пленка плесеней, потребляющая молочную кислоту, чему способствует прекращение выделения углекислого газа на поверхность капусты. Вся эта микрофлора развивается тем энергичнее, чем выше температура хранения. Продолжается испарение влаги и общее уплотнение всей капустной массы в дошнике.
Вполне естественно поэтому, что химический состав квашеной капусты не остается стабильным, а продолжает изменяться. Однако вследствие преобладания побочных микробиологических процессов химические изменения носят отрицательный характер. С достаточной наглядностью это подтверждают химические анализы капусты в процессе ее хранения в неохлаждаемых помещениях, приведенные в табл. 72.
Сравнение химического состава капусты по окончании ферментации с капустой, хранившейся два, пять и семь месяцев, дает представление о сущности происходящих изменений. Происходит потеря сухих веществ под влиянием микробиологических процессов. Сахар, расходуется до полного его исчезновения. Уменьшается кислотность вследствие преобладания процессов расщепления кислоты над процессами ее образования. Особенно усиливается падение кислотности после израсходования сахара, т. е. с прекращением
| {128} |
|
ТАБЛИЦА 72
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
процесса накопления молочной кислоты. Уменьшается содержание азотистых и минеральных веществ, расходуемых развивающейся микрофлорой. Повышается содержание соли вследствие испарения влаги. Увеличивается содержание спирта и летучих кислот. Значительно разрушается витамин С — через семь месяцев хранения его остается всего 46,4% первоначального содержания. Такое большое разрушение витамина С вызвано, видимо, не столько падением кислотности, так как даже к концу хранения ее оставалось 1,26%, сколько удалением из капусты углекислого газа.
Таким образом, качество капусты по мере удлинения сроков хранения постепенно ухудшается.
Темпы химических изменений, как показывают наши исследования, замедляются с понижением температуры хранения. В табл. 73 мы приводим химический состав капусты, хранившейся в дошниках пять месяцев при разных температурах.
|
ТАБЛИЦА 73
| |||||||||||||||||||||||||||||
Все составные вещества капусты при температуре 3,2° сохранились лучше, чем при 10,5°, к тому же и летучих кислот {129} образовалось меньше. Исключение составляет спирт, которого при более низкой температуре накопилось несколько больше.
Снижение кислотности в процессе хранения капусты и, в частности, темпы снижения достаточно верно отражают интенсивность развития всех побочных процессов, которые следовало бы назвать процессами распада. Это будет справедливо не только в отношении самой кислоты, но и всех составных частей капусты, как это видно из приведенного выше химического состава ее при разных сроках хранения. На темпы снижения кислотности основное влияние оказывает температура хранения — чем она выше, тем выше и темпы распада кислоты. Этот вывод, сделанный микробиологами, нашел подтверждение и в наших исследованиях. На рис. 20
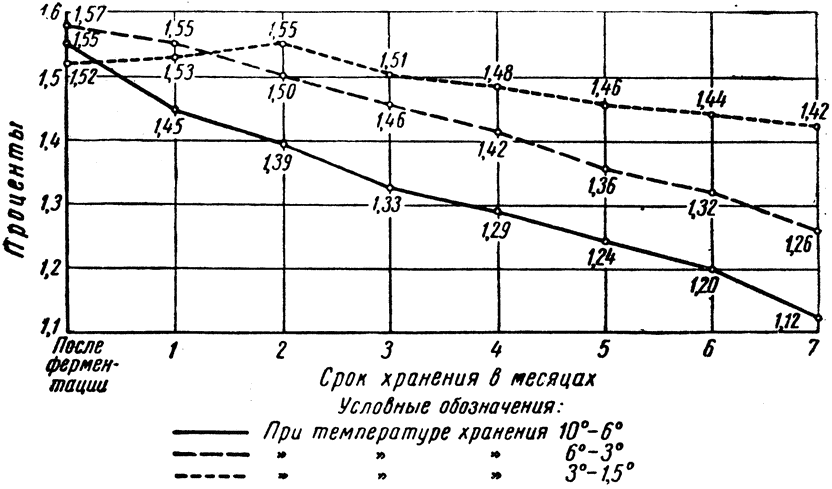 |
Рис. 20. Содержание общей кислотности в верхнем слое квашеной капусты в дошниках (в процентах) |
приведены кривые падения кислотности в верхнем слое капусты, хранившейся в крупных дошниках при разных, но низких температурах. Общая тенденция всех кривых — падение по мере удлинения сроков хранения. Но в то время как при температуре 3–1,5° на 7-й месяц хранения кислотность сохранилась на 93,4% от первоначального содержания, при 3–6° — на 80,3%, при 10–6° ее осталось к концу хранения только 75,5%. Необходимо отметить, что во всех этих случаях кислотность капусты сохранялась вполне удовлетворительно, так как при наиболее высокой температуре (6–10°) ее в абсолютных количествах осталось 1,12%. Сохранению кислотности способствовали пониженные температуры хранения и тщательный уход за капустой, заключающийся в систематическом удалении образующейся поверхностной пленки. {130}
Совсем иными темпами снижается кислотность при более высоких температурах и, особенно, если образующуюся пленку не удаляют. Поставленные с этой целью лабораторные опыты, в которых квашеная капуста хранилась при 18–20°, показали, что через десять дней хранения в банках, с поверхности которых пленку систематически снимали, кислоты осталось 53,1% ее первоначального содержания, а в тех банках, где пленка не снималась, — всего 20%.
Развитие плесеневой пленки на поверхности капустного сока во время хранения, состоящей в основном из потребителей молочной кислоты, является основным фактором, сокращающим сроки хранения квашеной капусты. Понижение кислотности с последующим полным распадом кислоты в поверхностном слое неминуемо приводит к развитию гнилостных процессов, постепенно проникающих в глубь дошников.
Мы уже отмечали, что с повышением температуры хранений пленка развивается более энергично. Специально поставленными опытами установлено, что пленка появлялась на поверхности капустного сока при разных температурах в такие сроки:
При | 20° | через | 2 | дня |
„ | 15° | „ | 3 | „ |
„ | 10° | „ | 5 | дней |
„ | 5° | „ | 6 | „ |
„ | 2° | „ | 8 | „ |
Следовательно, весьма существенным фактором снижения активности развития пленки является понижение температуры хранения. Однако даже такая низкая температура, как +2, не предохраняет от появления пленки, которую систематически надо удалять с поверхности капусты.
Вполне естественно поэтому стремление изыскать средства борьбы с развитием пленки.
Ф. В. Церевитинов и другие исследователи считают, что развитие пленки легко предотвращается покрытием поверхности капусты эмульсией горчичного масла или бумагой, пропитанной парафином и горчичным маслом. На практике иногда применяют засыпку поверхности капусты в дошнике слоем сухой соли или заливку солевыми растворами разной крепости. Хотя такой способ отрицательно сказывается на качестве довольно значительного по глубине слоя капусты, увеличивая в ней содержание соли, все же он является довольно эффективным. Надо иметь в виду, что солевые растворы необходимо применять с концентрацией соли не ниже 12,5%, потому что на таких растворах поверхностная пленка не развивается. Более слабые растворы только задерживают развитие пленки, но не могут его предотвратить.
В табл. 74 показана зависимость появления пленки от концентрации соли в капустном соке почти при одинаковой температуре. Из этих данных видно, что даже при 10% -ной концентрации соли на 17-й день появилась пленка.
| {131} |
|
ТАБЛИЦА 74
| ||||||||||||||||||||||||||||||
Наиболее существенным средством борьбы со всеми плесенями, а попутно и со всеми побочными брожениями надо признать закрытое брожение капусты с последующим хранением ее в герметизированных дошниках. Как показали наши опыты по закрытому брожению, несмотря на выход излишков, образующихся при брожении газов, под подгнетным кругом и в толще капусты накопляется столько углекислого газа, что он препятствует развитию всей микрофлоры, за исключением молочнокислых и масляно-кислых бактерий. Но маслянокислые бактерии, требующие повышенных температур для своей жизнедеятельности, при этом тоже не развиваются.
При хранении в герметизированных дошниках накопившийся в больших количествах углекислый газ способствует образованию более резкого вкуса капусты, несколько ухудшая ее вкусовые достоинства. Но это только в первые часы после открытия дошника. Достаточно оставить дошник открытым в течение 24–36 час. для удаления излишка газов, как капуста принимает нормальный приятный вкус.
Химический же состав капусты закрытого брожения и хранения изменяется меньше, чем при открытом брожении. Для сравнения
|
ТАБЛИЦА 75
| ||||||||||||||||||||||||||||||||
| {132} |
в табл. 75 приводим химический состав квашеной капусты из закрытого дошника через 190 дней хранения в сопоставлении с химическим составом капусты из контрольного открытого дошника.
Приведенные данные показывают, что в закрытом дошнике лучше сохранились сахар, кислота, азотистые вещества, витамин С, меньше образовалось летучих кислот и спирта. Кроме того, из этого дошника не испарилась влага, вследствие чего лучше сохранился первоначальный вес. Этим объясняется несколько меньшее содержание сухих веществ по сравнению с открытым дошником.
В герметически закрытых дошниках плесеневая пленка не образуется.
В дошниках происходит дальнейшее, хотя и незначительное, уплотнение капусты и уменьшение объема и веса ее в основном за счет испарения влаги и разрушения сухих веществ.
В табл. 76 приведены средние данные изменения объема капусты по 3-летним исследованиям.
|
ТАБЛИЦА 76
| ||||||||||||||||||||||||||||||||||||||||||
Как средние, эти данные не связаны с определенными условиями хранения — температурой и влажностью воздуха и емкостью дошников. Задача авторов при изучении этого вопроса заключалась в том, чтобы установить общие тенденции. Все же необходимо отметить, что в исследованиях преобладала температура хранения в пределах 5–10° и относительная влажность воздуха 85–95%. Наблюдения велись преимущественно над капустой, хранившейся в 5- и 15-тонных дошниках.
Приведенные данные показывают, что при хранении капуста незначительно меняет свой объем. Так, за семь месяцев хранения объем уменьшился в среднем на 2,84%, тогда как за короткий период ферментации объем капусты уменьшается на 15–17%. Такое незначительное уменьшение объема капусты происходит при нормальных условиях хранения. При повышении температуры {133} и снижении относительной влажности воздуха объем капусты может уменьшиться в значительно большей степени, так как уменьшение его происходит в основном за счет испарения влаги и разрушения сухих веществ, а интенсивность этих процессов находится в тесной зависимости от внешних условий.
Из трех факторов, вызывающих уменьшение объема, наиболее значительно влияние испарения влаги — 68,3% к общему уменьшению, затем разрушение сухих веществ — 25,4% и самое незначительное — 6,3% — оказывает вытеснение газов из массы капусты под действием собственной тяжести и гнета.
Уплотнение и уменьшение объема капусты происходит постепенно и почти пропорционально продолжительности хранения, если условия его примерно одинаковы.
Изменение объема капусты находится в тесной связи с весовыми потерями капусты. В табл. 77 приведены средние месячные весовые потери капусты при хранении с октября по май. Эти данные показывают, что весовые потери по отдельным месяцам в абсолютных величинах незначительны — от 0,4 до 0,7% (данные за два года исследований).
|
ТАБЛИЦА 77
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Однако колебания довольно велики и определяются в основном испарением влаги, которое находится в прямой зависимости от дефицита влажности воздуха. Наибольшие средние потери от испарения влаги — 0,52% — получены для октября со средней температурой 6° при относительной влажности воздуха 90%. Самые незначительные потери — 0,396% — получены в апреле при средней температуре 5,4° и относительной влажности воздуха 97%. Испарение влаги при хранении подчиняется общим физическим законам и для каждого отдельного случая может быть вычислено по приведенной нами выше формуле (7).
Что касается потерь сухих веществ, то, как показано в табл. 77, в среднем для всех месяцев хранения они составляют незначительную {134} величину — 0,17% с колебаниями в отдельные месяцы от 0,013 в сторону уменьшения до 0,049% в сторону увеличения. Потери сухих веществ находятся в зависимости от температуры хранения, которая определяет активность микробиологических процессов. Так, при 2,9° потери в среднем составили 0,157%, при 5,4° — 0,166% и 8,1° — 0,219%.
Так как абсолютные потери сухих веществ при хранении очень невелики, то для практических расчетов при хранении капусты можно принять их среднемесячную величину, равную 0,17%. Приняв эту величину за постоянную, общие весовые потери капусты при хранении в процентах Пх можно подсчитать по формуле:
|
(11) |
Проверка применения этих расчетов в практике производства показала, что отклонения расчетов от фактических потерь колеблются от 0 до 0,03%, как это видно из данных табл. 78.
|
ТАБЛИЦА 78
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Потери при хранении капусты, так же как и при ферментации, подчинены общим физическим законам, нашедшим свое отражение в наших расчетных формулах. Поэтому будет правильным принять потери при хранении, рассчитанные по приведенным формулам, как нормальные для открытых дошников. Возможные отклонения фактических потерь в сторону увеличения от расчетных будут показателем того, что, кроме естественных факторов, на образование фактических потерь влияли и другие (вытекание сока из дошников, прямое изъятие из дошника капусты или сока и пр.).
Хранение квашеной капусты в закрытых дошниках приводит практически к полному прекращению испарения, значительно сокращая общие весовые потери при хранении.
Сокращению естественных весовых потерь квашеной капусты при хранении способствует и применяемая иногда на практике заливка поверхности капусты крепким солевым раствором. Как {135} мы уже указывали, капусту заливают солевым раствором, чтобы предупредить развитие плесеней и порчу капусты. Но солевые растворы имеют еще и то преимущество, что испарение влаги из них значительно тормозится и тем более, чем концентрированнее раствор. Специально поставленными в большом количестве лабораторными опытами нам удалось установить зависимость скорости испарения влаги из капустного сока от количества растворенной в нем соли. Если испарение из чистой воды принять за 100, то испарение из капустных соков с различным содержанием соли будет следующим:
3% | соли | ...... | 95,3 | 8,0% | соли | ..... | 72,2 |
|
4,5% | „ | ...... | 85,8 | 10,0% | „ | ....... | 65,9 |
|
6,0% | „ | ...... | 80,2 | 12,5% | „ | ....... | 57,8 |
Согласно этим данным концентрация соли в 12,5%, т. е. та концентрация, при которой прекращается развитие плесеней, вызывает сокращение испарения влаги в среднем на 42,2%.
Поскольку испарение влаги из капусты во время хранения является основным слагаемым весовых потерь, самое существенное сокращение их может быть достигнуто поддержанием высокой относительной влажности воздуха и особенно в сочетании с низкими температурами.
Наилучшими вкусовыми достоинствами обладает капуста, в которой процесс брожения не доведен до конца, т. е. до полного сбраживания сахара. Обычно в такой капусте накапливается от 0,7 до 1% кислоты и остается свыше 1% (до 2%) сахара. Наличие сахара при небольшом количестве кислоты придает капусте приятный винно-солоноватый вкус. Когда же брожение заходит более глубоко, т. е. совпадает со временем окончания ферментации, содержание кислоты в капусте превышает 1 и доходит до 1,5%. В этом случае в ней остается еще от 0,5 до 1% сахара. Капуста приобретает более острый вкус, но и в данном случае острота вкуса несколько смягчается наличием небольшого количества сахара. Вкус можно характеризовать, как кисловато-солоноватый.
При хранении такой капусты в открытых дошниках, как об этом было сказано выше, сахар окончательно сбраживается, возрастает содержание летучих кислот и спирта, а общая кислотность либо повышается до 2%, либо снижается до 1–1,2%. В обоих случаях возрастает ощущение остроты во вкусе из-за отсутствия сахара и увеличенного содержания летучих кислот и спирта. Такая капуста может быть охарактеризована как солоновато-кислая. В тех же случаях, когда содержание кислоты повышается до 2%, она ощущается как острокислая.
Таким образом, длительное хранение квашеной капусты в дошниках из-за продолжающихся в ней микробиологических {136} процессов приводит к ухудшению ее вкусовых достоинств (как следствие общего ухудшения химического состава). Это, однако, наблюдается в случаях хранения капусты при температуре выше 0°. Хранением капусты при температуре от 0° и до –2°, обычно удается фиксировать ее химический состав на уровне окончания ферментации.
Кроме ухудшения вкусовых достоинств капусты, хранящейся в неохлаждаемых помещениях, при значительном снижении кислотности наблюдается потеря капустой упругой консистенции. Последнее связано, видимо, с уменьшением степени набухания белков капустной ткани. Капуста иногда становится вначале слабохрустящей и, наконец, дряблой. Затормозить развитие процессов, ухудшающих качество капусты при длительном хранении, можно только понижением температуры хранения до –2–0° и борьбой со снижением кислотности.
Говоря о вкусовых достоинствах капусты и определяющих их факторах, следует отметить некоторые противоречия в стандарте на квашеную капусту (ГОСТ 3858–47).
В стандарте вкус капусты первого сорта характеризуется как «кисловато-солоноватый, освежающий, приятный». По химическим же показателям в капусте допускается кислоты от 0,7 до 2% и соли от 1,5 до 2,5%. Наличие сахара не обусловлено.
При указанных нормах капуста с содержанием соли 1,5% и кислоты 2% будет ощущаться, как острокислая.
Только капуста с содержанием соли 2–2,5% и кислоты 0,7–1,0% будет обладать кисловато-солоноватым вкусом. Но капуста может содержать 0,7–1,0% кислоты в результате неполного брожения, — и тогда в ней будет еще 1–2% сахара, — или в результате снижения кислотности при длительном хранении. В первом случае, т. е. когда капуста свеже заквашена и в ней сохранился сахар, она, действительно, будет на вкус «приятной, освежающей». Во втором случае капуста лишена приятного освежающего вкуса — это лежалый продукт с деградирующими процессами, с наличием повышенного содержания летучих кислот и, может быть, спирта.
Глава пятнадцатая
Столовая свекла (Beta vulgaris hortensis L.) в зависимости от климатических и почвенных условий местности, где она произрастает, от агротехники выращивания и сортовых особенностей имеет довольно разнообразный химический состав. Ф. В. Церевитинов приводит такие колебания химического состава свеклы (табл. 79).
| {137} |
|
ТАБЛИЦА 79
| |||||||||||||||||||||||||||||||||||||||
По данным Е. Д. Остренко, химический состав основных хозяйственно-ботанических сортов столовой свеклы следующий (см. табл. 80):
|
ТАБЛИЦА 80
| ||||||||||||||||||||||||||||||||||||||||||||||
Применительно к вызревшим корням наиболее распространенных у нас сортов свеклы данные Е. Д. Остренко наиболее типичны. Это подтверждается и нашими анализами свеклы сорта египетская из Киевской области. Состав свеклы был следующий (в процентах): воды — 83,33, общего сахара — 10,26, инвертного сахара — 0,12, сахарозы — 10,14, кислоты (по яблочной) — 0,25, азотистых веществ — 1,98, золы — 0,86, витамина С — 8,54 мг%.
Сахара свеклы состоят в основном из сахарозы, инвертный же сахар находится в незначительных количествах — от 0,12 до 1,20%. Что касается азотистых веществ, то, по данным Ф. В. Церевитинова, примерно половина их — от 0,36 до 1,55% — приходится на долю белков и столько же — небелковых соединений. Витамином С свекла вообще не богата. По данным В. Н. Букина, в свекле содержится 8 мг% витамина С.
Свеклу квасят в небольших количествах для приготовления маринадных полуфабрикатов, свекольного кваса, винегретов и пр. {138} Способы квашения весьма разнообразны: квасят ее целой и разрезанной на части, без соли и с заливкой солевыми растворами разной крепости — от 2 до 6%.
Наличие в свекле большого количества сахара и особенности разных способов квашения определяют содержание и ход ферментативного процесса и химический состав квашеной свеклы. Ниже, в табл. 81, приводим наши данные о химическом составе свеклы, заквашенной без соли и залитой 4%-ным раствором соли, в сравнении с составом свежей свеклы (свекла сорта египетская, средняя температура ферментации 13,4°, продолжительность ферментации 30 дней).
|
ТАБЛИЦА 81
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Из этих данных видно, что в обоих случаях в квашеной свекле спирта образовалось больше, чем кислоты: спирта обнаружено 1,29 и 1,64%, а кислоты — 0,72 и 0,82%. Следовательно, при квашении свеклы ведущим является спиртовое брожение, а не молочнокислое. Это обстоятельство вызвано, видимо, как значительным содержанием сахара (более 10%), так и температурой брожения (в среднем 13,4°). Наибольшая направленность молочнокислого брожения, вызываемого эпифитной микрофлорой, создается ведением его либо при температуре выше 20° либо при температуре, близкой к 0°. В одном случае (при высокой температуре) происходит быстрое подкисление среды интенсивно развивающимися молочнокислыми бактериями, а в другом (при низких температурах) все побочные брожения затухают, тогда как молочнокислое в медленных темпах неуклонно развивается.
Заливка свеклы 4%-ным раствором соли привела к тому, что и кислоты и спирта в квашеной свекле образовалось больше (0,82 и 1,62%) по сравнению с квашением в чистой воде (0,72 и {139} 1,29%), а летучих кислот — меньше. Витамин С при квашении с солью сохранился на 75%, а в чистой воде полностью разрушился. И, наконец, что не менее важно, в свекле, заквашенной с солью, сухих веществ осталось больше на 1,2% чем в свекле, залитой водой. Это произошло, как будет видно из дальнейшего, вследствие меньшего увеличения ее объема при квашении.
Физические свойства свеклы также изменяются по-разному в зависимости от способа квашения (с солью или без нее, целыми корнями или разрезанными).
В табл. 82 приводятся данные по изменению абсолютного и удельного веса, объема свеклы и содержания в ней воздуха при разных способах квашения.
|
ТАБЛИЦА 82
| ||||||||||||||||||||||||||||||||||||||||||||
Оказывается, что квашение в чистой воде приводит к очень большому увеличению объема — на 15,2% в целых корнях и на 21,6% в корнях, разрезанных на 4 части. Это вызывает увеличение веса, соответственно, на 13,8 и 16,8% по сравнению со свежей свеклой. Таких значительных изменений объема и веса не наблюдается при квашении в соленых растворах. Так, в 4%-ном растворе соли объем целых корней увеличился всего на 2,5 и разрезанных — на 8,5%, а вес, соответственно, на 0,1 и 4,2%. В этом случае очень ярко сказалось действие соли как средства, уменьшающего способность коллоидов к набуханию.
Удельный вес корней и сока свеклы квашеной меньше, чем свежей, вследствие разбавления сухих веществ а заливке, и тем меньше, чем больше увеличение объема свеклы.
Следует отметить, что в первые дни квашения в чистой воде свекла в еще большей мере увеличивается в весе, чем это наблюдалось в конце ферментации. И только в последующие дни вес ее постепенно уменьшается, значительно превышая, однако, вес свежей.
В табл. 83 приведены данные об изменении веса свеклы в процессе ферментации.
Если сравнивать весовые изменения свеклы в процессе ферментации с изменениями огурцов, то наблюдаются диаметрально
| {140} |
|
ТАБЛИЦА 83
| ||||||||||||||||||||||||||||||||||||||
противоположные явления. Огурцы вследствие отдачи (осмоса) сока в рассол в первые дни ферментации значительно теряли в своем объеме и весе и лишь потом несколько восстанавливали его под влиянием обратного процесса диффузии. Свекла, наоборот, в первые дни чрезвычайно набухает, увеличиваясь в объеме и весе, а в последующий период уменьшается и в объеме и в весе.
Особенно резко, с большими отклонениями, это проявляется при квашении свеклы в чистой воде. С точки зрения физической эти явления отнюдь не противоречивы и вполне закономерны.
Огурцы, содержащие 2–3% сухих веществ, заливали рассолом с содержанием 8% сухих веществ (соли) и направление осмоса было от меньшей концентрации к большей — из огурцов в рассол. В свекле растворимых веществ 10–11%, а в воде — 0%. При том же. направлении диффузия — от меньшей концентрации к большей — вода должна поступать в свеклу. И только в последующем, при уравнивании концентрации сухих веществ в свекле и в заливке, сухие вещества должны переходить из свеклы в заливку.
Ход этих двух взаимно противоположных процессов ясно виден из данных табл. 84, показывающих изменения веса свеклы и заливки в абсолютных величинах (в г).
С 1-го до 5-го дня ферментации происходит впитывание воды свеклой, причем количество воды уменьшается в большей мере, чем впитывает свекла, так как часть воды испаряется из открытых
|
ТАБЛИЦА 84
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {141} |
банок. На 10-й день уже заметен обратный процесс — диффузия сока в заливку (воду) — и процесс этот продолжается до конца опыта: свекла теряет в своем весе больше, чем прибавляется вес заливки, вследствие испарения части воды.
По истечении 60 дней общий вес бродящей массы уменьшился вследствие испарения воды на 9,7%, количество заливки (воды) уменьшилось на 22%, а вес свеклы увеличился на 14,9%. Абсолютные числа лучше характеризуют изменение баланса заливки свеклы: воды из заливки уменьшилось на 77 г, из которых затрачено на испарение 50,4 г и 26,6 г впитала свекла.
С прибавлением в заливку 4% соли первоначальный осмос и последующая диффузия проходят медленнее и в бродящей массе между свеклой и заливкой не происходит таких значительных весовых и объемных изменений. С увеличением содержания соли в заливке, учитывая водопоглощающую способность соли, можно вызвать в первые дни брожения осмос сока из свеклы в заливку, как это мы наблюдали в огурцах.
Анализируя данные по квашению свеклы, следует сделать такие практические выводы.
Квашение надо проводить при низких температурах, близких к 0°, чтобы сделать основным молочнокислое брожение и подавить спиртовое и другие виды побочных брожений. Это приведет к значительному накоплению молочной кислоты, лучшему качеству и хорошей сохранности продукта.
В процессе ферментации свекла значительно увеличивается в объеме. Параллельно с увеличением объема свеклы увеличивается и ее вес.
Квашение свеклы следует вести с применением соли, так как при этом условии в ней сохраняется больше сухих веществ, витамина С, больше накопляется молочной кислоты и меньше летучих кислот.
Морковь (Daucus carota L.) представляет собой ценный в пищевом отношении корнеплод, значение которого определяется в основном наличием сахаров, эфирных масел и значительного количества каротина. Содержание всех этих и других составных веществ значительно колеблется по сортам и климатическим зонам, а также находится в зависимости от состава почв и агротехники выращивания. Химический состав разных сортов моркови, по данным Ф. В. Церевитинова, приведен в табл. 85.
Состав моркови по отдельным сортам колеблется довольно значительно: содержание сухих веществ — от 10,07 до 15,50%, общего количества сахаров — от 4,52 до 7,78%, азотистых веществ — от 0,63 до 1,90%, клетчатки — от 1,05 до 2,11% и минеральных веществ — от 0,62 до 1,10%.
| {142} |
|
ТАБЛИЦА 85
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
На химический состав моркови влияют климатические условия ее произрастания, что подтверждается данными биохимической лаборатории Всесоюзного института растениеводства, приведенными в табл. 86.
|
ТАБЛИЦА 86
| ||||||||||||||||||||||||||||||||||||||||||||||||
Данные ВИР показывают, что морковь одних и тех же хозяйственно-ботанических сортов, выращенная на юге, содержит всех сахаров примерно на 50% больше, чем северная.
Южная морковь богата сахарозой, которая преобладает в общем количестве сахаров, тогда как в северной моркови преобладает инвертный сахар, а сахароза составляет всего лишь от 21,1 до 29% всех сахаров. Вес корня южной моркови в три-четыре раза более северной тех же сортов.
В составе азотистых веществ моркови более половины составляют белки, а меньшую часть — амиды и другие азотистые соединения; следовательно, белков в моркови содержится примерно от 0,4 до 1,0%.
А. А. Колесник установил в моркови содержание каротина от 0,050 до 0,077% на сухое вещество корня, витамина С — от 4,7 до 14,6 мг%. По данным В. Н. Букина, в моркови содержится {143} витамина А 62,5 гаммы в 1 г или, что то же, 6,25 мг в 100 г.
По исследованиям многих авторов в моркови имеются также витамины В1 и В2.
Морковь заквашивается в небольших количествах, главным образом с целью получения полуфабриката для овощных маринадов. Единой технологии квашения моркови не существует; ее квасят, заливая солевыми растворами крепостью 3–5% и 8–10%, а иногда и в чистой воде. В зависимости от концентрации соли в рассоле квашеная морковь приобретает различные вкусовые достоинства, обусловливаемые различием химического состава.
В табл. 87 приведены данные наших исследований о химическом составе заквашенной разными способами моркови (морковь сорта нантская, средняя температура ферментации 13,4°, продолжительность 30 суток).
|
ТАБЛИЦА 87
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Анализ данных этих исследований приводит к заключению, что более направленное молочнокислое брожение проходит при заливке моркови рассолом. В моркови, квашенной в чистой воде, сахара осталось всего 0,12%, а кислоты образовалось 0,54%, тогда как в моркови, залитой 4- и 8%-ным рассолами, осталось сахара, соответственно, 0,87 и 1,44% и образовалось кислоты 0,81 и 0,84%. Об этом же свидетельствует и содержание летучих кислот: при квашении в воде их накопилось 0,11, а в рассолах 0,04–0,05. Если также учесть, что квашение в рассолах диет возможность сохранить и витамин С на 60,5–71,2% его содержания в свежей моркови, то окажется, что квашение в рассолах приводит не только к большей направленности процесса, но и к лучшему химическому составу квашеного продукта. Наличие кислоты в количестве 0,81–0,84% в сочетании с солью дает возможность сохранять квашеный продукт. Морковь же, {144} заквашенная в воде, с наличием 0,54% кислоты сохраняться не может, так как быстрое развитие плесеневой пленки разрушает кислоту, вследствие чего могут возникнуть процессы гниения.
Сравнивая квашение в солевых растворах разной концентрации, надо отдать предпочтение химическому составу моркови, заквашенной в 8%-ном рассоле.
При квашении моркови изменяются не только химический состав, но и физические свойства.
В табл. 88 показано изменение физических свойств квашеной моркови в сравнении со свежей.
|
ТАБЛИЦА 88
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Морковь, заквашенная в чистой воде, несколько увеличилась в объеме и весе, тогда как морковь, заквашенная в рассолах, уменьшилась и в объеме и в весе. При этом целая морковь в 4%-ном рассоле потеряла в весе 4%, а в 8%-ном рассоле — 6,1%.
На моркови, разрезанной на части, резче сказываются общие тенденции изменения объема и веса: в чистой воде они больше увеличиваются, чем целый корень, а в рассоле сильнее уменьшаются.
Воздух, находящийся в тканях свежей моркови, в квашеной замещен в большей своей части заливкой. Вследствие этого увеличивается вес квашеных корнеплодов.
Проведенные исследования дают основание сделать практические выводы, что квасить морковь следует целыми корнями и в рассолах, а не в чистой воде. В зависимости от дальнейшего применения моркови ее можно квасить в рассолах с концентрацией соли от 4 до 8%. Квашение в более слабых рассолах приведет к малому накоплению кислоты, а в более крепких — к повышению содержания соли, что ухудшит качество квашеного продукта. Кроме того, применение более крепких рассолов вызовет большие весовые потери.
| {145} |
Арбузы (Citrullus vulgaris Schard) всегда пользовались большим спросом со стороны потребителей как вкусные, сладкие, с освежающей мякотью плоды. Они по праву могут быть названы полевыми фруктами.
В химическом составе арбузов преобладают сахара, содержание которых колеблется от 6 до 11%. Из сахара больше половины приходится на долю фруктозы, около 15% составляет сахароза и примерно одну треть глюкоза. Вследствие преобладания наиболее сладких сахаров арбузы по ощущению сладости превосходят многие фрукты.
Из других веществ в арбузах, по данным Ф. В. Церевитинова, найдено (в процентах): азотистых веществ — 0,76, клетчатки — 0,4, минеральных веществ (золы) — 0,36, кислоты (яблочной) — 0,06 и жира — 0,6. В. Н. Букин приводит такое содержание витаминов в арбузах (в мг%): витамина А — 1–1,1, витамина B — 0,04–0,08 и витамина С — 5–10.
Естественно желание и стремление многих потребителей и производственников консервировать арбузы солением для получения не менее вкусного продукта в зимнее время.
Однако далеко не всегда засоленные арбузы получаются хорошего качества. Очень часто соленые арбузы теряют свою первоначальную форму, имеют вмятины или превращаются в лепешку, мякоть внутри дряблая, осклизлая. Иногда при разрезании хорошего по внешнему виду арбуза из него выходит много газов, а вся суховатая мякоть прижата к кожице и не имеет никакого вкуса. Неудачи при засолке арбузов постигают не только впервые берущихся за это дело, но и опытных производственников.
Этими неудачами в засолке арбузов, видимо, вызвано широкое искание способов наилучшего их приготовления. Искания эти, к сожалению, ограничиваются только кругом непосредственных потребителей и любителей — мастеров-производственников.
Научных исследований в области засолки арбузов нет и, несмотря на наличие многочисленных практических рецептур, нет возможности рекомендовать такую технологию соления, которая гарантировала бы получение арбузов всегда высокого качества. До сих пор еще не выяснены достаточно микробиологические процессы, происходящие в арбузах при солении разными способами, не установлены факторы, способствующие сохранению хорошей структуры мякоти арбузов и получению продукта высоких вкусовых достоинств.
Существующие производственные инструкции разных ведомств по солению арбузов характерны отсутствием обоснованности устанавливаемой ими технологии в целом и отдельных ее процессов. По одним инструкциям можно солить и крупные и мелкие арбузы, по другим — только мелких размеров. Одни инструкции рекомендуют накалывать арбузы перед засолкой, другие — не {146} рекомендуют. Одни предлагают заливать арбузы рассолом крепостью 8–12%, другие — 1–3%. Одни считают необходимым вести ферментацию арбузов на холоду, другие — не указывают никаких особенностей ферментации.
Среди непромышленных рецептур потребительского характера следует еще отметить соление арбузов в песке, в арбузной мякоти, в соломе, с поспой, с прибавлением сахара в заливку со специями — гвоздикой и корицей и пр.
Все существующие способы консервирования арбузов молочнокислым брожением по количеству вводимой соли и вызываемой этим направленностью брожения можно разбить на две группы: мочение и соление арбузов. При мочении арбузы заливают 2–4%-ным раствором соли; в консервированном виде они обладают приятным сладко-кислым вкусом с солоноватым привкусом. При солении арбузы заливают 8–12%-ным рассолом; в готовом виде они имеют кисло-соленый вкус, не характерный для арбузов.
Не располагая специальными исследованиями по солению арбузов, мы попытались обобщить опыт практиков и дать объяснение некоторым явлениям.
Прежде всего, следует обратить внимание на то обстоятельство, что арбузы отличаются непрочной структурой мякоти, в которой очень мало коллоидов и клетчатки. Некоторое представление об этом дает сравнение содержания азотистых веществ и клетчатки в арбузах с другими рассмотренными овощами — свеклой, морковью, огурцами (см. табл. 89).
|
ТАБЛИЦА 89
| |||||||||||||||||
В арбузах меньше, чем в других овощах, азотистых веществ и клетчатки. Но и из этого небольшого количества клетчатки, по данным М. И. Княгиничева, в мякоти плода ее содержится всего 0,04%, а остальное количество сосредоточено в кожуре. К сожалению, нет исследований состава азотистых веществ и, следовательно, неизвестно, какое место среди них занимают белки — истинные коллоиды. Но если они составляют даже 50%, то становится очевидной сравнительная бедность ими арбузов. В огурцах белки составляют 65% и больше половины в свекле и моркови.
Ничтожное содержание коллоидов при крайне незначительном количестве клетчатки требует иной технологии соления, арбузов {147} по сравнению с огурцами. Между тем по производственным инструкциям ферментация арбузов и огурцов должна проводиться одинаково.
Выяснение причин образования пустот в арбузах и вследствие этого потери ими формы и сочности мякоти привело нас к выводу, что в процессе брожения в арбузах, богатых сахарами, активно развивается спиртовое брожение. В результате этого внутри плодов накапливается значительное количество газов, задерживающихся плотной оболочкой, пропитанной воскоподобными веществами. Количество газов увеличивается молочнокислым брожением, вызываемым газообразующими бактериями. Образовавшиеся внутри плодов газы разрывают мякоть, уплотняя ее и прижимая к коре. Если газы находят выход, внутреннее давление ослабляется и вследствие образовавшихся пустот плоды теряют форму.
Чтобы не допустить этих явлений, необходимо при ферментации арбузов избегать, прежде всего, спиртового брожения и не допускать энергичного молочнокислого, которое тоже может привести к значительному накоплению углекислого газа. Этого можно достичь только проведением ферментации арбузов на холоду, при температуре от 0 до +5°. При такой температуре спиртовое брожение будет подавлено, а молочнокислое будет проходить медленно, не вызывая скопления большого количества газов.
В этом свете становятся понятными удачи мастеров и отдельных потребителей, которые солят арбузы только в ледниках или в холодных подвалах.
Большое значение имело бы применение при солке арбузов чистых культур тех рас молочнокислых бактерий, которые не образуют газов.
Что касается влияния величины плодов на качество соленых арбузов, то учет положительного опыта практиков дает на это прямой ответ: лучшая продукция получается при засолке мелких плодов. В этих случаях хорошо сохраняется форма плодов и мякоть остается сочной, пропитанной рассолом (при ферментации на холоде).
Этот факт может быть объясним только тем, что в мелких арбузах быстрее проходят процессы диффузии, что способствует прекращению в плодах биохимических процессов на ранней стадии брожения. Это подтверждают простые математические расчеты.
Очевидно, что арбузная масса тем быстрее будет пропитываться рассолом, чем больше поверхности плода приходится на единицу массы.
В арбузах, имеющих форму шара, отношение поверхности к объему следующее:
S V |
= |
4πR2 4/3πR3 |
= |
3 R |
. |
| {148} |
Иначе говоря, количество квадратных сантиметров поверхности, приходящихся на один кубический сантиметр массы, обратно пропорционально радиусу. Следовательно, чем мельче арбуз, тем больше поверхности приходится на единицу его массы. Вот некоторые расчеты:
Диаметр |
Количество см2 |
|
10 |
0,6 |
|
15 |
0,4 |
|
20 |
0,3 |
|
25 |
0,24 |
|
30 |
0,2 |
Эти расчеты достаточно наглядно показывают, что мелкий арбуз, диаметром в 10 см, располагает втрое большей относительной поверхностью, чем крупный арбуз, диаметром в 30 см. Естественно, что масса мелкого арбуза будет просаливаться быстрее. А это очень важно, так как при этом быстрее погибает живая клетка, прекращается ее жизнедеятельность. Арбузы, залитые рассолом, находятся в анаэробных условиях; вследствие этого до просаливания развивается интрамолекулярное дыхание с накоплением спирта и газов, что ведет к разрушению мякоти. Быстрое проникновение в арбузы рассола приостанавливает развитие этого явления и все другие биохимические процессы при условии проведения ферментации в низких температурах.
Правда, при солении арбузов, даже мелких, можно говорить лишь об относительной быстроте проникновения рассола внутрь плодов. Дело в том, что арбузы имеют шарообразную форму. А шар, как известно, обладает наиболее экономной поверхностью по отношению к заключенной в ней массе. Это обстоятельство, а также наличие толстой коры, пропитанной большим количеством воскоподобных веществ (0,6%), и являются одним из основных причин неудач при засолке арбузов.
Если сравнить удельную поверхность огурцов (количество квадратных сантиметров поверхности на 1 см3 объема или массы) с удельной поверхностью арбузов, то окажется, что самые мелкие, т. е. наилучшие для засолки, арбузы имеют удельную поверхность в 1,4 раза меньшую, чем самые крупные и худшие для засолки огурцы. Так, наиболее мелкие огурцы, лучшие в засолке, имеют удельную поверхность 2,4 см2, а наиболее крупные, худшие в солении, — 0,86 см2 (см. табл. 10). В то же время удельная поверхность самых мелких арбузов составляет всего 0,6 см2, а наиболее крупных — 0,2 см2. Если же сопоставить удельные поверхности огурцов и арбузов самых мелких и самых крупных, то окажется, что удельная поверхность арбузов в четыре раза меньше поверхности огурцов. {149}
Сопоставление этих фактов дает возможность понять причину более медленной усолки арбузов по сравнению с огурцами при одинаковых температурах брожения. Пока рассол из заливки успеет проникнуть внутрь арбузной ткани, интрамолекулярное дыхание и других биохимические процессы уже произведут в ней свое разрушительное действие. Отсюда следует, что технологию соления арбузов надо разработать с учетом этого фактора. В арбузах необходимо затормозить все ферментативные процессы, свойственные живой ткани, для чего не только следует проводить их засолку на холоду, а возможно даже предварительно охлаждать плоды на леднике или в холодильнике.
Рекомендуемая некоторыми инструкциями наколка арбузов, которая, по мысли авторов, должна ускорить ферментацию, не дала положительных результатов. Возможно, более эффективной была бы промывка плодов в легких щелочных растворах для удаления с коры воскоподобных веществ, что должно облегчить диффузию. Но это требует экспериментальной проверка.
Мы наблюдали, что при засолке огурцов, заливаемых 6–8–10%-ным рассолом, вследствие небольшого содержания в них растворимых веществ (2–3%) в первые дни ферментации происходит энергичный осмос огуречного сока в рассол. В квашении свеклы, заливаемой 4%-ным рассолом, в первые дни брожения рассол проникает в свеклу, так как в ней содержится свыше 10% сухих веществ. Таким образом, первичное направление диффузионных процессов — от меньшей концентрации к большей. Это надо учесть при солении арбузов и, учитывая непрочную структуру их мякоти, ни в коем случае не допускать, чтобы первичное движение соков было из арбузов в рассол. Арбузы не обладают такими коллоидами, как огурцы, и, потеряв сок, не в состоянии будут обратно его впитывать. Поэтому обезвоживание арбузной мякоти равносильно ее разрушению. Необходимо, чтобы технология их соления предусматривала первичную диффузию из рассола в плоды.
Такое первичное направление диффузии может быть обеспечено только в том случае, если концентрация сухих веществ в заливке будет значительно меньше их концентрации в арбузном соке.
В связи с бесспорной необходимостью первичной диффузии в направлении от заливки в плоды становится сомнительной целесообразность квашения арбузов в арбузной массе и арбузном соку. В арбузной массе, к которой прибавляется 2–3% соли, создается концентрация сухих веществ большая, чем в плодах. Это неминуемо должно привести к первичной диффузии соков из плодов в заливку, что должно вызвать, по крайней мере, частичное разрушение мякоти плодов и появление плодов с вмятинами. В данном случае плоды могут подвергаться меньшей деформации, чем в других случаях с таким же направлением первичной диффузии, так как вследствие незначительной разницы в концентрациях {150} сухих веществ плодов и окружающей их мякоти осмос сока будет замедленным, вследствие чего на ранней стадии брожения наступит и обратная диффузия сока из заливки в плоды. Однако этот способ квашения не может гарантировать сохранения в целости плодовой мякоти арбузов.
Наоборот, способ соления арбузов в песке с заливкой их 2–3%-ным раствором соли создает все предпосылки для направления первичной диффузии из заливки в плоды, что будет способствовать набуханию и сохранению от разрушения арбузной мякоти. Засолка арбузов с пересыпкой их песком хороша еще и тем, что при этом заливки приходится добавлять в бочки незначительное количество, так как пространства между арбузами в бочке заняты песком.
Вследствие небольшого содержания заливки в бочках вторичная диффузия сока из арбузов в заливку не вызывает значительного выщелачивания сахаров арбузов до уравновешивания концентраций сухих веществ в обеих фазах (плоды — заливка). В результате арбузы сохраняют много сахаров, а с ними и приятный освежающий вкус.
Наконец, следует сделать вывод об очевидной неэффективности соления арбузов с заливкой их рассолами 8–12%-ной крепости. При таком способе консервирования неизбежен первичный осмос сока из плодов в заливку, а вместе с ним и разрушение мякоти плодов. К тому же, при этом способе посола из плодов арбузов выщелачивается примерно 50% сахаров (учитывая, что в бочках рассола по весу находится примерно столько же, сколько и арбузов).
Вследствие большого понижения концентрации сахаров они полностью или почти полностью перебраживают и соленые арбузы приобретают кисло-соленый вкус, совершенно не характерный для арбузов.
Таким образом, теоретический анализ положительного и отрицательного опыта практики соления арбузов приводит к таким выводам:
1. При солении арбузов надо избегать газообразования, что достигается их ферментацией и дальнейшим хранением при низких температурах — от 0 до +5°, которыми подавляется спиртовое брожение.
2. Из этих же соображений желательно вести квашение арбузов чистыми культурами негазообразующих молочнокислых бактерий.
3. Для соления следует отбирать только мелкие арбузы, чтобы мякоть быстрее пропитывалась консервирующими веществами, что прекращает жизнедеятельность плодовой ткани и способствует фиксации ее структуры.
4. В процессе соления по любым технологическим схемам и рецептурам должно быть обеспечено первичное движение соков из заливки в плоды, так как обратное первичное движение соков {151} вследствие непрочной структуры плодовой мякоти вызывает ее разрушение.
5. На этом основании следует рекомендовать заливку арбузов рассолами с меньшей концентрацией сухих веществ, чем в арбузах (2–4% соли), и отказаться от крепких рассолов (8–12%), что вызывает разрушение плодовой мякоти.
Консервирование арбузов нуждается в экспериментальном научном изучении для обоснования рациональной технологии такой трудной для соления культуры, как арбузы.
| {152} |
ЛИТЕРАТУРА
1. | Авраменко П., Консервування огiркiв без охолодження. Держсiльгоспвидав Украiни, 1931 р. |
2. | Алеев Б. С. и Чистяков Ф. М.. Микробиология консервирования, часть III, Пищепромиздат, 1945 г. |
3. | Бычков П. А., Организация и техника заготовки овощей, Госторгиздат, 1938 г. |
4. | Букин В. Н., Витамины, Пищепромиздат, изд. II, 1941 г. |
5. | Будыко М. И., Испарение в естественных условиях, Гидрометеоиздат, 1948 г. |
6. | Беляева В. А., Пряновкусовые растения, Госторгиздат, 1946 г. |
7. | Веселовский И. А., Макарова М. М. и Кирьялов Н. П., Использование молочнокислых бактерий при квашении капусты. Журн. «Сад и огород» № 7, 1947 г. |
8. | Вячеславов А. Н., Переработка плодов и овощей, Госторгиздат, 1939 г. |
9. | Войткевич А. Ф. (ред.), Курс микробиологии, Сельхозгиз, 1940 г. |
10. | Васильев В. Ф. и Кисис А. Д., Эфиромасличные растения, Воронежский сельскохозяйственный институт, т. 1-й, 1939 г. |
11. | Вульф Е. В. и Нилов В. И., (редакторы), Эфиромасличные растения, их культура и эфирные масла, Пищепромиздат, т. 3-й, 1937 г. |
12. | Всеукраинский научно-исследовательский институт ферментативной и плодоовощной промышленности. Бюллетень № 4, апрель 1933 г. |
13. | Всеукраiнський науково-дослiдний iнститут плодоовочевоi промисловости. Збiрник iнструкцiй, Киiв, 1931 р. |
14. | Габаев С. Г., Огурцы, Сельхозгиз, 1932 г. |
15. | Токин Б. В., Фитонциды, изд. Академии медицинских наук СССР, 1951 г. |
16. | Гребинский С. О., Биохимия капусты. Биохимия культурных растений, т. IV. Сельхозгиз, 1938 г. |
17. | Герасимов Ф. П., Ростовский способ засолки огурцов. Журн. «Новая деревня» № 17, 1929 г. |
18. | Думанский А. В., Учение о коллоидах, Государственный научно-исследовательский институт коллоидной химии, Воронеж, 1937 г. |
19. | Думанский А. В., Коллоидная химия в пищевой промышленности. Журнал «Пищевая промышленность СССР», № 10, 1944 г. |
20. | Дуброва Г. Б., Действие фитонцидов чеснока на плесневые грибы. Журн. «Микробиология», т. XIX, вып. 3, изд. Академии наук СССР, 1950 г. |
21. | Жилинский С. В., Душистые растения, их сбор и заготовка, Сельхозгиз, 1932 г. |
22. | 3ахаревич Н. И., Огурцы, Сельхозгиз, 1942 г. |
23. | Иванов Н. Н. (редактор), Биохимия культурных растений, том IV, Сельхозгиз, 1938 г. {153} |
24. | Каменев А. и Клименко К., Матерiалы до вивчения нiжинського огiрка та засобiв його солiння. Записки Нiжинського iнституту народньоi освiти ИНХ, 1930 р. |
25. | Каменев А. А., Сборник работ Всесоюзного научно-исследовательского института плодоовощной промышленности за 1937 г., Киев 1939 г. |
26. | Кичунов Н. И., Огурцы, дыни, тыквы, СПБ, 1910 г. |
27. | Костычев С. П., Физиология растений, т. 1, Сельхозгиз, 1937 г. |
28. | Коган Ф. Я., За улучшение качества соленых огурцов. Журн. «Плодоовощное хозяйство» № 7, 1935 г. |
29. | Колесник А. А., Изменение содержания витамина С в картофеле и моркови в процессе хранения. Сборник научных трудов Института народного хозяйства им. Г. В. Плеханова, Госторгиздат, 1947 г. |
30. | Кедроливанский В. Н., Метеорологические приборы, Гидрометеоиздат, 1947 г. |
31. | Лавров Б. А., Учебник физиологии питания, Биомедиздат, 1935 г. |
32. | Любченко Г. М., Найпростiша переробка й зберiгания плодiв та овочiв. Сiльгоспвидав УРСР, 1947 р. |
33. | Лыков А. В. и Ауэрман Л. Я., Теория сушки капиллярно пористых коллоидных материалов пищевой промышленности, Пищепромиздат, 1948 г. |
34. | Мельман М. Е., Основы технологии соления огурцов. Укртехиздат, 1948 г. |
35. | Мельман М. Е., О естественных изменениях в весе огурцов при брожении. Журн. «Консервная и плодоовощная промышленность», № 4, 1940 г. |
36. | Мельман М. Е., О нормах убыли соленых огурцов, Научные записки Харьковского института советской торговли, т. 1, Харьков, 1941 г. |
37. | Муppи И. К., Биохимия культурных растений, т. IV, Сельхозгиз, 1938 г. |
38. | Мушкатин С. Е., Простейшие способы переработки плодов, овощей и ягод, Пищепромиздат, 1933 г. |
39. | Моркович И., Переработка овощей. Журн. «Вопросы советской торговли», № 10, 1939 г. |
40. | Марков А. В., Хранение солений и маринадов, Снабтехиздат, 1934 г. |
41. | Марков А. В., Засолка огурцов в дошниках, Снабтехиздат, 1934 г. |
42. | Никитинский Я. Я. и Алеев Б. С, Микробиология скоропортящихся продуктов, Снабтехиздат, 1934 г. |
43. | Hiкiтiн В. Н., Огiрки, Сiльгоспвидав УРСР, 1931 р. |
44. | НИИТОП, Хранение и переработка овощей, Госторгиздат, 1945 г. |
45. | Опарин А. И., Происхождение жизни, Военное издательство, Москва. 1948 г. |
46. | Обухов А. Н. и Понпа Д. Л., Пряное сырье СССР, Пищепромиздат, 1936 г. |
47. | Павлов И. П. (редактор), Сортоведение овощных культур, Сельхозгиз, 1933 г. |
48. | Панфилов С., Микробиология молока и молочных продуктов, Харьков, Советский крестьянин, 1930 г. |
49. | Палей Т. Я., Противоцынготная активность квашеной капусты. Журн. «Консервная и плодоовощная промышленность», № 5, 1938 г. |
50. | Пигулевский Г. В. (редактор), Эфирные масла, Пищепромиздат, 1938 г. |
51. | Рубин Б. А. и Старчицкий К. И., О содержании антицынготного витамина в овощах. Журн. «Плодоовощное хозяйство», № 4, 1936 г. {154} |
52. | Рытов М. В., Огородничество, Сяйво, 1925 г. |
53. | Раевский Н. И., Простейшие способы переработки овощей, Сельхозиздат, 1937 г. |
54. | Рутовский, Эфирные масла, Пищепромиздат, т. 1-й, 1931 г. |
55. | Рагулин Н. Г., Сортовые различия огурцов и их значение при засолке. Журн. «Консервная и плодоовощная промышленность» № 5, 1939 г. |
56. | Ситников А. П., Микробиология брожения, Пищепромиздат, 1936 г. |
57. | Сорокин П. Г., Хранение и переработка плодов и овощей, Сельхозгиз, 1947 г. |
58. | Семенов В., О квашении капусты. Журн. «Плодоовощное дело», № 7–8, 1930 г. |
59. | Соколова В. Т. и Черникова З. В., Витамин С в свежих овощах Западной Сибири. Сборник работ Новосибирского научно-исследовательского института питания, 1938 г. |
60. | Саруханян Ф. Г. и Киримян Р. С, О микрофлоре квашеных овощей. Микробиологический сборник, вып. II, Академия наук Армянской ССР, Ереван, 1946 г. |
61. | Садановский М. В., Характеристика некоторых эфиромасляничных и лекарственных растений Украины, «Научно-агрономический журнал», № 1, 1930 г. |
62. | Столетов Е. А., Кориандр, Всесоюзная академия сельскохозяйственных наук им. Ленина, 1931 г. |
63. | Сперанский В. Г. и др., Товароведение пищевых товаров, том 2, Госторгиздат, 1949 г. |
64. | Токин Б. П., Биологическая роль фитонцидов. Сборник научных исследований об антисептиках растительного происхождения, Томск, изд. «Красное знамя», 1944 г. |
65. | Титоренко Г. К., Химико-микробиологический контроль квашения капусты без трамбовки и гнета. Сборник работ Всесоюзного научно-исследовательского института плодоовощной промышленности за 1957 г., Киев, 1939 г. |
66. | Техническая энциклопедия. Справочник физических, химических и технологических величин. Том VII, Огиз, 1931 г. |
67. | Укрглавплодоконсерв. Переработка плодов и овощей, Госсельхозиздат УССР, Киев, 1947 г. |
68. | Xарузин А. Н., Огурцы, дыни, тыквы. Сельхозгиз, 1928 г. |
69. | Церевитинов Ф. В., Химия и товароведение свежих плодов и овощей, изд. 3-е, тт. I и II, Госторгиздат, 1949 г. |
70. | Церевитинов Ф. В. (редактор), Технология переработки плодов и овощей, Госторгиздат, 1945 г. |
71. | Церевитинов Ф. В., Химия свежих плодов и овощей, изд. 2-е, Издательство колхозной и совхозной литературы, 1933 г. |
72. | Церевитинов Ф. В., Микодерма, появляющаяся на соленых и других продуктах. Журн. «Консервная и плодоовощная промышленность», № 4, 1940 г. |
73. | Церевитинов С. Ф. и Метлицкий А. В., Товароведение плодов и овощей и продуктов их переработки, Госторгиздат, 1939 г. |
74. | Шугаевская П. Г., Квашение огурцов и капусты чистыми культурами. Сборник работ Всесоюзного научно-исследовательского института плодоовощной промышленности за 1937 г., Киев, 1939 г. |
75. | Шугаевская П. Г., Ослизнение огуречных рассолов. Журн. «Консервная и плодоовощная промышленность», № 5, 1938 г. {155} |
76. | Шалимова М. П., Характеристика специй, применяемых для соления огурцов. Научные записки Харьковского института советской торговли, т. 1, Харьков, 1941 г. |
77. | Ярусова Н. С., Материалы к оценке противоцынготной активности некоторых продуктов. Журн. «Вопросы питания», № 5, 1937 г. |
78. | Якимович А. Д. и Шереметьевский П. В., Огурцы, Сельхозгиз, 1933 г. |
79. | Якубец-Якубчик Е. I., Лiкарсько-технiчнi рослини Украiни, Сiльгоспвидав, 1930 р. |
80. | Руководство по аппробации сельскохозяйственных культур, т. V, Огиз — Сельхозгиз, 1948 г. |
81. | Справочник агронома-овощевода, Огиз—Сельсозгиз, 1947 г. |
| {156} |
1 Отношение длины к толщине называют также индексом формы (см. табл. 3).
1 Н. Г. Рагулин, Сортовые различия огурцов и их значение при засолке, журнал «Консервная и плодоовощная промышленность», 1939, № 5.
2 Данные взяты из «Руководства по аппробации сельскохозяйственных культур», т. V, Сельхозгиз, 1948.
1 Для исследования взяты огурцы сорта нежинские размеров 91–120 мм в таре емкостью 18 л.
1 Детальная инструкция по солению огурцов, разработанная плодоовощной лабораторией НИИТОП с учетом многих современных исследований в этой области, утверждена Министерством торговли Союза ССР для руководства.
1 Данные взяты из книги А. Н. Вячеславова «Переработка плодов и овощей», Госторгиздат, 1939, стр. 75.
2 Рассчитано на основании изменений емкости тары.
1 Главный технолог Укрторгплодоовощтреста.
| {158} |
Обложка художника М. Н. Симакова
Редактор Е. Г. Нечаева
Техн. редактор Д. М. Медриш
Л-30114. Сдано в набор 28 IX 1951 г. Подписано
к печати 16 II 1952 г. Формат 60×921/16. Бум.
л. 5. Печ. л. 10. Уч.-изд. л. 11,42. Авторск. л. 11,07
Тираж 8000 экз. Заказ № 3249.
Типография «Юхисэлу», Таллин, Пикк, 40.